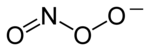
 Химическая структура аниона пероксинитрита | |
| Имена | |
|---|---|
| Название ИЮПАК Оксидонитрит | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| КЕГГ | |
PubChem CID | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| N O 3 - | |
| Молярная масса | 62,005 г · моль -1 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Пероксинитрит (иногда называемый пероксонитритом ) - это ион с формулой ONOO - . Это неустойчивый структурный изомер из нитрата , NO-
3. Хотя его сопряженная кислота пероксинизотистая кислота обладает высокой реакционной способностью, пероксинитрит стабилен в щелочных растворах. [1] [2] Его получают реакцией перекиси водорода с нитритом :
- Н 2 О 2 + НЕТ-
2→ ОНОО - + Н 2 О
Пероксинитрит - окислитель и нитрующий агент. Из-за своих окислительных свойств пероксинитрит может повреждать широкий спектр молекул в клетках , включая ДНК и белки . Образование пероксинитрита in vivo приписывают реакции свободнорадикального супероксида со свободнорадикальным оксидом азота : [3] [4]
- О• -
2+ НЕТ • → ONO-
2
В результате образования пары этих двух свободных радикалов образуется пероксинитрит, молекула, которая сама по себе не является свободным радикалом, но является мощным окислителем.
В лаборатории раствор пероксинитрита можно приготовить путем обработки подкисленной перекиси водорода раствором нитрита натрия с последующим быстрым добавлением NaOH. Его концентрация указывается оптической плотностью при 302 нм (pH 12, ε 302 = 1670 M -1 см -1 ). [5]
Как нуклеофил [ править ]
ONOO - нуклеофильно реагирует с диоксидом углерода . In vivo концентрация углекислого газа составляет около 1 мМ, и его реакция с ONOO - происходит быстро. Таким образом, в физиологических условиях реакция ONOO - с диоксидом углерода с образованием нитрозопероксикарбоната ( ONOOCO-
2), безусловно, является преобладающим путем для ONOO - . ONOOCO-
2гомолизируется с образованием карбонатного радикала и диоксида азота снова в виде пары радикалов в клетке . Примерно в 66% случаев эти два радикала рекомбинируют с образованием диоксида углерода и нитрата. В остальных 33% случаев эти два радикала покидают клетку растворителя и становятся свободными радикалами. Считается, что именно эти радикалы ( карбонатный радикал и диоксид азота ) вызывают повреждение клеток, связанное с пероксинитритом.
Пероксинизотистая кислота [ править ]
Пероксиазотистая кислота (HNO 3 ) является химически активным азотсодержащим веществом. Это конъюгированная кислота пероксинитрита. Его p K a составляет ~ 6,8.
См. Также [ править ]
- Нитротирозин
- Активные формы азота
Ссылки [ править ]
- ^ Holleman, AF; Виберг, E.Академическая пресса неорганической химии : Сан-Диего, 2001. ISBN 0-12-352651-5 .
- ^ Коппенол, W. H (1998). «Химия пероксинитрита, биологического токсина <a name=TOP1> </a>» . Química Nova . 21 (3): 326–331. DOI : 10.1590 / S0100-40421998000300014 .
- ^ Пачер, P; Бекман, Дж. С; Liaudet, L (2007). «Оксид азота и пероксинитрит в здоровье и болезни» . Физиологические обзоры . 87 (1): 315–424. DOI : 10.1152 / Physrev.00029.2006 . PMC 2248324 . PMID 17237348 .
- ^ Сабо, C; Ischiropoulos, H; Ради, Р. (2007). «Пероксинитрит: биохимия, патофизиология и разработка терапевтических средств». Обзоры природы Открытие лекарств . 6 (8): 662–80. DOI : 10.1038 / nrd2222 . PMID 17667957 .
- ^ Бекман, Дж. С; Коппенол, В. Х (1996). «Оксид азота, супероксид и пероксинитрит: хорошее, плохое и уродливое». Американский журнал физиологии. Клеточная физиология . 271 (5, часть 1): C1424–37. DOI : 10.1152 / ajpcell.1996.271.5.C1424 . PMID 8944624 .
