 | |
 | |
| Имена | |
|---|---|
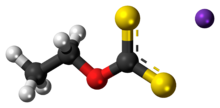
| Предпочтительное название IUPAC О- этилкарбонодитиоат калия | |
| Другие названия Калий ethylxanthogenate калий- O - этил дитиокарбонат | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.004.946 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| С 3 Н 5 К О С 2 | |
| Молярная масса | 160,29 г · моль -1 |
| Появление | Бледно-желтый порошок |
| Плотность | 1,263 г / см 3 [1] |
| Температура плавления | От 225 до 226 ° C (от 437 до 439 ° F, от 498 до 499 K) |
| Точка кипения | разлагается |
| Кислотность (p K a ) | примерно 1,6 |
| Опасности | |
| R-фразы (устаревшие) | R15 R21 R22 R29 R36 R38 |
| S-фразы (устаревшие) | S3 S9 S35 S36 S37 S38 S39 S16 S23 S51 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Этилксантогенат калия (KEX) представляет собой сероорганическое соединение с химической формулой CH 3 CH 2 OCS 2 K. Это бледно-желтый порошок, который используется в горнодобывающей промышленности для разделения руд . В отличие от родственного этилксантогената натрия , калиевая соль существует в виде безводной соли.
Производство и свойства [ править ]
Ксантогенатные соли получают действием алкоксидов на сероуглерод . Алкоксид часто образуется in situ из гидроксида калия: [2]
- СН 3 СН 2 ОН + CS 2 + КОН → СН 3 СН 2 OCS 2 К + Н 2 О
Этилксантогенат калия представляет собой бледно-желтый порошок, который стабилен при высоком pH, но быстро гидролизуется при pH <9 при 25 ° C. В отличие от производного натрия, ксантогенат калия кристаллизуется в виде безводной соли и не гигроскопичен.
Приложения [ править ]
Этилксантогенат калия используется в горнодобывающей промышленности как флотационный агент для извлечения руд меди, никеля и серебра. [3] В методе используется сродство этих «мягких» металлов к сероорганическому лиганду.
Ксантогенат калия является полезным реагентом для получения сложных эфиров ксантогената из алкил- и арилгалогенидов. Полученные сложные эфиры ксантогената являются полезными промежуточными продуктами в органическом синтезе . [4]
Безопасность [ править ]
Составляет 683 мг / кг (перорально, крысы) для этилового калия ксантогената. [3] LD 50 {\ displaystyle {\ text {LD}} _ {50}}
Ссылки [ править ]
- ↑ Report 5 (1995) p. 5
- ↑ В этом отчете подробно описана процедура Чарльза К. Прайса и Гарднера В. Стейси (1948). «п-нитрофенил) сульфид» . Органический синтез . 28 : 82.; Сборник , 3 , с. 667
- ^ a b Катрин-Мария Рой (2005). «Ксантат». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a28_423 . ISBN 3527306730.
- ^ Одна из нескольких процедур с использованием ксантогенатных эфиров: Фабьен Гагош и Самир З. Зард (1948). «Подход Xanthate-Transfer для α-Trifluoromethylamines» . Органический синтез . 84 : 32.; Коллективный том , 11 , с. 212