| Имена | |||
|---|---|---|---|
| Название ИЮПАК пиридиний | |||
| Идентификаторы | |||
| |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
PubChem CID | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 5 H 6 N | |||
| Молярная масса | 80,110 г · моль -1 | ||
| Кислотность (p K a ) | ~ 5 (для конъюгированной кислоты) [1] [2] | ||
| Основание конъюгата | Пиридин | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
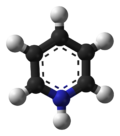
Пиридиний относится к катиону [C 5 H 5 NH] + . Это конъюгат кислоты из пиридина . Известно много родственных катионов, включая замещенные пиридины, например пиколины, лутидины, коллидины. Их получают обработкой пиридина кислотами. [3]
Поскольку пиридин часто используется в качестве органического основания в химических реакциях, соли пиридиния образуются во многих кислотно-основных реакциях. Его соли часто нерастворимы в органическом растворителе, поэтому осаждение комплекса уходящей группы пиридиния является показателем развития реакции. Ион пиридиния также играет роль в ацилировании Фриделя-Крафтса . Когда пиридин включен, он образует комплекс с электрофильным ионом ацилия , что делает его еще более реактивным.
Катионы пиридини являются ароматическими ионами, как определено с помощью правила Хюккеля . [4] Он изоэлектронен бензолу .
Катионы N- алкилпиридиния [ править ]
Когда кислотный протон заменяется алкилом , соединения называются N- алкилпиридинием. Простым представителем является N- метилпиридиний ([C 5 H 5 NCH 3 ] + ). С коммерческой точки зрения важным пиридиниевым соединением является гербицид паракват . [5]
См. Также [ править ]
- Пиридиний хлорхромат
- Пиридиний хлорид
Ссылки [ править ]
- ^ Линнелл, Роберт (1960). «Примечания - Константы диссоциации 2-замещенных пиридинов». Журнал органической химии . 25 (2): 290. DOI : 10.1021 / jo01072a623 .
- ^ Пирсон, Ральф G .; Уильямс, Форрест В. (1953). "Скорости ионизации псевдокислот. 1. Стерические эффекты в катализируемой основанием ионизации нитроэтана". Журнал Американского химического общества . 75 (13): 3073. DOI : 10.1021 / ja01109a008 .
- ^ Джордж А. Олах, Майкл Уоткинс (1978). «Фторирование с реагентом на основе фторида пиридиний-полигидроген: 1-фторадамантан». Орг. Synth . 58 : 75. DOI : 10,15227 / orgsyn.058.0075 .CS1 maint: использует параметр авторов ( ссылка )
- ^ «Ароматические соединения» (PDF) . Алекс Рош, Университет Рутгерса.
- ↑ Симидзу, Шинкичи; Ватанабэ, Нанао; Катаока, Тошиаки; Сёдзи, Такаяки; Абэ, Нобуюки; Моришита, Синджи; Ичимура, Хисао (2007). «Пиридин и производные пиридина». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a22_399 .