| пируватдегидрогеназа (переносящая ацетил) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Кристаллографическая структура пируватдегидрогеназы (ПДГ). PH представляет собой димер с шестью доменами, где области α (синий), α '(желтый), β (красный) и β' (бирюзовый) обозначены разными цветами. Пирофосфат тиамина (ТФФ) показан серым цветом в виде шарика и палочек, два иона магния фиолетовым цветом подвергаются металлической связи с ТФФ, а два иона калия - оранжевым. [1] | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 1.2.4.1 | ||||||||
| Количество CAS | 9014-20-4 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
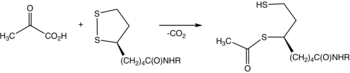
Пируватдегидрогеназа - это фермент, который катализирует реакцию пирувата и липоамида с образованием ацетилированного дигидролипоамида и диоксида углерода . Для преобразования необходим кофермент тиаминпирофосфат .
Пируватдегидрогеназа обычно встречается как компонент, называемый E1, пируватдегидрогеназного комплекса (PDC). PDC состоит из других ферментов, называемых E2 и E3. Совместно E1-E3 превращает пируват , NAD + , кофермент A в ацетил-CoA , CO 2 и NADH. Преобразование имеет решающее значение, потому что ацетил-КоА может затем использоваться в цикле лимонной кислоты для осуществления клеточного дыхания . [2] Чтобы отличить этот фермент от PDC, его систематически называют пируватдегидрогеназой (переносящая ацетил) .
Механизм [ править ]
Пирофосфат тиамина (TPP) превращается в илид путем депротонирования. Илид атакует кетонную группу пирувата. Образующиеся аддукты декарбоксилаты . Полученный 1,3-диполь восстанавливает ацетилирование липоамида-E2. [2]
Что касается деталей, биохимические и структурные данные для E1 выявили механизм активации кофермента TPP за счет образования консервативной водородной связи с остатком глутамата (Glu59 в человеческом E1) и за счет введения V-конформации, которая приводит к N4 'атому аминопиримидина к внутримолекулярной водородной связи с атомом С2 тиазолия. Эта уникальная комбинация контактов и конформаций TPP в конечном итоге приводит к образованию реактивного C2-карбаниона. После того, как кофактор TPP декарбоксилат пирувата, ацетильная часть становится гидроксиэтиловым производным, ковалентно присоединенным к TPP. [1]
Структура [ править ]
E1 - мультимерный белок. Е1 млекопитающих, включая Е1 человека, являются тетрамерными и состоят из двух α- и двух β-субъединиц. [1] Некоторые бактериальные E1, в том числе E1 из Escherichia coli , состоят из двух одинаковых субъединиц, каждая из которых равна сумме молекулярных масс α- и β-субъединиц. [3]
.
Активный сайт [ править ]
E1 имеет два каталитических центра, каждый из которых обеспечивает пирофосфат тиамина ( TPP ) и ион магния в качестве кофакторов. Α-субъединица связывает ион магния и пирофосфатный фрагмент, тогда как β-субъединица связывает пиримидиновый фрагмент TPP , образуя вместе каталитический сайт на границе раздела субъединиц. [1]
Активный сайт для пирувата - дегидрогеназы (изображения , созданной из PDB : 1NI4 ) проводит ТЭС через металлическое лигирования ион магния (фиолетовую область) и через водородные связи с аминокислотами. В то время как в активном сайте можно найти более 20 аминокислот, аминокислоты Tyr 89, Arg 90, Gly 136, Val 138, Asp 167, Gly 168, Ala 169, Asn, 196 и His 263 фактически участвуют в водородных связях, чтобы удерживать TPP и пируват (здесь не показаны) в активном сайте. Аминокислоты показаны в виде проволок, а TPP имеет форму шара и палочек. Активный сайт также способствует переносу ацила на TPP в липоамид, ожидающий на E2. [1]
Регламент [ править ]
Фосфорилирование E1 киназой пируватдегидрогеназы (PDK) инактивирует E1, а затем и весь комплекс. PDK ингибируется дихлоруксусной кислотой и пируватом , что приводит к большему количеству активного, нефосфорилированного PDH. [4] Фосфорилатон реверсируется пируватдегидрогеназной фосфатазой , которая стимулируется инсулином , PEP и AMP , но конкурентно ингибируется АТФ , НАДН и ацетил-КоА .
Патология [ править ]
Пируватдегидрогеназа нацелена на аутоантиген, известный как антимитохондриальные антитела (АМА), что приводит к прогрессивному разрушению мелких желчных протоков печени, что приводит к первичному билиарному циррозу . Эти антитела, по-видимому, распознают окисленный белок, возникший в результате воспалительных иммунных реакций. Некоторые из этих воспалительных реакций могут быть связаны с чувствительностью к глютену, поскольку более 50% пациентов с острой печеночной недостаточностью в одном исследовании продемонстрировали немитохондриальные аутоантитела против тканевой трансглутаминазы . [5] Другие митохондриальные аутоантигены включают оксоглутаратдегидрогеназу икомплекс дегидрогеназы альфа-кетокислот с разветвленной цепью , которые являются антигенами, распознаваемыми антимитохондриальными антителами .
Дефицит пируватдегидрогеназы (PDH) - это врожденное дегенеративное метаболическое заболевание, возникающее в результате мутации комплекса пируватдегидрогеназы (PDC), расположенного на X-хромосоме. В то время как дефекты были идентифицированы во всех 3 ферментах комплекса, субъединица E1-α преимущественно является виновником. Нарушение цикла лимонной кислоты из-за дефицита ПДГ лишает организм энергии и приводит к аномальному накоплению лактата. Дефицит ПДГ является частой причиной лактоацидоза у новорожденных и часто проявляется тяжелой летаргией, плохим кормлением, тахипноэ и случаями смерти. [6]
Примеры [ править ]
Белки человека, обладающие активностью пируватдегидрогеназы, включают:
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Связанные ферменты [ править ]
У бактерий существует форма пируватдегидрогеназы (также называемая пируватоксидазой, EC 1.2.2.2), которая связывает окисление пирувата в ацетат и диоксид углерода с восстановлением ферроцитохрома. В E. coli этот фермент кодируется геном оспы B , и этот белок имеет кофактор флавина. [7] Этот фермент увеличивает эффективность роста кишечной палочки в аэробных условиях. [8]
См. Также [ править ]
- Дефицит пируватдегидрогеназы
Ссылки [ править ]
- ^ a b c d e PDB : 1ni4 ; Ciszak EM, Короткина LG, Dominiak PM, Sidhu S, Patel MS (июнь 2003 г.). «Структурные основы триггерного действия тиаминпирофосфат-зависимых ферментов, выявленных пируватдегидрогеназой человека» . J. Biol. Chem . 278 (23): 21240–6. DOI : 10.1074 / jbc.M300339200 . PMID 12651851 .
- ^ а б Дж. М. Берг; Ю.Л. Тимочко, Л. Страйер (2007). Биохимия (6-е изд.). Фримен. ISBN 978-0-7167-8724-2.CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Арджунан П., Немерия Н., Бранскилл А., Чандрасекхар К., Сакс М., Ян Y и др. (Апрель 2002 г.). «Структура компонента Е1 мультиферментного комплекса пируватдегидрогеназы из Escherichia coli при разрешении 1,85 А». Биохимия . 41 (16): 5213–21. DOI : 10.1021 / bi0118557 . PMID 11955070 .
- ^ Jaimes, R третий (июль 2015). «Функциональный ответ изолированного перфузированного нормоксического сердца на активацию пируватдегидрогеназы дихлорацетатом и пируватом» . Pflügers Arch . 468 (1): 131–42. DOI : 10.1007 / s00424-015-1717-1 . PMC 4701640 . PMID 26142699 .
- ^ Леунг П.С., Россаро Л., Дэвис П.А. и др. (2007). «Антимитохондриальные антитела при острой печеночной недостаточности: последствия для первичного билиарного цирроза» . Гепатология . 46 (5): 1436–42. DOI : 10.1002 / hep.21828 . PMC 3731127 . PMID 17657817 .
- ^ Дефицит пируватдегидрогеназного комплекса в eMedicine
- ^ Recny MA, Hager LP (1982). «Восстановление нативной пируватоксидазы Escherichia coli из мономеров апофермента и FAD». J. Biol. Chem . 257 (21): 12878–86. PMID 6752142 .
- Перейти ↑ Abdel-Hamid AM, Attwood MM, Guest JR (2001). «Пируватоксидаза способствует аэробной эффективности роста Escherichia coli » . Микробиология . 147 (Pt 6): 1483–98. DOI : 10.1099 / 00221287-147-6-1483 . PMID 11390679 .
- Очоа С (1954). «Ферментативные механизмы в цикле лимонной кислоты». Достижения в энзимологии и смежных областях молекулярной биологии . Достижения в энзимологии и смежных областях биохимии . Достижения в энзимологии и смежных областях молекулярной биологии. 15 . С. 183–270. DOI : 10.1002 / 9780470122600.ch5 . ISBN 9780470122600. PMID 13158180 .
- Скриба П., Хольцер Х (1961). "Gewinnung von alphaHydroxyathyl-2-thiaminpyrophosphat mit Pyruvatoxydase aus Schweineherzmuskel". Biochem. Z . 334 : 473–486.
- Перхам Р.Н. (2000). «Качающиеся рычаги и качающиеся домены в многофункциональных ферментах: каталитические машины для многоступенчатых реакций». Ежегодный обзор биохимии . 69 (1): 961–1004. DOI : 10.1146 / annurev.biochem.69.1.961 . PMID 10966480 .
Внешние ссылки [ править ]
- Пируват + дегидрогеназа-E1 в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- http://www.brookscole.com/chemistry_d/templates/student_resources/shared_resources/animations/pdc/pdc.html
- PDBe-KB предоставляет обзор всей информации о структуре, доступной в PDB для человеческого пируватдегидрогеназы (липоамида) альфа 1.
- PDBe-KB предоставляет обзор всей информации о структуре, доступной в PDB для бета-пируватдегидрогеназы (липоамида) человека.
| vте Путь метаболизма гликолиза |
|---|
Глюкоза Гексокиназа АТФ ADP Глюкозо-6-фосфат Глюкозо-6-фосфат- изомераза Фруктоза 6-фосфат Фосфофруктокиназа-1 АТФ ADP 1,6-бисфосфат фруктозы Бисфосфат-фруктозы альдолазы Дигидроксиацетонфосфат + + Глицеральдегид 3-фосфат Триозофосфат изомераза 2 × Глицеральдегид-3-фосфат 2 × Глицеральдегид-3- фосфатдегидрогеназа НАД + + P i НАДН + Н + НАД + + P i НАДН + Н + 2 × 1,3-бисфосфоглицерат 2 × Фосфоглицераткиназа ADP АТФ ADP АТФ 2 × 3-фосфоглицерат 2 × Фосфоглицерат мутаза 2 × 2-фосфоглицерат 2 × Phosphopyruvate гидратаз ( енолаз ) H 2 O H 2 O 2 × Фосфоенолпируват 2 × Пируваткиназа ADP АТФ 2 × Пируват 2 × |