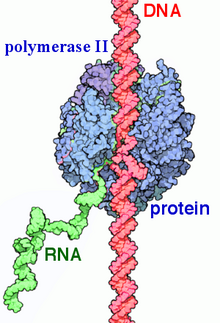
РНК-полимераза II ( РНКП II и Pol II ) представляет собой мультибелковый комплекс, который транскрибирует ДНК в предшественники информационной РНК (мРНК) и большинства малых ядерных РНК (мяРНК) и микроРНК . [1] [2] Это один из трех ферментов РНКП, обнаруженных в ядре эукариотических клеток. [3] РНКП II представляет собой комплекс из 12 субъединиц массой 550 кДа , который является наиболее изученным типом РНК-полимеразы . Для связывания с вышестоящим геном требуется широкий спектр факторов транскрипции.промоторы и начать транскрипцию.
Открытие [ править ]
Ранние исследования предполагали наличие минимум двух РНКП: одна, которая синтезировала рРНК в ядрышке , а другая - другую РНК в нуклеоплазме , являющейся частью ядра, но вне ядрышка. [5] В 1969 году научные экспериментаторы Роберт Родер и Уильям Раттер окончательно открыли дополнительную РНКП, которая отвечает за транскрипцию некоторого вида РНК в нуклеоплазме. Вывод был получен при использовании ионообменной хроматографии с помощью DEAE с покрытием Сефадексабусы. Методика разделяла ферменты в порядке соответствующих элюций, ΙΙ, путем увеличения концентрации сульфата аммония. Ферменты были названы в соответствии с порядком элюирования: RNAP I , RNAP II, RNAP IΙI . [3] Это открытие продемонстрировало, что в нуклеоплазме присутствует дополнительный фермент, который позволяет дифференцировать RNAP II и RNAP III.
Подразделения [ править ]
Эукариотической ядро РНК - полимеразы II , сначала очищали с помощью транскрипции анализов. [7] Очищенный фермент обычно состоит из 10–12 субъединиц (12 у человека и дрожжей) и неспособен к специфическому распознаванию промотора. [8] Известно много взаимодействий субъединица-субъединица. [9]
- ДНК-направленная субъединица РНК-полимеразы II RPB1 - фермент, который у человека кодируется геном POLR2A , а у дрожжей - RPO21. RPB1 - самая крупная субъединица РНК-полимеразы II. Он содержит карбоксиконцевой домен (CTD), состоящий из 52 гептапептидных повторов (YSPTSPS), которые необходимы для активности полимеразы. [10] CTD был впервые обнаружен в лаборатории CJ Ingles в Университете Торонто и JL Corden в Университете Джона Хопкинса . В сочетании с несколькими другими субъединицами полимеразы субъединица RPB1 образует ДНК-связывающий домен полимеразы, бороздку, в которой матрица ДНК транскрибируется в РНК. [11]Он сильно взаимодействует с RPB8. [9]
- RPB2 ( POLR2B ) - вторая по величине субъединица, которая в сочетании по крайней мере с двумя другими субъединицами полимеразы образует структуру внутри полимеразы, которая поддерживает контакт в активном центре фермента между матрицей ДНК и вновь синтезированной РНК. [12]
- RPB3 ( POLR2C ) - третья по величине субъединица. Существует как гетеродимер с другой субъединицей полимеразы, POLR2J, образующей ядро подсборки. RPB3 сильно взаимодействует с RPB1-5,7,10–12. [9]
- РНК - полимераза II , субъединица В4 (RPB4) - кодируется POLR2D геной [13] является четвертой по величине субъединицы и может иметь стрессзащитную роль.
- RPB5 - у человека кодируется геном POLR2E . Две молекулы этой субъединицы присутствуют в каждой РНК-полимеразе II. [14] RPB5 сильно взаимодействует с RPB1, RPB3 и RPB6. [9]
- RPB6 ( polr2f ) - образует структуру с по меньшей мере двух других субъединиц , что стабилизирует транскрибировать полимеразу на ДНК - матрице. [15]
- RPB7 - кодируется POLR2G и может играть роль в регуляции функции полимеразы. [16] RPB7 сильно взаимодействует с RPB1 и RPB5. [9]
- RPB8 ( POLR2H ) - взаимодействует с субъединицами RPB1-3, 5 и 7. [9]
- RPB9 - бороздка, в которой матрица ДНК транскрибируется в РНК, состоит из RPB9 ( POLR2I ) и RPB1.
- RPB10 - продукт гена POLR2L . Он взаимодействует с RPB1-3 и 5 и сильно с RPB3. [9]
- RPB11 - субъединица RPB11 у человека состоит из трех субъединиц: POLR2J (RPB11-a), POLR2J2 (RPB11-b) и POLR2J3 [17] (RPB11-c).
- RPB12 - Также с RPB3 взаимодействует RPB12 ( POLR2K ). [9]
Сборка [ править ]
RPB3 участвует в сборке РНК-полимеразы II. [18] Субкомплекс RPB2 и RPB3 появляется вскоре после синтеза субъединицы. [18] Этот комплекс впоследствии взаимодействует с RPB1. [18] RPB3, RPB5 и RPB7 взаимодействуют между собой с образованием гомодимеров, а RPB3 и RPB5 вместе могут связываться со всеми другими субъединицами RPB, кроме RPB9. [9] Только RPB1 прочно связывается с RPB5. [9] Субъединица RPB1 также связывается с RPB7, RPB10 и более слабо, но наиболее эффективно с RPB8. [9] Как только RPB1 входит в комплекс, могут входить другие субъединицы, такие как RPB5 и RPB7, где RPB5 связывается с RPB6 и RPB8, а RPB3 вводит RPB10, RPB 11 и RPB12. [9]RPB4 и RPB9 могут войти, как только большая часть комплекса будет собрана. RPB4 образует комплекс с RPB7. [9]
Кинетика [ править ]
Ферменты могут катализировать до нескольких миллионов реакций в секунду. Нормы содержания ферментов зависят от условий раствора и концентрации субстрата. Как и другие ферменты, POLR2 имеет кривую насыщения и максимальную скорость ( V max ). Он имеет K m (концентрация субстрата, необходимая для половины V max ) и k cat (количество молекул субстрата, обрабатываемых одним активным центром в секунду). Константа специфичности определяется как k cat / K m . Теоретический максимум для константы специфичности - это предел диффузии примерно от 10 8 до 10 9 ( M -1с -1 ), где каждое столкновение фермента с его субстратом приводит к катализу. У дрожжей мутация в домене триггерной петли самой большой субъединицы может изменить кинетику фермента. [19]
Бактериальная РНК-полимераза, родственница РНК-полимеразы II, переключается между инактивированным и активированным состояниями, перемещаясь вперед и назад вдоль ДНК. [20] Концентрации [NTP] eq = 10 мкМ GTP, 10 мкМ UTP, 5 мкМ ATP и 2,5 мкМ CTP, дают среднюю скорость элонгации, число оборота, ~ 1 п.н. (NTP) -1 для бактериальной RNAP, относительной РНК-полимеразы II. [20]
РНК-полимераза II претерпевает обширную котранскрипционную паузу во время элонгации транскрипции. [21] [22] Эта пауза особенно выражена в нуклеосомах и частично возникает из-за того, что полимераза входит в транскрипционно некомпетентное состояние обратного отслеживания. [21] Продолжительность этих пауз колеблется от секунд до минут или дольше, и выходу из долгоживущих пауз могут способствовать факторы удлинения, такие как TFIIS. [23] В свою очередь, скорость транскрипции влияет на то, удаляются ли гистоны транскрибируемых нуклеосом из хроматина или повторно вставляются за транскрибирующей полимеразой. [24]
Альфа-Аманитин [ править ]
РНК-полимераза II ингибируется α-аманитином [25] и другими аматоксинами . α-Аманитин - очень ядовитое вещество, которое содержится во многих грибах. [5] Грибной яд по-разному воздействует на каждую из РНК-полимераз: I, II, III. RNAP I полностью не реагирует на вещество и будет функционировать нормально, в то время как RNAP III имеет умеренную чувствительность. Однако RNAP II полностью подавляется токсином. Альфа-аманитин ингибирует RNAP II за счет сильных взаимодействий в «воронке», «щели» и ключевом «мостиковом α-спирали » субъединицы RPB-1. [26]
Холоэнзим [ править ]
Холофермент РНК-полимеразы II представляет собой форму эукариотической РНК-полимеразы II, которая задействована в промоторах генов, кодирующих белок, в живых клетках. [8] Он состоит из РНК-полимеразы II, подмножества общих факторов транскрипции , и регуляторных белков, известных как белки SRB.
Часть сборки холофермента называется преинициационным комплексом , потому что его сборка происходит на промоторе гена до инициации транскрипции . В медиатора комплекс действует как мостик между РНК - полимеразы II , и факторов транскрипции.
Контроль структурой хроматина [ править ]
Это набросок примера механизма дрожжевых клеток , с помощью которого хроматина структура и гистона посттрансляционной модификации помогают регулировать и регистрировать транскрипции из генов с помощью РНК - полимеразы II.
Этот путь дает примеры регуляции в следующих точках транскрипции:
- Предварительная инициация (продвижение Bre1, модификация гистона)
- Инициирование (продвижение с помощью TFIIH, модификация Pol II И продвижение с помощью COMPASS, модификация гистонов)
- Удлинение (продвижение Set2, модификация гистонов)
Это относится к различным этапам процесса как к этапам регулирования. Не было доказано, что они используются для регулирования, но весьма вероятно, что это так.
Промоторы элонгации РНК Pol II можно разделить на 3 класса.
- Факторы, влияющие на арест лекарственного средства / последовательности (различные мешающие белки)
- Факторы, ориентированные на структуру хроматина (посттранскрипционные модификаторы гистонов, например, метилтрансферазы гистонов)
- Факторы, улучшающие катализ РНК Pol II (различные мешающие белки и кофакторы Pol II; см. РНК-полимераза II).
Механизмы транскрипции [ править ]
- Структуры хроматина ориентированные факторы:
(HMTs ( Н istone М этил Т ransferases)):
COMPASS§ † - ( COM - сплетение из P roteins AS sociated с S et1) - метилирует лизина 4 гистона Н3: Отвечает репрессии / глушителей транскрипции. Нормальная часть регуляции роста клеток и транскрипции в RNAP II. [27] - Set2 - метилирует лизин 36 гистона H3: Set2 участвует в регуляции элонгации транскрипции посредством прямого контакта с CTD. [28]
(интересный не относящийся к делу пример: Dot1 * ‡ - метилирует лизин 79 гистона H3.) - Bre1 - Убихинат (добавляет убиквитин ) лизин 123 гистона H2B. Связан с пре-инициацией и позволяет связываться с РНК Pol II.
CTD РНК-полимеразы [ править ]
С-конец RPB1 присоединяется для образования С-концевого домена (CTD). Карбоксиконцевой домен РНК-полимеразы II обычно состоит из 52 повторов последовательности Tyr-Ser-Pro-Thr-Ser-Pro-Ser. [29] Домен простирается от ядра фермента RNAPII до выходного канала, это размещение эффективно из-за индукции «реакций процессинга РНК через прямые или косвенные взаимодействия с компонентами механизма процессинга РНК». [30] Домен CTD не существует в РНК-полимеразе I или РНК-полимеразе III. [3]CTD РНК-полимеразы был впервые обнаружен в лаборатории CJIngles в Университете Торонто, а также в лаборатории Дж. Кордена в Университете Джона Хопкинса во время процессов секвенирования ДНК, кодирующей субъединицу RPB1 РНК-полимеразы дрожжей и мышей соответственно. Другие белки часто связывают С-концевой домен РНК-полимеразы, чтобы активировать полимеразную активность. Это домен белка , который участвует в инициации транскрипции, в укупорки из транскрипта РНК и прикрепления к сплайсосома для сплайсинга РНК . [10]
Фосфорилирование домена CTD [ править ]
РНК-полимераза II существует в двух нефосфорилированных и фосфорилированных формах, IIA и IIO соответственно. [5] [3] Переход между двумя формами способствует различным функциям транскрипции. Фосфорилирование из CTD катализируется одним из шести общих факторов транскрипции , TFIIH . TFIIH служит двум целям: первая - раскручивать ДНК в стартовом сайте транскрипции, а другая - фосфорилировать. Полимераза формы IIA присоединяется к преинициативному комплексу, это предполагается, потому что IIA связывается с более высокой аффинностью с TBP ( связывающий белок TATA-бокса ), субъединицей общего фактора транскрипции TFIID., чем форма полимеразы IIO. Полимераза формы IIO способствует удлинению цепи РНК. [5] Метод инициации элонгации осуществляется путем фосфорилирования серина в положении 5 (Ser5) через TFIIH. Вновь фосфорилированный Ser5 рекрутирует ферменты, которые закрывают 5'-конец вновь синтезированной РНК и «3'-процессинговые факторы до поли (А) сайтов». [30] Как только второй серин фосфорилируется, Ser2, элонгация активируется. Чтобы прекратить удлинение, должно произойти дефосфорилирование. Как только домен полностью дефосфорилируется, фермент RNAP II «рециркулирует» и катализирует тот же процесс с другим сайтом инициации. [30]
Рекомбинационная репарация, связанная с транскрипцией [ править ]
Окислительное повреждение ДНК может блокировать транскрипцию РНК-полимеразы II и вызывать разрывы цепи. Описан процесс рекомбинации, связанный с транскрипцией, который может защитить от повреждения ДНК. [31] Во время стадий G1 / G0 клеточного цикла клетки демонстрируют сборку гомологичных факторов рекомбинации на двухцепочечных разрывах внутри активно транскрибируемых областей. Похоже, что транскрипция связана с репарацией двухцепочечных разрывов ДНК с помощью шаблонной гомологичной рекомбинации РНК. Этот процесс репарации эффективно и точно воссоединяет двухцепочечные разрывы в генах , активно транскрибируемых РНК-полимеразой II.
См. Также [ править ]
- Эукариотическая транскрипция
- Посттранскрипционная модификация
- РНК-полимераза I
- Холофермент РНК-полимеразы II
- РНК-полимераза III
- Транскрипция (генетика)
Ссылки [ править ]
- ^ Корнберг RD (декабрь 1999). «Контроль транскрипции эукариот». Тенденции в клеточной биологии . 9 (12): M46–9. DOI : 10.1016 / S0962-8924 (99) 01679-7 . PMID 10611681 .
- ↑ Sims RJ, Mandal SS, Reinberg D (июнь 2004 г.). «Последние основные моменты транскрипции, опосредованной РНК-полимеразой-II». Текущее мнение в клеточной биологии . 16 (3): 263–71. DOI : 10.1016 / j.ceb.2004.04.004 . PMID 15145350 .
- ^ a b c d Янг, Ричард А. (28 ноября 2003 г.). «РНК-полимераза II». Ежегодный обзор биохимии . 60 (1): 689–715. DOI : 10.1146 / annurev.bi.60.070191.003353 . PMID 1883205 .
- Перейти ↑ Meyer PA, Ye P, Zhang M, Suh MH, Fu J (июнь 2006 г.). «Фазирование РНК-полимеразы II с использованием внутренне связанных атомов Zn: обновленная структурная модель» . Структура . 14 (6): 973–82. DOI : 10.1016 / j.str.2006.04.003 . PMID 16765890 .
- ^ a b c d 1942-, Уивер, Роберт Франклин (01.01.2012). Молекулярная биология . Макгроу-Хилл. ISBN 9780073525327. OCLC 789601172 .CS1 maint: numeric names: authors list (link)
- ^ Армаш, Карим-Жан; Миттервегер, Симона; Мейнхарт, Антон; Крамер, Патрик (2019). «Структуры полной РНК-полимеразы II и ее подкомплекса, Rpb4 / 7» (PDF) . Журнал биологической химии . 280 (8): 7131–1734. DOI : 10,2210 / pdb1wcm / PDB . PMID 15591044 .
- ^ Савадого М, Sentenac А (1990). «РНК-полимераза B (II) и общие факторы транскрипции». Ежегодный обзор биохимии . 59 : 711–54. DOI : 10.1146 / annurev.bi.59.070190.003431 . PMID 2197989 .
- ^ a b Майер В. Э., Янг Р. А. (октябрь 1998 г.). «Холоферменты и субкомплексы РНК-полимеразы II» . Журнал биологической химии . 273 (43): 27757–60. DOI : 10.1074 / jbc.273.43.27757 . PMID 9774381 .
- ^ a b c d e f g h i j k l m Acker J, de Graaff M, Cheynel I, Khazak V, Kedinger C, Vigneron M (июль 1997 г.). «Взаимодействие между субъединицами РНК-полимеразы II человека» . Журнал биологической химии . 272 (27): 16815–21. DOI : 10.1074 / jbc.272.27.16815 . PMID 9201987 .
- ^ a b Brickey WJ, Greenleaf AL (июнь 1995 г.). «Функциональные исследования карбоксиконцевого повторяющегося домена РНК-полимеразы II дрозофилы in vivo» . Генетика . 140 (2): 599–613. PMC 1206638 . PMID 7498740 .
- ^ "Entrez Gene: POLR2A-полимераза (РНК) II (ДНК-направленный) полипептид A, 220 кДа" .
- ^ "Entrez Gene: POLR2B полимераза (РНК) II (ДНК-направленный) полипептид B, 140 кДа" .
- ^ Khazak В, Estojak Дж, чо Н, Мейджорс Дж, Соноды G, Тест JR, Golemis Е.А. (апрель 1998 г.). «Анализ взаимодействия новой субъединицы РНК-полимеразы II (pol II) hsRPB4 с ее партнером hsRPB7 и с pol II» . Молекулярная и клеточная биология . 18 (4): 1935–45. DOI : 10.1128 / mcb.18.4.1935 . PMC 121423 . PMID 9528765 .
- ^ "Entrez Gene: POLR2E-полимераза (РНК) II (ДНК-направленный) полипептид E, 25 кДа" .
- ^ "Entrez Gene: POLR2F полимераза (РНК) II (ДНК-направленный) полипептид F" .
- ^ "Entrez Gene: POLR2G полимераза (РНК) II (ДНК-направленный) полипептид G" .
- ^ "Полипептид J3 полимеразы (РНК) II (ДНК-направленный) POLR2J3" .
- ^ a b c Колодзей П.А., Молодой Р.А. (сентябрь 1991 г.). «Мутации в трех крупнейших субъединицах дрожжевой РНК-полимеразы II, которые влияют на сборку ферментов» . Молекулярная и клеточная биология . 11 (9): 4669–78. DOI : 10.1128 / mcb.11.9.4669 . PMC 361357 . PMID 1715023 .
- Перейти ↑ Kaplan CD, Jin H, Zhang IL, Belyanin A (12 апреля 2012 г.). «Рассечение функции триггерной петли Pol II и зависимый от активности Pol II контроль выбора стартового сайта in vivo» . PLOS Genetics . 8 (4): e1002627. DOI : 10.1371 / journal.pgen.1002627 . PMC 3325174 . PMID 22511879 .
- ^ Б Abbondanzieri Е.А., Greenleaf WJ, Shaevitz JW, Landick R, блок SM (ноябрь 2005 года). «Прямое наблюдение шага пар оснований с помощью РНК-полимеразы» . Природа . 438 (7067): 460–5. Bibcode : 2005Natur.438..460A . DOI : 10,1038 / природа04268 . PMC 1356566 . PMID 16284617 .
- ^ a b Ходжес, Кортни; Бинту, Лакрамиоара; Лубковская, Люцина; Кашлев Михаил; Бустаманте, Карлос (31.07.2009). «Нуклеосомные колебания определяют динамику транскрипции РНК-полимеразы II» . Наука . 325 (5940): 626–628. Bibcode : 2009Sci ... 325..626H . DOI : 10.1126 / science.1172926 . ISSN 1095-9203 . PMC 2775800 . PMID 19644123 .
- ^ Черчман, Л. Стирлинг; Вайсман, Джонатан С. (20 января 2011 г.). «Секвенирование зарождающегося транскрипта визуализирует транскрипцию при разрешении нуклеотидов» . Природа . 469 (7330): 368–373. Bibcode : 2011Natur.469..368C . DOI : 10,1038 / природа09652 . ISSN 1476-4687 . PMC 3880149 . PMID 21248844 .
- ^ Galburt, Эрик A .; Гриль, Стефан В .; Видманн, Анна; Лубковская, Люцина; Чой, Джейсон; Ногалес, Ева; Кашлев Михаил; Бустаманте, Карлос (2007-04-12). «Обратное отслеживание определяет силовую чувствительность RNAP II в зависимости от факторов». Природа . 446 (7137): 820–823. Bibcode : 2007Natur.446..820G . DOI : 10,1038 / природа05701 . ISSN 1476-4687 . PMID 17361130 . S2CID 4310108 .
- ^ Бинту, Лакрамиоара; Копачинская, Марта; Ходжес, Кортни; Лубковская, Люцина; Кашлев Михаил; Бустаманте, Карлос (13 ноября 2011 г.). «Скорость удлинения РНК-полимеразы определяет судьбу транскрибируемых нуклеосом» . Структурная и молекулярная биология природы . 18 (12): 1394–1399. DOI : 10.1038 / nsmb.2164 . ISSN 1545-9985 . PMC 3279329 . PMID 22081017 .
- Перейти ↑ Kaplan CD, Larsson KM, Kornberg RD (июнь 2008 г.). «Триггерная петля РНК-полимеразы II участвует в выборе субстрата и напрямую нацелена на альфа-аманитин» . Молекулярная клетка . 30 (5): 547–56. DOI : 10.1016 / j.molcel.2008.04.023 . PMC 2475549 . PMID 18538653 .
- ^ Гонг, Сюэ Q .; Недиалков, Юрий А .; Бертон, Захари Ф. (2004-06-25). «-Аманитин блокирует транслокацию человеческой РНК-полимеразы II» . Журнал биологической химии . 279 (26): 27422–27427. DOI : 10.1074 / jbc.M402163200 . ISSN 0021-9258 . PMID 15096519 .
- ^ Бриггс, Скотт Д.; Брик, Мэри; Strahl, Brian D .; Cheung, Wang L .; Дэви, Джудит К .; Dent, Sharon YR; Уинстон, Фред; Аллис, К. Дэвид (2001-12-15). «Метилирование гистона H3 по лизину 4 опосредуется Set1 и требуется для роста клеток и подавления рДНК у Saccharomyces cerevisiae» . Гены и развитие . 15 (24): 3286–3295. DOI : 10,1101 / gad.940201 . ISSN 0890-9369 . PMC 312847 . PMID 11751634 .
- ^ Ли, Бинг; Хау, Лиэнн; Андерсон, Скотт; Йейтс, Джон Р .; Уоркман, Джерри Л. (14 марта 2003 г.). «Гистон-метилтрансфераза Set2 функционирует через фосфорилированный карбоксиконцевой домен РНК-полимеразы II» . Журнал биологической химии . 278 (11): 8897–8903. DOI : 10.1074 / jbc.M212134200 . ISSN 0021-9258 . PMID 12511561 .
- ^ Meinhart A, Крамер P (июль 2004). «Распознавание карбоксиконцевого домена РНК-полимеразы II факторами процессинга 3'-РНК» . Природа . 430 (6996): 223–6. Bibcode : 2004Natur.430..223M . DOI : 10,1038 / природа02679 . PMID 15241417 . S2CID 4418258 .
- ^ a b c Эглофф, Сильвен; Мерфи, Шона (2008). «Взлом кода CTD РНК-полимеразы II». Тенденции в генетике . 24 (6): 280–288. DOI : 10.1016 / j.tig.2008.03.008 . PMID 18457900 .
- Перейти ↑ Wei L, Levine AS, Lan L (2016). «Транскрипционно-связанная гомологичная рекомбинация после окислительного повреждения». Ремонт ДНК (Amst.) . 44 : 76–80. DOI : 10.1016 / j.dnarep.2016.05.009 . PMID 27233112 .
Внешние ссылки [ править ]
- Дополнительная информация в Национальной лаборатории Беркли
( Копия Wayback Machine )
- РНК + полимераза + II в медицинских предметных рубриках Национальной медицинской библиотеки США (MeSH)