 | |||
| Имена | |||
|---|---|---|---|
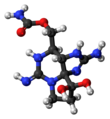
| Название ИЮПАК [(3a S , 4 R , 10a S ) -10,10-дигидрокси-2,6-дииминооктагидро-1 H , 8 H -пирроло [1,2- c ] пурин-4-ил] метилкарбамат | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.160.395 | ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 10 H 17 N 7 O 4 | |||
| Молярная масса | 299,291 г · моль -1 | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Сакситоксин ( STX ) - мощный нейротоксин и самый известный паралитический токсин моллюсков (PST). Проглатывание сакситоксина людьми, обычно при употреблении в пищу моллюсков, зараженных токсичным цветением водорослей , вызывает заболевание, известное как паралитическое отравление моллюсками (PSP).
Термин сакситоксин происходит от названия рода масляных моллюсков ( Saxidomus ), из которых он был впервые выделен. Но термин сакситоксин может также относиться ко всему набору из более чем 50 структурно связанных нейротоксинов (известных под общим названием «сакситоксины»), продуцируемых водорослями и цианобактериями, включая сам сакситоксин (STX), неосакситоксин (NSTX), гониутоксины (GTX) и декарбамоилсакситоксин (dcSTX).
Сакситоксин имеет большое экологическое и экономическое воздействие, поскольку его присутствие в двустворчатых моллюсках, таких как мидии , моллюски , устрицы и гребешки, часто приводит к запретам на коммерческий и рекреационный промысел моллюсков во многих прибрежных водах умеренного пояса по всему миру, включая северо-восток и запад США, запад Европа, Восточная Азия, Австралия, Новая Зеландия и Южная Африка. В Соединенных Штатах паралитическое отравление моллюсками произошло в Калифорнии , Орегоне , Вашингтоне , Аляске и Новой Англии .
Источник в природе [ править ]
Сакситоксин представляет собой нейротоксин, который естественным образом вырабатывается некоторыми видами морских динофлагеллят ( Alexandrium sp., Gymnodinium sp., Pyrodinium sp.) И пресноводными цианобактериями ( [(Dolichospermum cicinale]] sp., Некоторыми Aphanizomenon spp., Cylindrospermopsis sp., Lyngbya sp. , Planktothrix зр.) [2] [3] Сакситоксин аккумулирует в частности , в двустворчатых фильтраторы. [ править ]
Сакситоксин также был обнаружен по крайней мере у 12 видов морских рыб фугу в Азии и у одной пресноводной рыбы тилапии в Бразилии. [4] Однако окончательный источник STX часто остается неясным. Динофлагеллята Pyrodinium bahamense является источником STX, обнаруженного во Флориде . [5] [6] Недавние исследования показывают обнаружение STX в коже, мышцах, внутренних органах и гонадах южной рыбы- фугу " Indian River Lagoon " с самой высокой концентрацией (22 104 мкг STX-экв / 100 г ткани), измеренной в яичники . Даже после года плена кожная слизь оставалась очень токсичной. [7]Концентрации в фугу из США аналогичны концентрациям, обнаруженным на Филиппинах, в Таиланде [6], Японии [6] [8] и странах Южной Америки. [9] Рыба фугу также накапливает структурно отличный токсин, тетродотоксин . [ необходима цитата ]
Структура и синтез [ править ]
Дигидрохлорид сакситоксина представляет собой аморфное гигроскопичное твердое вещество, но рентгеновская кристаллография кристаллических производных позволила определить структуру сакситоксина. [10] [11] Окисление сакситоксина приводит к образованию производного пурина с высокой флуоресценцией, которое было использовано для обнаружения его присутствия. [12]
Было выполнено несколько полных синтезов сакситоксина. [13] [14] [15]
Механизм действия [ править ]
Сакситоксин - нейротоксин, который действует как селективный обратимый блокатор потенциалзависимых натриевых каналов. [16] [17] Один из самых мощных известных природных токсинов, он действует на потенциал-управляемые натриевые каналы нейронов , препятствуя нормальному функционированию клеток и приводя к параличу . [ необходима цитата ]
Напряжение-управляемые натриевые каналы необходимы для нормального функционирования нейронов. Он существует в виде интегральных мембранных белков, расположенных вдоль аксона нейрона и обладающих четырьмя доменами, охватывающими клеточную мембрану . Открытие потенциалзависимого натриевого канала происходит при изменении напряжения или при правильном связывании какого-либо лиганда . Чрезвычайно важно, чтобы эти натриевые каналы функционировали должным образом, поскольку они необходимы для распространения потенциала действия . Без этой способности нервная клетка становится неспособной передавать сигналы, и область тела, которую она обессиливает, оказывается отрезанной от нервной системы.. Это может привести к параличу пораженной области, как в случае с сакситоксином. [ необходима цитата ]
Сакситоксин обратимо связывается с натриевым каналом. Он связывается непосредственно в поре белка канала, закрывая отверстие и предотвращая поток ионов натрия через мембрану. Это приводит к нервному отключению, описанному выше. [ необходима цитата ]
Биосинтез [ править ]
Хотя биосинтез сакситоксина кажется сложным, организмы из двух разных царств , фактически из двух разных доменов , видов морских динофлагеллят и пресноводных цианобактерий , способны продуцировать эти токсины. В то время как преобладающая теория образования динофлагеллят происходила через симбиотический мутуализм с цианобактериями, появились данные, свидетельствующие о том, что сами динофлагеллаты также обладают генами, необходимыми для синтеза сакситоксина. [18]
Биосинтез сакситоксина - это первый нетерпеновый алкалоидный путь, описанный для бактерий, хотя точный механизм биосинтеза сакситоксина все еще является теоретической моделью. Точный механизм связывания субстратов с ферментами до сих пор неизвестен, а гены, участвующие в биосинтезе сакситоксина, либо предполагаются, либо были идентифицированы только недавно. [18] [19]
В прошлом были предложены два биосинтеза. Более ранние версии отличаются от более позднего предложения Kellmann, et al. основано как на биосинтетических соображениях, так и на генетических данных, недоступных на момент первого предложения. Более поздняя модель описывает кластер генов STX (sxt), используемый для получения более благоприятной реакции. Самая последняя последовательность реакций Sxt у цианобактерий [19] выглядит следующим образом. Обратитесь к диаграмме для подробного описания биосинтеза и промежуточных структур.
- Он начинается с загрузки ацильного белка-носителя (АСР) ацетатом из ацетил-КоА с образованием промежуточного соединения 1.
- За этим следует катализируемое SxtA метилирование ацетил-ACP, которое затем превращается в пропионил-ACP, давая промежуточное соединение 2.
- Позже другой SxtA выполняет реакцию конденсации Клайзена между пропионил-ACP и аргинином, образуя промежуточное соединение 4 и промежуточное соединение 3.
- SxtG переносит амидиногруппу от аргинина к α-аминогруппе промежуточного соединения 4, продуцируя промежуточное соединение 5.
- Промежуточное соединение 5 затем подвергается ретроальдольной конденсации под действием SxtBC, образуя промежуточное соединение 6.
- SxtD добавляет двойную связь между C-1 и C-5 промежуточного соединения 6, что вызывает сдвиг 1,2-H между C-5 и C-6 в промежуточном соединении 7.
- SxtS выполняет эпоксидирование двойной связи с образованием промежуточного соединения 8, а затем раскрытие эпоксида в альдегид с образованием промежуточного соединения 9.
- SxtU восстанавливает концевую альдегидную группу промежуточного соединения 9 STX, образуя таким образом промежуточное соединение 10.
- SxtIJK катализирует перенос карбамоильной группы на свободную гидроксильную группу на промежуточном соединении 10, образуя промежуточное соединение 11.
- SxtH и SxtT в сочетании с SxtV и кластером генов SxtW выполняют аналогичную функцию, которая заключается в последовательном гидроксилировании C-12, тем самым продуцируя сакситоксин и завершая путь биосинтеза STX.
Болезнь и отравление [ править ]
Токсикология [ править ]
Сакситоксин очень токсичен для морских свинок , смертельный только при 5 мкг / кг при внутримышечном введении . Летальные дозы ( LD50 ) для мышей очень похожи при различных способах введения: внутривенно - 3,4 мкг / кг, внутрибрюшинно - 10 мкг / кг и перорально - 263 мкг / кг. Пероральная LD50 для человека составляет 5,7 мкг / кг, поэтому примерно 0,57 мг сакситоксина (1/8 песчинки среднего размера) является летальным при проглатывании, а смертельная доза при инъекции составляет примерно 1/10 от этой дозы (примерно 0,6 мкг / кг). Ингаляционная токсичность сакситоксина в аэрозольной форме для человека оценивается в 5 мг · мин / м 3.. Сакситоксин может попадать в организм через открытые раны, и была предложена смертельная доза 50 мкг на человека при использовании этого пути. [20]
Болезнь человека [ править ]
Заболевание человека, связанное с приемом вредных уровней сакситоксина, известно как паралитическое отравление моллюсками , или PSP, а сакситоксин и его производные часто называют «токсинами PSP». [2]
Медицинское и экологическое значение сакситоксина связано с потреблением зараженных моллюсков и некоторых видов рыб, которые могут концентрировать токсин из динофлагеллат или цианобактерий. Блокирование нейронных натриевых каналов, которое происходит при PSP, вызывает вялый паралич, который оставляет жертву спокойной и сознательной в процессе прогрессирования симптомов . Смерть часто наступает от дыхательной недостаточности . Токсины PSP причастны к гибели различных морских животных, включая трофический перенос токсина от источника водорослей вверх по пищевой цепи к высшим хищникам . [ необходима цитата ]
Исследования на животных показали , что летальные эффекты сакситаксина могут быть отменены с 4-аминопиридином , [21] [22] [23] , но нет никаких исследований на человеке. Как и в случае с любым паралитическим агентом, реанимация «рот в рот» или искусственная вентиляция с использованием любых средств сохранят отравленную жертву в живых до тех пор, пока не будет введено противоядие или пока яд не исчезнет. [ необходима цитата ]
Военный интерес [ править ]
Сакситоксин, в силу его чрезвычайно низкой LD50, легко может быть использован в качестве оружия. В прошлом считалось для военного использования Соединенных Штатов и был разработан в качестве химического оружия со стороны американских военных . [24] Известно, что сакситоксин был разработан ЦРУ как для открытого военного использования, так и для тайных целей . [25] Среди запасов оружия были боеприпасы M1, которые содержали либо сакситоксин, либо ботулотоксин, либо их смесь. [26] С другой стороны, известно, что ЦРУ выдало небольшую дозу сакситоксина пилоту самолета-разведчика U-2 Фрэнсису Гэри Пауэрсу.в виде небольшой инъекции, спрятанной в серебряном долларе, для использования в случае его поимки и задержания. [25] [26]
После запрета президента Никсона на биологическую войну в 1969 году запасы сакситоксина в США были уничтожены, и разработка сакситоксина в качестве военного оружия прекратилась. [27] Однако в 1975 году ЦРУ сообщило Конгрессу, что оно сохранило небольшое количество сакситоксина и яда кобры против приказов Никсона, которое затем было уничтожено или передано исследователям. [25]
Он указан в таблице 1 в Конвенции о запрещении химического оружия . Военные США выделили сакситоксин и присвоили ему обозначение химического оружия TZ . [ необходима цитата ]
См. Также [ править ]
- Канадские справочные материалы
- Потенциал действия
- Александрий тамаренс
- Анабаена циркиналис
- Вредное цветение водорослей
- Паралитическое отравление моллюсками
- Бреветоксин
- Цигуатоксин
- Домоевая кислота
- Окадаиновая кислота
- Тетродотоксин
Ссылки [ править ]
- ^ https://lpsn.dsmz.de/species/dolichospermum-circinale,https://lpsn.dsmz.de/species/anabaena-circinalis, https://www.who.int/water_sanitation_health/water-quality/guidelines /chemicals/saxitoxin-gdwq-bd-for-review-20191125.pdf
- ^ a b Кларк РФ; Williams SR; Nordt SP; Маногуэрра А.С. (1999). «Обзор избранных отравлений морепродуктами» . Undersea Hyperb Med . 26 (3): 175–84. PMID 10485519 . Проверено 12 августа 2008 .
- ^ Ландсберг, Ян Х. (2002). «Влияние вредоносного цветения водорослей на водные организмы». Обзоры в Науке о рыболовстве . 10 (2): 113–390. DOI : 10.1080 / 20026491051695 . S2CID 86185142 .
- ^ Galvão, JA; Oetterer, M .; Биттенкур-Оливейра Мдо, MDC; Gouvêa-Barros, S .; Хиллер, С .; Erler, K .; Luckas, B .; Pinto, E .; Куйбида, П. (2009). «Накопление сакситоксинов пресноводной тилапией (Oreochromis niloticus) для потребления человеком». Токсикон . 54 (6): 891–894. DOI : 10.1016 / j.toxicon.2009.06.021 . PMID 19560484 .
- ^ Смит, EA; Грант, Ф .; Фергюсон, CMJ; Галлахер, С. (2001). «Биотрансформации паралитических токсинов моллюсков бактериями, выделенными из двустворчатых моллюсков» . Прикладная и экологическая микробиология . 67 (5): 2345–2353. DOI : 10,1128 / AEM.67.5.2345-2353.2001 . PMC 92876 . PMID 11319121 .
- ^ a b c Sato, S .; Kodama, M .; Огата, Т .; Saitanu, K .; Furuya, M .; Hirayama, K .; Какинума, К. (1997). «Сакситоксин как токсичный компонент пресноводного иглобрюха Tetraodon fangi в Таиланде». Токсикон . 35 (1): 137–140. DOI : 10.1016 / S0041-0101 (96) 00003-7 . PMID 9028016 .
- ^ Ландсберг, JH; Холл, С .; Johannessen, JN; Белый, КД; Конрад, С.М.; Abbott, JP; Flewelling, LJ; Ричардсон, RW; Дики, RW; Шут, Эдвард Л. Е.; Этеридж, Стейси М .; Дело, Джонатан Р .; Ван Долах, Фрэнсис М .; Leighfield, Tod A .; Цзоу, Инлинь; Beaudry, Clarke G .; Беннер, Рональд А .; Роджерс, Патрисия Л .; Скотт, Паула С .; Кавабата, Кенджи; Wolny, Jennifer L .; Штайдингер, Карен А. (2006). «Отравление сакситоксиновыми рыбами-фугу в Соединенных Штатах, с первым отчетом о Pyrodinium bahamense как предполагаемом источнике токсина» . Перспективы гигиены окружающей среды . 114 (10): 1502–1507. DOI : 10.1289 / ehp.8998 . PMC 1626430 . PMID 17035133 .
- ^ Документы, JR; Ландсберг, Дж. Х .; Этеридж, С.М.; Кувшин, GC; Лонган, SW (2008). «Нетрадиционные переносчики паралитического отравления моллюсками» . Морские препараты . 6 (2): 308–348. DOI : 10.3390 / md6020308 . PMC 2525492 . PMID 18728730 .
- ^ Лагос, NS; Onodera, H .; Загатто, Пенсильвания; Андриноло, D. ́O .; Азеведо, SMFQ; Осима, Ю. (1999). «Первое свидетельство паралитических токсинов моллюсков в пресноводной цианобактерии Cylindrospermopsis raciborskii, выделенной из Бразилии». Токсикон . 37 (10): 1359–1373. DOI : 10.1016 / S0041-0101 (99) 00080-X . PMID 10414862 .
- ^ Борднер Дж .; Thiessen WE; Bates HA; Рапопорт Х. (1975). «Строение кристаллического производного сакситоксина. Строение сакситоксина». Журнал Американского химического общества . 97 (21): 6008–12. DOI : 10.1021 / ja00854a009 . PMID 1176726 .
- ^ Шанц EJ; Газаросян В.Е .; Schnoes HK; Сильный FM; Springer JP; Пеццанит JO; Кларди Дж. (1975). «Строение сакситоксина». Журнал Американского химического общества . 97 (5): 1238–1239. DOI : 10.1021 / ja00838a045 . PMID 1133383 .
- ^ Бейтс HA; Кострикен Р .; Рапопорт Х. (1978). «Химический анализ сакситоксина. Усовершенствования и модификации». Журнал сельскохозяйственной и пищевой химии . 26 (1): 252–4. DOI : 10.1021 / jf60215a060 . PMID 621331 .
- ^ Танино Х .; Наката Т .; Канеко Т .; Киши Ю. (1997). «Стереоспецифический тотальный синтез d, l-сакситоксина». Журнал Американского химического общества . 99 (8): 2818–9. DOI : 10.1021 / ja00450a079 . PMID 850038 .
- ^ Bhonde VR; Looper RE (2011). «Стереоконтролируемый синтез (+) - сакситоксина» . Журнал Американского химического общества . 133 (50): 20172–4. DOI : 10.1021 / ja2098063 . PMC 3320040 . PMID 22098556 .
- ^ Флеминг JJ; McReynolds MD; Дюбуа Ж. (2007). «(+) - Сакситоксин: стереоселективный синтез первого и второго поколения». Журнал Американского химического общества . 129 (32): 9964–75. DOI : 10.1021 / ja071501o . PMID 17658800 .
- ^ Справочник по токсикологии боевых отравляющих веществ . Гупта, Рамеш К. (Рамеш Чандра), 1949- (Второе изд.). Лондон: Academic Press. 21 января 2015. с. 426. ISBN. 978-0-12-800494-4. OCLC 903965588 .CS1 maint: другие ( ссылка )
- ^ Huot, RI; Армстронг, DL; Чан, ТС (июнь 1989 г.). «Защита нервной токсичности с помощью моноклональных антител к блокатору натриевых каналов тетродотоксину» . Журнал клинических исследований . 83 (6): 1821–1826. DOI : 10.1172 / JCI114087 . PMC 303901 . PMID 2542373 .
- ^ a b Stüken, Анке; Орр, Рассел; Келлманн, Ральф; Мюррей, Шона; Нейлан, Бретт; Якобсен, Кьетилль (18 мая 2011 г.). «Открытие ядерно-кодированных генов нейротоксина сакситоксина в динофлагеллятах» . PLOS ONE . 6 (5): e20096. Bibcode : 2011PLoSO ... 620096S . DOI : 10.1371 / journal.pone.0020096 . PMC 3097229 . PMID 21625593 .
- ^ a b Kellmann, R .; Михали, Т.К .; Jeon, YJ; Пикфорд, Р.; Помати, Ф .; Нейлан, Б.А. (2008). «Биосинтетический промежуточный анализ и функциональная гомология выявить кластер генов сакситоксина в цианобактериях» . Прикладная и экологическая микробиология . 74 (13): 4044–4053. DOI : 10,1128 / AEM.00353-08 . PMC 2446512 . PMID 18487408 .
- ^ Patocka J; Стредав Л. (23 апреля 2002 г.). Прайс, Ричард (ред.). «Краткий обзор природных небелковых нейротоксинов» . Информационный бюллетень ASA . 02–2 (89): 16–23. ISSN 1057-9419 . Проверено 26 мая 2012 года .
- ^ Бентон, BJ; Keller, SA; Сприггс, DL; Capacio, BR; Чанг, ФК (1998). «Восстановление после летального воздействия сакситоксина: терапевтическое окно для 4-аминопиридина (4-AP)». Токсикон . 36 (4): 571–588. DOI : 10.1016 / s0041-0101 (97) 00158-X . PMID 9643470 .
- ^ Чанг, ФК; Сприггс, DL; Benton, BJ; Keller, SA; Capacio, BR (1997). «4-аминопиридин обращает вспять вызванную сакситоксином (STX) и тетродотоксином (TTX) кардиореспираторную депрессию у морских свинок, подвергшихся хроническому механическому лечению». Фундаментальная и прикладная токсикология . 38 (1): 75–88. DOI : 10.1006 / faat.1997.2328 . PMID 9268607 .
- ^ Чен, H .; Lin, C .; Ван, Т. (1996). «Влияние 4-аминопиридина на интоксикацию сакситоксином». Токсикология и прикладная фармакология . 141 (1): 44–48. DOI : 10,1006 / taap.1996.0258 . PMID 8917674 .
- ^ Стюарт, Чарльз Эдвард (2006). Справочник по оружию массовых жертв и борьбе с терроризмом . Джонс и Бартлетт Обучение. п. 175. ISBN 978-0-7637-2425-2. Дата обращения 4 мая 2015 .
- ^ a b Уилис, Марк; Рожа, Лайош; Дандо, Малкольм (2006). Смертельные культуры: биологическое оружие с 1945 года . Президент и научные сотрудники Гарвардского колледжа. п. 39. ISBN 978-0-674-01699-6. Дата обращения 4 мая 2015 .
- ^ Мауони, Альберт Дж. (2000). Борьба Америки с химико-биологической войной . 88 Post Road West, Westport, CT 06881: Praeger Publishers. п. 50. ISBN 978-0-275-96756-7. Дата обращения 4 мая 2015 .CS1 maint: location ( ссылка )
Внешние ссылки [ править ]
- [1] Паралитическое отравление моллюсками
- [2] Нил Эдвардс. Химические лаборатории. Школа химии, физики и экологии. Университет Сассекса в Брайтоне. Сакситоксин - от пищевого отравления до химической войны
- Токсичные цианобактерии в воде: руководство по их последствиям для здоровья населения, мониторингу и управлению. Под редакцией Ингрид Хор и Джейми Бартрам, 1999 г. Опубликовано Всемирной организацией здравоохранения. ISBN 0-419-23930-8