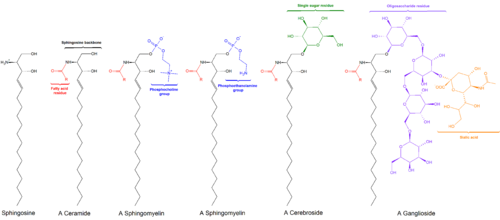
Сфинголипиды представляют собой класс липидов , содержащих основу сфингоидных оснований, набор алифатических аминокислот спиртов , который включает сфингозин . Они были обнаружены в экстрактах мозга в 1870-х годах и были названы в честь мифологического сфинкса из-за своей загадочной природы. [1] Эти соединения играют важную роль в передаче сигналов и распознавании клеток . Сфинголипидозы или нарушения метаболизма сфинголипидов особенно влияют на нервную ткань . Сфинголипид с группой R, состоящей только из атома водорода, является церамидом.. Другие общие группы R включают фосфохолин , дающий сфингомиелин , и различные мономеры или димеры сахаров, дающие цереброзиды и глобозиды , соответственно. Цереброзиды и глобозиды вместе известны как гликосфинголипиды .
Структура [ править ]
Основания с длинной цепью, иногда называемые просто сфингоидными основаниями, являются первыми непреходящими продуктами синтеза сфинголипидов de novo как у дрожжей, так и у млекопитающих. Эти соединения, особенно известные как фитосфингозин и дигидросфингозин (также известные как сфинганин [2], хотя этот термин встречается реже), в основном представляют собой соединения C 18 с несколько более низкими уровнями оснований C 20 . [3] Церамиды и гликосфинголипиды являются N- ацильными производными этих соединений. [4]
Основная цепь сфингозина O-связана с (обычно) заряженной головной группой, такой как этаноламин , серин или холин . [ необходима цитата ]
Основная цепь также связана амидом с ацильной группой , такой как жирная кислота . [ необходима цитата ]
Типы [ править ]
Простые сфинголипиды, которые включают основания сфингоидов и церамиды, составляют ранние продукты путей синтеза сфинголипидов.
- Основания сфингоидов - это фундаментальные строительные блоки всех сфинголипидов. Основными сфингоидными основаниями млекопитающих являются дигидросфингозин и сфингозин, тогда как дигидросфингозин и фитосфингозин являются основными сфингоидными основаниями в дрожжах. [5] [6] Сфингозин, дигидросфингозин и фитосфингозин могут фосфорилироваться.
- Керамиды , как общий класс, представляют собой N- ацилированные сфингоидные основания, лишенные дополнительных головных групп.
- Дигидроцерамид получают N- ацилированием дигидросфингозина. Дигидроцерамид обнаружен как в дрожжевых, так и в млекопитающих системах.
- Керамид производится в системах млекопитающих путем десатурации дигидроцерамида дигидроцерамид-десатуразой 1 (DES1). Эта высокобиоактивная молекула также может фосфорилироваться с образованием церамид-1-фосфата .
- Фитокерамид образуется в дрожжах путем гидроксилирования дигидроцерамида по C-4.
Сложные сфинголипиды могут быть образованы добавлением головных групп к церамиду или фитокерамиду:
- Сфингомиелины имеют молекулу фосфохолина или фосфоэтаноламина со сложноэфирной связью с 1-гидроксигруппой церамида.
- Гликосфинголипиды - это церамиды с одним или несколькими сахарными остатками, соединенными β- гликозидной связью в 1-гидроксильном положении (см. Изображение).
- Цереброзиды содержат одну глюкозу или галактозу в 1-гидрокси-положении.
- Сульфатиды - это сульфатированные цереброзиды.
- Ганглиозиды содержат по крайней мере три сахара, один из которых должен быть сиаловой кислотой .
- Цереброзиды содержат одну глюкозу или галактозу в 1-гидрокси-положении.
- Инозитол- содержащие церамиды, производные от фитокерамида, производятся дрожжами. К ним относятся инозитолфосфорилцерамид, манноза- инозитолфосфорилцерамид и маннозадинозитолфосфорилцерамид.
Метаболизм сфинголипидов млекопитающих [ править ]
Синтез сфинголипидов de novo начинается с образования 3-кето-дигидросфингозина серин-пальмитоилтрансферазой . [7] Предпочтительными субстратами для этой реакции являются пальмитоил-КоА и серин . Тем не менее, исследования показали , что серин palmitoyltransferase обладает некоторой активностью по отношению к другим видам жирной ацил-КоА [8] и альтернативные аминокислотам , [9] и разнообразие сфингоидного база недавно было рассмотрено. [10] Затем 3-кето-дигидросфингозин восстанавливается с образованием дигидросфингозина. Дигидросфингозин ацилируется одной из шести (дигидро) церамидсинтаз, CerS- первоначально назывался LASS - с образованием дигидроцерамида. [11] Шесть ферментов CerS имеют разную специфичность к субстратам ацил-КоА, что приводит к образованию дигидроцерамидов с разной длиной цепи (от C14 до C26). Затем дигидроцерамиды обесцвечиваются с образованием церамида. [12]
Образованный de novo церамид является центральным узлом сети сфинголипидов и, следовательно, имеет несколько судьб. Он может фосфорилироваться церамидкиназой с образованием церамид-1-фосфата. Альтернативно, он может быть гликозилирован глюкозилцерамидсинтазой или галактозилцерамидсинтазой . Кроме того, он может быть преобразован в сфингомиелин путем добавления головной группы фосфорилхолина сфингомиелинсинтазой . В результате этого процесса образуется диацилглицерин . Наконец, церамид может расщепляться церамидазой с образованием сфингозина.. Сфингозин может фосфорилироваться с образованием сфингозин-1-фосфата. Это может быть дефосфорилировано для преобразования сфингозина. [13]
Пути распада позволяют превращать эти метаболиты в церамид. Сложные гликосфинголипиды гидролизуются до глюкозилцерамида и галактозилцерамида. Эти липиды затем гидролизуются бета-глюкозидазами и бета-галактозидазами для регенерации церамида. Точно так же сфингомиелин может расщепляться сфингомиелиназой с образованием церамида. [ необходима цитата ]
Единственный путь превращения сфинголипидов в несфинголипиды - через сфингозин-1-фосфатлиазу. При этом образуется этаноламин фосфат и гексадеценан. [14]
Функции сфинголипидов млекопитающих [ править ]
Обычно считается, что сфинголипиды защищают поверхность клетки от вредных факторов окружающей среды, образуя механически стабильный и химически устойчивый внешний листок липидного бислоя плазматической мембраны . Было обнаружено, что некоторые сложные гликосфинголипиды участвуют в определенных функциях, таких как распознавание клеток и передача сигналов . Распознавание клеток зависит главным образом от физических свойств сфинголипидов, тогда как передача сигналов включает специфические взаимодействия гликановых структур гликосфинголипидов с аналогичными липидами, присутствующими на соседних клетках, или с белками . [ необходима цитата ]
Недавно было показано , что простые метаболиты сфинголипидов , такие как церамид и сфингозин-1-фосфат , являются важными медиаторами в сигнальных каскадах, участвующих в апоптозе , пролиферации , стрессовых ответах, некрозе , воспалении , аутофагии , старении и дифференцировке . [15] [16] [17] [18] [19] [20] Липиды на основе церамидов самоагрегируются в клеточных мембранах и образуют отдельные фазы, менее жидкие, чем основные фосфолипиды. Эти микродомены на основе сфинголипидов, или "липидные рафты »были первоначально предложены для сортировки мембранных белков по клеточным путям мембранного транспорта. В настоящее время большинство исследований сосредоточено на организующей функции во время передачи сигнала [21].
Сфинголипиды синтезируются путем, который начинается в ER и завершается в аппарате Гольджи , но эти липиды обогащены плазматической мембраной и эндосомами , где они выполняют многие из своих функций. [22] Транспорт происходит через везикулы и мономерный транспорт в цитозоле . Сфинголипиды практически отсутствуют в митохондриях и ER , но составляют 20-35 молярную долю липидов плазматической мембраны. [23]
У экспериментальных животных кормление сфинголипидами подавляет канцерогенез толстой кишки , снижает холестерин ЛПНП и повышает холестерин ЛПВП . [24]
Другие сфинголипиды [ править ]
Сфинголипиды универсальны у эукариот, но редко встречаются у бактерий и архей . Бактерии, которые действительно продуцируют сфинголипиды, обнаружены в семействе Sphingomonadaceae , группе FCB (некоторые члены) и некоторых частях Deltaproteobacteria . [25]
Сфинголипиды дрожжей [ править ]
Из-за невероятной сложности систем млекопитающих дрожжи часто используются в качестве модельного организма для разработки новых путей. Эти одноклеточные организмы часто более поддаются генетической трактовке, чем клетки млекопитающих, и библиотеки штаммов доступны для получения штаммов, содержащих практически любую нелетальную одиночную делецию в открытой рамке считывания . Двумя наиболее часто используемыми дрожжами являются Saccharomyces cerevisiae и Schizosaccharomyces pombe , хотя исследования также проводятся на патогенных дрожжах Candida albicans . [ необходима цитата ]
В дополнении к важным структурным функциям комплексных сфинголипидов (инозитол phosphorylceramide и его производных mannosylated), в сфингоидных основах фитосфингозин и dihydrosphingosine (sphinganine) играют жизненно важную роль в сигнальных S.cerevisiae , . Эти эффекты включают регуляцию эндоцитоза , убиквитин-зависимый протеолиз (и, таким образом, регуляцию поглощения питательных веществ [26] ), динамику цитоскелета , клеточный цикл , трансляцию , посттрансляционную модификацию белка и реакцию на тепловой стресс. [27] Кроме того, модуляция метаболизма сфинголипидов путем Передача сигналов фосфатидилинозитол (4,5) -бисфосфата через Slm1p и Slm2p и кальциневрин был недавно описан. [28] Кроме того, было показано взаимодействие на уровне субстрата между синтезом сложного сфинголипида и циклированием фосфатидилинозитол-4-фосфата фосфатидилинозитолкиназой Stt4p и липидной фосфатазой Sac1p. [29]
Сфинголипиды растений [ править ]
Высшие растения содержат более широкий спектр сфинголипидов, чем животные и грибы. [ необходима цитата ]
Заболевания [ править ]
Существует несколько нарушений метаболизма сфинголипидов, известных как сфинголипидозы . Основными членами этой группы являются болезнь Ниманна-Пика , болезнь Фабри , болезнь Краббе , болезнь Гоше , болезнь Тея-Сакса и метахроматическая лейкодистрофия . Они , как правило , наследуется по аутосомно - рецессивным моды, но особенно Фабри заболевание является Х-хромосомой . Взятые вместе, сфинголипидозы имеют заболеваемость примерно 1 из 10 000, но значительно больше у некоторых групп населения, таких как евреи-ашкенази . Заместительная ферментная терапиядоступно для лечения в основном болезни Фабри и болезни Гоши , и людей с этими типами сфинголипидоза может жить хорошо во взрослую жизнь. Другие типы обычно приводят к летальному исходу в возрасте от 1 до 5 лет для младенческих форм, но прогрессирование может быть легким для ювенильных или взрослых форм. [ необходима цитата ]
Сфинголипиды также связаны с белком фратаксин (Fxn), дефицит которого связан с атаксией Фридрейха (FRDA). Потеря Fxn в нервной системе у мышей также активирует путь железо / сфинголипид / PDK1 / Mef2, указывая на то, что механизм эволюционно консервативен. Кроме того, уровни сфинголипидов и активность PDK1 также увеличиваются в сердцах пациентов с FRDA, что позволяет предположить, что аналогичный путь затрагивается при FRDA. [30] Другие исследования показали, что накопление железа в нервной системе мух усиливает синтез сфинголипидов, что, в свою очередь, активирует 3-фосфоинозитидзависимую протеинкиназу-1 (Pdk1) и фактор-усилитель миоцитов-2 (Mef2), чтобы вызвать нейродегенерацию фоторецепторы взрослых. [31]
Дополнительные изображения [ править ]
Сфингозин
См. Также [ править ]
- Сфингозил фосфатид
Ссылки [ править ]
- Перейти ↑ Chun J, Hartung HP (2010). «Механизм действия перорального финголимода (FTY720) при рассеянном склерозе» . Клиническая нейрофармакология . 33 (2): 91–101. DOI : 10,1097 / wnf.0b013e3181cbf825 . PMC 2859693 . PMID 20061941 .
- ^ Страница продукта в Sigma Aldrich
- ^ Диксон RC (1998). «Функции сфинголипидов у Saccharomyces cerevisiae: сравнение с млекопитающими» . Ежегодный обзор биохимии . 67 : 27–48. DOI : 10.1146 / annurev.biochem.67.1.27 . PMID 9759481 .
- ^ Краткий, очень понятный обзор дан в Gunstone, F. (1996) Fatty Acid and Lipid Chemistry , pp 43-44. Блэки Академический и Профессиональный. ISBN 0-7514-0253-2
- ↑ Dickson RC (май 2008 г.). «Серия тематических обзоров: сфинголипиды. Новые сведения о метаболизме и функциях сфинголипидов у почкующихся дрожжей» . Журнал липидных исследований . 49 (5): 909–21. DOI : 10,1194 / jlr.R800003-JLR200 . PMC 2311445 . PMID 18296751 .
- ^ Bartke N, Hannun YA (апрель 2009). «Биоактивные сфинголипиды: метаболизм и функции» . Журнал липидных исследований . 50 Приложение: S91-6. DOI : 10,1194 / jlr.R800080-JLR200 . PMC 2674734 . PMID 19017611 .
- ↑ Merrill AH (декабрь 1983 г.). «Характеристика активности серинпальмитоилтрансферазы в клетках яичников китайского хомячка». Biochimica et Biophysica Acta (BBA) - липиды и липидный метаболизм . 754 (3): 284–91. DOI : 10.1016 / 0005-2760 (83) 90144-3 . PMID 6652105 .
- ↑ Merrill AH, Williams RD (февраль 1984 г.). «Использование различных тиоэфиров ацил-КоА жирных кислот сериновой пальмитоилтрансферазой из головного мозга крысы» . Журнал липидных исследований . 25 (2): 185–8. PMID 6707526 .
- ^ Zitomer NC, Митчелл Т, Восс К.А., Бонди Г.С., Пруетт СТ, Garnier-Amblard ЕС, Либескинд Л.С., Парк Н, Ван Е, Sullards МС, Меррилл АГ, Райли РТ (февраль 2009 г.). «Ингибирование церамидсинтазы фумонизином B1 вызывает накопление 1-дезоксисфинганина: новой категории биоактивных 1-дезоксисфингоидных оснований и 1-дезоксидигидроцерамидов, биосинтезируемых линиями клеток млекопитающих и животными» . Журнал биологической химии . 284 (8): 4786–95. DOI : 10.1074 / jbc.M808798200 . PMC 2643501 . PMID 19095642 .
- ^ Pruett ST, Бушнев A, Хагедорн K, M Adiga, Haynes CA, Sullards MC, Лиотта DC, Меррилл AH (август 2008). «Биоразнообразие сфингоидных оснований (« сфингозинов ») и родственных аминоспиртов» . Журнал липидных исследований . 49 (8): 1621–39. DOI : 10,1194 / jlr.R800012-JLR200 . PMC 2444003 . PMID 18499644 .
- ^ Певзнер-Jung Y, Бен-Дор S, Futerman AH (сентябрь 2006). «Когда Lasses (гены, обеспечивающие долголетие) превращаются в CerS (керамидсинтазы) ?: Понимание регуляции синтеза церамидов» . Журнал биологической химии . 281 (35): 25001–5. DOI : 10.1074 / jbc.R600010200 . PMID 16793762 .
- ^ Causeret C, Geeraert L, Ван дер Хувен G, Маннартс GP, Ван Вельдховен PP (октябрь 2000). «Дальнейшая характеристика дигидроцерамид-десатуразы крысы: распределение в тканях, субклеточная локализация и субстратная специфичность». Липиды . 35 (10): 1117–25. DOI : 10.1007 / s11745-000-0627-6 . PMID 11104018 .
- ^ Hannun Ю.А., Obeid LM (февраль 2008). «Принципы передачи сигналов биоактивными липидами: уроки сфинголипидов». Обзоры природы Молекулярная клеточная биология . 9 (2): 139–50. DOI : 10.1038 / nrm2329 . PMID 18216770 .
- ^ Bandhuvula P, Саб JD (май 2007). «Сфингозин-1-фосфатлиаза в иммунитете и раке: подавление сирены». Тенденции молекулярной медицины . 13 (5): 210–7. DOI : 10.1016 / j.molmed.2007.03.005 . PMID 17416206 .
- ^ Hannun Ю.А., Obeid Л.М. (июль 2002). «Церамид-центрическая вселенная липид-опосредованной регуляции клеток: стрессовые столкновения липидного типа» . Журнал биологической химии . 277 (29): 25847–50. DOI : 10.1074 / jbc.R200008200 . PMID 12011103 .
- ^ Spiegel S, Milstien S (июль 2002). «Сфингозин-1-фосфат, ключевая сигнальная молекула клетки» . Журнал биологической химии . 277 (29): 25851–4. DOI : 10.1074 / jbc.R200007200 . PMID 12011102 .
- ^ Lavieu G, Scarlatti F, Sala G, Carpentier S, Levade T, Ghidoni R, Botti J, Codogno P (март 2006). «Регулирование аутофагии сфингозинкиназой 1 и ее роль в выживании клеток во время нехватки питательных веществ» . Журнал биологической химии . 281 (13): 8518–27. DOI : 10.1074 / jbc.M506182200 . PMID 16415355 .
- ^ Венейбл ME, Ли JY, Смит MJ, Bielawska A, Obeid LM (декабрь 1995). «Роль церамида в клеточном старении» . Журнал биологической химии . 270 (51): 30701–8. DOI : 10.1074 / jbc.270.51.30701 . PMID 8530509 .
- ^ Хец CA, Хунн M, P Rojas, Торрес V, Лейтон L, Quest AF (декабрь 2002). «Зависящее от каспаз инициирование апоптоза и некроза рецептором Fas в лимфоидных клетках: начало некроза связано с задержкой увеличения церамидов» . Журнал клеточной науки . 115 (Pt 23): 4671–83. DOI : 10,1242 / jcs.00153 . PMID 12415011 .
- ^ Снайдер AJ, Орр Gandy KA, Obeid LM (июнь 2010). «Сфингозинкиназа: роль в регуляции биоактивных сфинголипидных медиаторов при воспалении» . Биохимия . 92 (6): 707–15. DOI : 10.1016 / j.biochi.2010.02.008 . PMC 2878898 . PMID 20156522 .
- Перейти ↑ Brown DA, London E (июнь 2000). «Структура и функция мембранных рафтов, богатых сфинголипидами и холестерином» . Журнал биологической химии . 275 (23): 17221–4. DOI : 10.1074 / jbc.R000005200 . PMID 10770957 .
- ^ Futerman АХ (декабрь 2006). «Внутриклеточный трафик сфинголипидов: связь с биосинтезом» . Biochimica et Biophysica Acta (BBA) - Биомембраны . 1758 (12): 1885–92. DOI : 10.1016 / j.bbamem.2006.08.004 . PMID 16996025 .
- ^ Ван Меер G, Lisman Q (июль 2002). «Транспорт сфинголипидов: рафты и транслокаторы» . Журнал биологической химии . 277 (29): 25855–8. DOI : 10.1074 / jbc.R200010200 . PMID 12011105 .
- ^ Веспер Н, Шмельц Е.М., Николова-Каракашян М.Н., Dillehay Д.Л., Линча Д.В., Меррилл АГ (июль 1999 года). «Сфинголипиды в пище и возрастающее значение сфинголипидов для питания» . Журнал питания . 129 (7): 1239–50. DOI : 10.1093 / JN / 129.7.1239 . PMID 10395583 .
- ^ Хивер, SL; Джонсон, Э.Л .; Лей, RE (июнь 2018 г.). «Сфинголипиды во взаимодействиях между хозяином и микробами» (PDF) . Текущее мнение в микробиологии . 43 : 92–99. DOI : 10.1016 / j.mib.2017.12.011 . PMID 29328957 .
- ^ Чанг Н, Мао С, Хейтман Дж, Hannun Ю.А., ОБЕЙД Л.М. (сентябрь 2001 г.). «Фитосфингозин как специфический ингибитор роста и импорта питательных веществ в Saccharomyces cerevisiae» . Журнал биологической химии . 276 (38): 35614–21. DOI : 10,1074 / jbc.m105653200 . PMID 11468289 .
- ^ Cowart LA, Obeid LM (март 2007). «Сфинголипиды дрожжей: последние достижения в понимании биосинтеза, регуляции и функции» . Biochimica et Biophysica Acta (BBA) - молекулярная и клеточная биология липидов . 1771 (3): 421–31. DOI : 10.1016 / j.bbalip.2006.08.005 . PMC 1868558 . PMID 16997623 .
- ↑ Dickson RC (май 2008 г.). «Серия тематических обзоров: сфинголипиды. Новые сведения о метаболизме и функциях сфинголипидов у почкующихся дрожжей» . Журнал липидных исследований . 49 (5): 909–21. DOI : 10,1194 / jlr.R800003-JLR200 . PMC 2311445 . PMID 18296751 .
- ↑ Brice SE, Alford CW, Cowart LA (март 2009 г.). «Модуляция метаболизма сфинголипидов фосфатидилинозитол-4-фосфатфосфатазой Sac1p посредством регуляции фосфатидилинозитола в Saccharomyces cerevisiae» . Журнал биологической химии . 284 (12): 7588–96. DOI : 10.1074 / jbc.M808325200 . PMC 2658053 . PMID 19139096 .
- ↑ Chen K, Ho TS, Lin G, Tan KL, Rasband MN, Bellen HJ (ноябрь 2016 г.). «Потеря фратаксина активирует путь железо / сфинголипид / PDK1 / Mef2 у млекопитающих» . eLife . 5 . DOI : 10.7554 / eLife.20732 . PMC 5130293 . PMID 27901468 .
- ^ Chen K, Lin G, Haelterman NA, Ho TS, Li T, Li Z, Duraine L, Graham BH, Jaiswal M, Yamamoto S, Rasband MN, Bellen HJ (июнь 2016 г.). «Потеря фратаксина вызывает токсичность железа, синтез сфинголипидов и активацию Pdk1 / Mef2, что приводит к нейродегенерации» . eLife . 5 . DOI : 10.7554 / eLife.16043 . PMC 4956409 . PMID 27343351 .
Внешние ссылки [ править ]
- Сфинголипиды в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)