| Имена | |||
|---|---|---|---|
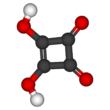
| Предпочтительное название IUPAC 3,4-дигидроксициклобут-3-ен-1,2-дион | |||
| Другие названия Квадратичная кислота | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.018.875 | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 4 Н 2 О 4 | |||
| Молярная масса | 114,056 г · моль -1 | ||
| Появление | белый кристаллический порошок | ||
| Температура плавления | > 300 ° С (572 ° F, 573 К) | ||
| Кислотность (p K a ) | 1,5, 3,4 | ||
| Опасности | |||
| R-фразы (устаревшие) | R36 / 37/38 R43 | ||
| S-фразы (устаревшие) | S26 S36 | ||
| точка возгорания | 190 ° С (374 ° F, 463 К) [2] | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Квадратная кислота , также называемая квадратичной кислотой, потому что ее четыре атома углерода приблизительно образуют квадрат, представляет собой двухосновную органическую кислоту с химической формулой C 4 O 2 (OH) 2 . [3]
Основание, сопряженное с квадратной кислотой, представляет собой гидрокварат анион C
4HO-
4; и сопряженное основание аниона квадрата водорода представляет собой двухвалентный анион квадрата C
4О2-
4. Это один из оксоуглеродных анионов , состоящий только из углерода и кислорода.
Квадратная кислота - это реагент для химического синтеза , который используется, например, для изготовления светочувствительных сквараиновых красителей и ингибиторов протеинтирозинфосфатаз .
Химические свойства [ править ]
Квадратная кислота представляет собой белый кристаллический порошок. [4] Начало термического разложения зависит от различных термодинамических условий, таких как скорость нагрева.
Структура квадратной кислоты не является идеальным квадратом, поскольку длины углерод-углеродных связей не совсем равны. Высокая кислотность с р К а = 1,5 для первого протона и р К = 3,4 для второго объясняется резонансная стабилизацией из аниона . [5] Поскольку отрицательные заряды одинаково распределены между каждым атомом кислорода, дианион квадратной кислоты полностью симметричен (в отличие от самой квадратной кислоты), причем все длины связей C-C идентичны, а длины всех связей C-O идентичны.
Производные [ править ]
Во многих реакциях квадратной кислоты участвуют ОН-группы. Молекула ведет себя как сильная дикарбоновая кислота. Это более сильная кислота, чем обычные карбоновые кислоты. [6]
- C 4 O 2 (OH) 2 → [C 4 O 3 (OH)] - + H + pK = 1,5
- [C 4 O 3 (OH)] - → [C 4 O 4 ] 2- + H + pK = 3,5
Группы ОН лабильны в квадратной кислоте. Он образует дихлорид с тионилхлоридом:
- C 4 O 2 (OH) 2 + 2 SOCl 2 → C 4 O 2 Cl 2 + 2 HCl + 2 SO 2
Хлориды - хорошие уходящие группы, напоминающие хлорангидриды . Их вытесняют разнообразные нуклеофилы. Таким образом можно получить дитиоскварат. [7]
Бис ( метиловый эфир ) получают алкилированием триметилортоформиатом . [8]
Кварамиды получают замещением алкоксильных или хлоридных групп из C 4 O 2 X 2 (X = OR, Cl). [7] [9]
Одна или обе кислородные (= O) группы в квадратичном анионе могут быть заменены дицианометиленом = C (CN) 2 . Образующиеся анионы, такие как 1,2-бис (дицианометилен) скварат и 1,3-бис (дицианометилен) скварат , сохраняют ароматический характер скварата и были названы псевдооксоуглеродными анионами .
Фотолиз квадратной кислоты в твердой матрице аргона при 10 К (-263 ° C) дает ацетилендиол . [10]
Координационные комплексы [ править ]
Квадратный дианион ведет себя аналогично оксалату , образуя моно- и полиядерные комплексы с ионами твердых металлов. Гидрат скварата кобальта (II) Co (C 4 O 4 ) (H 2 O) 2 (желтый, кубический) можно получить путем автоклавирования гидроксида кобальта (II) и квадратной кислоты в воде при 200 ° C. Вода связана с атомом кобальта , а кристаллическая структура состоит из кубического расположения полых ячеек, стенки которых представляют собой либо шесть квадратных анионов (оставляя пустоту шириной 7 Å), либо несколько молекул воды (оставляя пустоту 5 Å). [11]
Дигидроксид скварата кобальта (II) Co 3 (OH) 2 (C 4 O 4 ) 2 · 3H 2 O (коричневый) получают вместе с предыдущим соединением. Он имеет столбчатую структуру, включающую каналы, заполненные молекулами воды; их можно удалить и заменить без разрушения кристаллической структуры. Цепи ферромагнитные ; они связаны антиферромагнитно в гидратированной форме и ферромагнитно в безводной форме. [11]
Синтезированы и охарактеризованы мономерные и димерные смешанно-лигандные комплексы квадрата меди (II). [12] Приведены инфракрасные, электронные спектры и спектры ЭПР в Q-диапазоне, а также магнитная восприимчивость.
Тот же метод дает дигидроксид квадрата железа (II) Fe 2 (OH) 2 (C 4 O 4 ) (светло-коричневый). [11]
Синтез [ править ]
Оригинальный синтез начался с Этанолизом perfluorocyclobutene , чтобы дать 1,2-диэтокси-3,3,4,4-тетрафтор-1-циклобутно. Гидролиз дает квадратную кислоту. [13] [3]
Хотя это непрактично, скварат и родственные анионы, такие как дельтат C
3О2-
3и ацетилендиолат C
2О2-
2могут быть получены восстановительным связыванием монооксида углерода с использованием уранорганических комплексов . [14] [15]
Медицинское использование [ править ]
С медицинской точки зрения, SADBE или дибутиловый эфир квадратной кислоты или дибутилскварат получают из квадратной кислоты. [16] используется для лечения бородавок . [17] квадратная кислота дибутиловый эфир также используется для лечения очаговой алопеции или облысения Totalis ( аутоиммунное выпадение волос ) через местную иммунотерапию с участием продуцирования аллергической сыпи. [18] Дибутиловый эфир квадратной кислоты в настоящее время проходит испытания для использования при лечении герпеса на губах (герпес). [19]
Диэтилскварат был использован при синтезе Perzinfotel .
См. Также [ править ]
- Циклобутен , C
4ЧАС
6 - Дельтовая кислота , C
3ЧАС
2О
3 - Кроконовая кислота , C
5ЧАС
2О
5 - Родизоновая кислота , C
6ЧАС
2О
6 - Скварамиды , амиды квадратных кислот
Ссылки [ править ]
- ^ 3,4-Дигидрокси-3-циклобутен-1,2-дион . Сигма-Олдрич
- ^ 3,4-Дигидрокси-3-циклобутен-1,2-дион, 98 +% . Альфа Эзар
- ^ а б Роберт Уэст (1980). «История оксоуглеродов». В Роберте Уэсте (ред.). Оксоуглероды . Академическая пресса. С. 1–14. DOI : 10.1016 / B978-0-12-744580-9.50005-1 . ISBN 9780127445809.
- ^ Ли, К.-С .; Квеон, JJ; Ой, И.-Х .; Ли, CE (2012). «Полиморфный фазовый переход и термическая стабильность в квадратной кислоте ( H
2C
4О
4.)» . J. Phys , Chem Сухой остаток. . 73 (7):. 890-895 DOI : 10.1016 / j.jpcs.2012.02.013 . - ^ Запад, Роберт ; Пауэлл, Дэвид Л. (1963). «Новые ароматические анионы. III. Расчет молекулярных орбиталей на оксигенированных анионах». Варенье. Chem. Soc. 85 (17): 2577–2579. DOI : 10.1021 / ja00900a010 .
- ^ «Таблицы кислотности гетероатомных органических кислот и углеродных кислот» .
- ^ а б Артур Х. Шмидт (1980). "Reaktionen von Quadratsäure und Quadratsäure-Derivaten". Синтез . 1980 (12): 961. DOI : 10,1055 / с-1980-29291 .
- ^ Лю, Хуэй; Tomooka, Craig S .; Xu, Simon L .; и другие. (1999). «Диметил скварат и его превращение в 3-этенил-4-метоксициклобутен-1,2-дион и 2-бутил-6-этенил-5-метокси-1,4-бензохинон». Органический синтез . 76 : 189. DOI : 10,15227 / orgsyn.076.0189 .
- ^ Ян Сторер, R .; Ачиро, Кэролайн; Джонс, Лин Х. (2011). «Кварамиды: физические свойства, синтез и применение». Chem. Soc. Ред . 40 (5): 2330–2346. DOI : 10.1039 / c0cs00200c . PMID 21399835 .
- ^ Майер, Гюнтер; Рор, Кристин (1995). «Этиндиол: фотохимическая генерация и матрично-спектроскопическая идентификация». Либигс Аннален . 1996 (3): 307–309. DOI : 10.1002 / jlac.199619960303 .
- ^ a b c Хитоши, Кумагаи; Хидео, Собукава; Мохамедалли, Курму (2008). «Гидротермальные синтезы, структуры и магнитные свойства координационных каркасов двухвалентных переходных металлов». Журнал материаловедения . 43 (7): 2123–2130. Bibcode : 2008JMatS..43.2123K . DOI : 10.1007 / s10853-007-2033-8 . S2CID 95205908 .
- ^ Reinprecht, JT; Миллер, JG; Vogel, GC; и другие. (1979). «Синтез и характеристика комплексов квадрата меди (II)». Неорг. Chem., 19, 927-931
- ^ Парк, JD; Коэн, С. и Лачер, младший (1962). «Реакции гидролиза галогенированных циклобутеновых эфиров: синтез дикетоциклобутендиола». Варенье. Chem. Soc. 84 (15): 2919–2922. DOI : 10.1021 / ja00874a015 .
- ^ Фрей, Алистер S .; Cloke, F. Geoffrey N .; Хичкок, Питер Б. (2008). "Механистические исследования восстановительной циклоолигомеризации CO смешанными сэндвичевыми комплексами U (III). Молекулярная структура [(U (η-C 8 H 6 {Si′Pr 3 -1,4} 2 ) (η-Cp * )» ] 2 (μ-η 1 : η 1 -C 2 O 2 ) ". Журнал Американского химического общества . 130 (42): 13816–13817. Doi : 10.1021 / ja8059792 . PMID 18817397 .
- ^ Summerscales, Оуэн Т .; Фрей, Алистер С.П.; Cloke, F. Geoffrey N .; Хичкок, Питер Б. (2009). «Восстановительное диспропорционирование диоксида углерода в карбонатные и скваратные продукты с использованием смешанного сэндвич-комплекса U (III)». Химические коммуникации (2): 198–200. DOI : 10.1039 / b815576c . PMID 19099067 .
- ^ "Дибутиловый эфир квадратной кислоты" .
- ^ "Бородавки" . Центр дерматологии Уилмингтона . Проверено 23 октября 2011 .
- ^ Holzer, AM; Каплан, LL; Левис, WR (2006). «Гаптены как лекарства: контактные аллергены - мощные иммуномодуляторы местного действия». J. Drugs Dermatol. 5 (5): 410–416. PMID 16703776 .
- ^ http://clinicaltrials.gov/show/NCT01971385