 | |
| Имена | |
|---|---|
| Другие имена пентафторид тантала | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ECHA InfoCard | 100.029.111 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| TaF 5 | |
| Молярная масса | 275,95 г / моль |
| Внешность | белый порошок |
| Плотность | 4,74 г / см 3 , твердый |
| Температура плавления | 96,8 ° С (206,2 ° F, 369,9 К) |
| Точка кипения | 229,5 ° С (445,1 ° F, 502,6 К) |
| разлагается | |
| + 795,0 · 10 −6 см 3 / моль | |
| Структура | |
| 0 Д | |
| Опасности | |
| Основные опасности | Источник ВЧ |
Классификация ЕС (DSD) (устарела) | нет в списке |
| R-фразы (устаревшие) | 34 |
| S-фразы (устарели) | 26-27-28-36 / 37 / 39-45 |
| точка возгорания | Негорючий |
| Родственные соединения | |
Родственные соединения | TaCl 5 NbCl 5 WF 6 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Фторид тантала (V) представляет собой неорганическое соединение с формулой TaF 5 . Это одно из основных молекулярных соединений тантала . Это соединение, характерное для некоторых других пентафторидов, является летучим, но существует в виде олигомера в твердом состоянии.
Подготовка и структура [ править ]
Его получают путем обработки металлического тантала газообразным фтором . [1] NbF 5 получают аналогично.
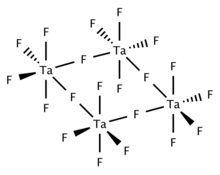
Твердый и расплавленный TaF 5 является тетрамерным и состоит из четырех центров TaF 6, связанных мостиковыми фторидными центрами. Газообразный TaF 5 имеет тригонально-пирамидальную структуру с симметрией D 3h . [2]
Реакции и производные [ править ]
Склонность TaF 5 к образованию кластеров в твердом состоянии указывает на льюисовскую кислотность мономера. Действительно, TaF 5 реагирует с источниками фторида с образованием ионов [TaF
6]-
, [TaF
7]2−
, и [TaF
8]3−
. С нейтральными основаниями Льюиса, такими как диэтиловый эфир, TaF 5 образует аддукты .
TaF
5используются в сочетании с HF в качестве катализатора для алкилирования из алканов и алкенов и для протонирования из ароматических соединений. TaF
5–HF система устойчива в восстановительных средах в отличие от SbF5–HF . [3] В присутствии фторида пентафторид тантала образует анионы [TaF
8]3−
, [TaF
7]2−
, или [TaF
6]-
в зависимости от природы противоиона и концентрации HF. Высокие концентрации HF способствуют образованию гексафторида за счет образования HF.-
2: [4]
- [TaF
7]2−
+ HF ⇌ [TaF
6]-
+ ВЧ-
2
Соли M 3 TaF 8 кристаллизованы. При K + = M + кристаллы состоят из [TaF
7]2−
анионы вместе с фторидом, который не координируется с Ta (V). [5] Для M + = M + кристаллы имеют [TaF
8]3−
. [6]
- Разрез структуры Na 3 TaF 8 (Ta = бирюзовый, F = зеленый).
Актуальность разделения Ta и Nb [ править ]
В процессе Мариньяка Nb и Ta разделяют путем фракционной кристаллизации K 2 TaF 7 из растворов плавиковой кислоты. В этих условиях ниобий образует K 2 NbOF 5 , который более растворим, чем K 2 TaF 7 . Восстановление K 2 TaF 7 натрием дает металлический Ta. [7]
Ссылки [ править ]
- ^ Священник, HF (1950). "Безводные фториды металлов" Неорганические синтезы ". 3 : 171-183. Doi : 10.1002 / 9780470132340.ch47 . Цитировать журнал требует
|journal=( помощь ) - ^ Holleman, AF; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5 .
- ↑ Арпад Мольнар; Г.К. Сурья Пракаш; Жан Соммер (2009). Суперкислотная химия (2-е изд.). Wiley-Interscience. п. 60. ISBN 978-0-471-59668-4.
- ^ Анатолий Agulyanski (2004). Химия фторидных соединений тантала и ниобия . Амстердам: Эльзевир. п. 134 . ISBN 0-444-51604-2.
- ^ Любомир Смрчок, Радован Черны, Мирослав Боча, Ивета Мацкова, Бланка Кубикова (2010). «K 3 TaF 8 по данным порошковой лабораторной рентгенографии» . Acta Crystallographica C . 66 (2): pi16 – pi18. DOI : 10.1107 / S0108270109055140 . PMID 20124670 . CS1 maint: использует параметр авторов ( ссылка )
- ^ Langer, V .; Smrčok, L .; Боча, М. (2010). «Повторное определение Na 3 TaF 8 ». Acta Crystallographica C . 66 (9): pi85 – pi86. DOI : 10.1107 / S0108270110030556 . PMID 20814090 . CS1 maint: использует параметр авторов ( ссылка )
- ↑ Клаус Андерссон, Карлхайнц Райхерт, Рюдигер Вольф «Тантал и соединения тантала» в Энциклопедии промышленной химии Ульмана 2002, Wiley-VCH. Вайнхайм. DOI : 10.1002 / 14356007.a26_071