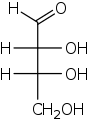
Тетрозы представляет собой моносахарид с 4 углеродных атомов. Они имеют либо альдегидную функциональную группу в положении 1 ( альдотетрозы ), либо кетоновую функциональную группу в положении 2 ( кетотетрозы ). [1] [2]
Альдотетрозы имеют два хиральных центра ( асимметричные атомы углерода ), поэтому возможны 4 различных стереоизомера . Есть два встречающихся в природе стереоизомеров, на энантиомеры из эритрозы и треоза , имеющие D конфигурации , но не в L энантиомеры. Кетотетрозы имеют один хиральный центр и, следовательно, два возможных стереоизомера: эритрулозу ( L- и D-формы ). Опять же, в природе встречается только D- энантиомер.
Биологические функции [ править ]
Есть несколько известных способов использования сахара тетрозы в природе. Некоторые из них наблюдаются в метаболических путях, а другие, как известно, влияют на определенные ферменты.
Промежуточные соединения пентозофосфатного пути [ править ]
Одним из метаболических путей, в которых участвует тетроза, является пентозофосфатный путь . [3] В пентозофосфатном пути есть окислительная стадия и неокислительная стадия. [4] Тетрозный сахар, D-эритроза , используется на неокислительной стадии, когда D-рибулозо-5-фосфат превращается в 6-углеродный сахар ( фруктозо-6-фосфат ) и 3-углеродный сахар ( глицеральдегид-3-фосфат. ). [4] Обе эти молекулы можно использовать в других частях тела.
D-эритрозо-4-фосфат образуется в результате реакции, называемой трансальдоляцией. [5] В пентозофосфатном пути трансальдолаза удаляет первые 3 молекулы углерода седогептулозо-7-фосфата и помещает их на глицеральдегид-3-фосфат. [4] Трансальдолаза использует основание Шиффа для выполнения обратной альдольной реакции и прямой альдольной реакции по своему механизму, генерируя эритрозо-4-фосфат и фруктозо-6-фосфат . [4] Эритрозо-4-фосфат является важным промежуточным звеном в пентозофосфатном пути, потому что затем он используется на заключительном неокислительном этапе этого пути.
Конечная неокислительная стадия пути - это транскетолазная реакция. Транскетолаза использует тиамин пирофосфат или ТЭС кофактор, чтобы разорвать неблагоприятное связь между атомом углерода в карбонильной и альфа - углерода . [4] TPP атакует молекулу ксилулозо-5-фосфата и способствует разрыву связи между C2 (карбонильный углерод) и C3 (альфа-углерод), при этом высвобождается глицеральдегид-3-фосфат. [4] Затем C2 может атаковать эритрозо-4-фосфат, который образует фруктозо-6-фосфат. [4] Оба продукта этой реакции могут вступать в путь глюконеогенеза для регенерации глюкозы .
Ингибиторы ферментов [ править ]
Было обнаружено, что молекула дифосфата тетрозы, 2,4-дифосфат D-треозы, является ингибитором глицеральдегид-3-фосфатдегидрогеназы . [3] Глицеральдегид-3-фосфатдегидрогеназа - шестой фермент, используемый в пути гликолиза , и его функция заключается в превращении глицеральдегид-3-фосфата в 1,3-бисфосфоглицерат . [6] Эта молекула дифосфата тетрозы ингибирует G3P-дегидрогеназу от проведения катализа, поскольку она окисляет фермент, связываясь с ним в активном центре. [7] Когда дифосфат тетрозы связывается с ферментом, активный центр фермента блокируется; поэтому фосфоролизG3P не может произойти. Высокие концентрации дифосфата тетрозы должны использоваться, чтобы превзойти субстрат, G3P, и заблокировать функцию G3P дегидрогеназы. При потере функции глицеральдегид-3-фосфатдегидрогеназы гликолиз не может продолжаться. [6]
Было обнаружено, что D-эритрозо-4-фосфат является ингибитором фосфоглюкозоизомеразы . [8] Фосфоглюкозоизомераза - второй фермент в пути гликолиза, и ее роль заключается в превращении глюкозо-6-фосфата во фруктозо-6-фосфат. [6]
В обоих случаях тетроза является ингибитором фермента в пути гликолиза, препятствуя его дальнейшему развитию.
Ссылки [ править ]
- ^ Lindhorst TK (2007). Основы химии и биохимии углеводов (1-е изд.). Wiley-VCH. ISBN 978-3-527-31528-4.
- ^ Robyt JF (1997). Основы химии углеводов (1-е изд.). Springer. ISBN 0-387-94951-8.
- ^ a b Batt RD, Dickens F, Williamson DH (ноябрь 1960). «Метаболизм тетрозы. 2. Утилизация тетроз и тетритолов тканями крысы» . Биохимический журнал . 77 (2): 281–94. DOI : 10.1042 / bj0770281 . PMC 1204983 . PMID 13687765 .
- ^ Б с д е е г Garrett RH, Гриши CM (2017). Биохимия . Бостон, Массачусетс: обучение Cengage. С. 755–794. ISBN 978-1-305-57720-6.
- ^ Horecker BL, Smyrniotis PZ, Хайятт HH, Marks PA (февраль 1955). «Фосфат тетрозы и образование дифосфата седогептулозы» . Журнал биологической химии . 212 (2): 827–36. PMID 14353884 .
- ^ a b c Гарретт Р.Х., Гришем К.М. (2017). Биохимия . Бостон, Массачусетс: обучение Cengage. С. 611–642. ISBN 978-1-305-57720-6.
- ^ Racker E, Klybas V, Шрамм M (октябрь 1959). «Тетрозодифосфат, специфический ингибитор глицеральдегид-3-фосфатдегидрогеназы» . Журнал биологической химии . 234 : 2510–6. PMID 14435686 .
- ^ Grazi E, De Flora A, S Понтремоли (февраль 1960). «Ингибирование фосфоглюкозоизомеразы D-эритрозо-4-фосфатом». Сообщения о биохимических и биофизических исследованиях . 2 (2): 121–5. DOI : 10.1016 / 0006-291X (60) 90201-1 .
| Эта статья по биохимии незавершена . Вы можете помочь Википедии, расширив ее . |