Циклогексан и изображения ванкозамина (вверху) и эпиванкозамина (внизу) на стуле. Обратите внимание на другой стереоцентр у углерода 4. | |
| Имена | |
|---|---|
| Название ИЮПАК (3 S , 4 S , 5 S ) -3-амино-4,5-дигидрокси-3-метилгексаналь | |
| Другие имена 3-амино-2,3,6-тридеокси-3-метил - L - lyxo -hexopyranose | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 7 H 15 N O 3 | |
| Молярная масса | 161,201 г · моль -1 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ванкозамины - это аминосахара , входящие в состав ванкомицина и других молекул антибиотиков семейства ванкомицинов. Синтез ванкозамина кодируется биосинтетическим кластером ванкомицина ( vps ). Эпиванкозамин, близкородственный аминосахар, кодируется биосинтетическим кластером хлороремомицина ( cep ). [1]
История [ править ]
Ванкозамин был впервые выделен Ломакиной и др. В 1968 году. [2] В 1972 году Джонсон и др. Были первыми, кто идентифицировал и полностью охарактеризовал ванкозамин. [3] Epivancosamine впоследствии был выделен в 1988 году Hunt и др в Eli Lilly [4]
Биосинтез [ править ]
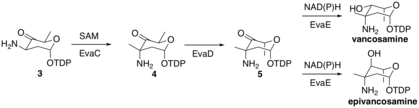
Биосинтез ванкозамина и эпиванкозамина идентичен, за исключением последней стадии. [5] Ферменты, катализирующие реакции, были обозначены как EvaA-E. Молекула TDP-D-глюкозы вступает в этот путь через превращение в молекулу 1 ферментом оксидоредуктазой, а затем ферментом дегидратазой. На следующем этапе EvaA дегидратирует молекулу 1 путем депротонирования при 3-C с образованием и еноляцией, которая затем удаляет 2-OH с образованием молекулы 2. Молекула 2 превращается в молекулу 3 путем таутомеризации в ее кетоформу и затем трансаминируется посредством EvaB использует L-Glu в качестве источника аммиака и PLP в качестве кофактора.
Затем EvaC метилирует молекулу 3 по 3-C с образованием молекулы 4 путем депротонирования с образованием промежуточного енолята, который затем атакует метильную группу SAM в активном центре EvaC. Затем EvaD эпимеризует молекулу 4 при 5-C с образованием молекулы 5. Наконец, EvaE может образовывать эпи / ванкозамин путем восстановления с использованием NADH или NADPH для восстановления карбонила при 4-C. Стереохимический результат зависит от EvaE, который закодирован в биосинтетическом кластере. Ванкомицин vps EvaE приводит к образованию ванкозамина, тогда как хлорэремомицин cep EvaE приводит к образованию эпиванкозамина.
Затем ванкозамины используются клеткой для синтеза ванкомицина и родственных молекул. Гликозилтрансфераза присоединяет аминосахар через α-1 эфирные связи.
Дополнительные модификации возможны в 3-C аминогруппа , чтобы создать N - алкил или N - ацил производные этого сахара.
Всего синтезов [ править ]
Было опубликовано несколько синтезов ванкозамина. [6] [7] [8]
См. Также [ править ]
- Ванкомицин
- Оритаванцин
- Гликопептидные антибиотики
Ссылки [ править ]
- ^ Йим, Г., Такер, М. Н., Котева, К., Райт, Г. «Биосинтез гликопептидных антибиотиков». Журнал антибиотиков , 2017 , 67 , 31-41.
- ^ Ломакина Н.Н., Спиридонова И.А., Bognár, Р., Puksás, М., Sztaricskai Ф. Антибиотики . 1968, 13 , 975.
- ^ Джонсон, А.В., Смит, Р.М., Гатри, Р.Д. «Ванкозамин: структура и конфигурация нового аминосахара из ванкомицина». JCS Perkin I , 1972, 2153-2159.
- ^ Хант, AH, Моллой, RM, Дебоно, М., Окколовиц, JL "Выделение и характеристика 4-эпи-ванкозамина". Tetrahedron Lett , 1988, 29 , 1223-1226.
- ^ Chen, H., Thomas, MG, Hubbard, BK, Losey, HC, Walsh, CT, Burkart, MD «Дезоксисахары в гликопептидных антибиотиках: ферментативный синтез TDP-L-эпиванкозамина в биосинтезе хлорэремомицина». PNAS , 2000 , 97 (22), 11942-11947
- ^ Hauser, FM, Ellenberger, SR, Glusker, JP, Smart, FJ, Carrell, HL «Стереоселективный синтез или +/- даунозамин, +/- ванкозамин и +/- ристозамин из ациклических предшественников». J. Org. Chem. 1986 , 51 , 50-57.
- ^ Николау, KC, Митчелл, HJ, ван Делфт, Флорида, Рюбсам, Ф., Родригрейс, RM «Ускоренные пути к производным и синтезу эвернитрозы и ванкозамина или модели ванкомицин-арилгликозида». Энгью. Chem. Int. Эд. 1998 , 37 , № 13/14, 1871–1874.
- ^ Паркер, К.А., Чанг, В. «Синтез производных L-ванкозамина из неуглеводных предшественников с помощью короткой последовательности на основе реакций Маршалла, Макдональда и Дюбуа». Орг. Lett. 2003 , 5 (21), 3891-3893.