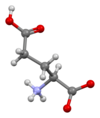
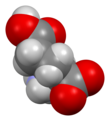
Скелетная формула из L глутаминовой кислоты | |||
 | |||
| Имена | |||
|---|---|---|---|
| Систематическое название ИЮПАК 2-аминопентандиовая кислота | |||
| Другие имена 2-аминоглутаровая кислота | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 3DMet |
| ||
| 1723801 (L) 1723799 (rac) 1723800 (D) | |||
| ЧЭБИ |
| ||
| ЧЭМБЛ |
| ||
| ChemSpider |
| ||
| DrugBank | |||
| ECHA InfoCard | 100.009.567 | ||
| Номер ЕС |
| ||
| Номер E | E620 (усилитель вкуса) | ||
| 3502 (л) 101971 (rac) 201189 (д) | |||
| КЕГГ | |||
PubChem CID | |||
| UNII |
| ||
Панель управления CompTox ( EPA ) |
| ||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
Химическая формула | C 5 H 9 N O 4 | ||
| Молярная масса | 147,130 г · моль -1 | ||
| Внешность | белый кристаллический порошок | ||
| Плотность | 1,4601 (20 ° С) | ||
| Температура плавления | 199 ° С (390 ° F, 472 К) разлагается | ||
Растворимость в воде | 7,5 г / л (20 ° C) [1] | ||
| Растворимость | 0,00035 г / 100 г этанола (25 ° C) [2] | ||
| Кислотность (p K a ) | 2.10, 4.07, 9.47 [3] | ||
Магнитная восприимчивость (χ) | -78,5 · 10 −6 см 3 / моль | ||
| Опасности | |||
| Паспорт безопасности | См .: страницу данных | ||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Предупреждение | ||
Положения об опасности GHS | H315 , H319 , H335 | ||
Меры предосторожности GHS | Р261 , Р264 , Р271 , Р280 , Р302 + 352 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , Р405 , Р501 | ||
| NFPA 704 (огненный алмаз) |  2 1 0 | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Глутаминовая кислота (символ Glu или Е ; [4] ионная форма известен как глутамат ) представляет собой α- аминокислота , которая используется почти во всех живых существах в биосинтезе из белков . Для человека это несущественно, то есть организм может его синтезировать. Это также возбуждающий нейротрансмиттер , фактически самый распространенный в нервной системе позвоночных . Он служит предшественником синтеза ингибирующей гамма-аминомасляной кислоты (ГАМК) в ГАМК-ергических нейронах.
Имеет формулу C
5ЧАС
9О
4N . Его молекулярную структуру можно было бы идеализировать как HOOC-CH ( NH
2) - ( CH
2) 2 -COOH, с двумя карбоксильными группами -COOH и одной аминогруппой - NH
2. Однако в твердом состоянии и слабокислых водных растворах молекула принимает электрически нейтральную цвиттерионную структуру - OOC-CH ( NH+
3) - ( CH
2) 2 -COOH. Он кодируется с помощью кодонов GAA или GAG.
Кислота может потерять один протон из своей второй карбоксильной группы с образованием конъюгированного основания , однозначно отрицательного аниона глутамата - OOC-CH ( NH+
3) - ( CH
2) 2 -COO - . Эта форма соединения преобладает в нейтральных растворах. Глутамат нейротрансмиттер играет главную роль в нервной активации . [5] Этот анион также отвечает за пикантный вкус ( умами ) некоторых продуктов и используется в глутаматных ароматизаторах, таких как глутамат натрия . В Европе классифицируется как пищевая добавка E620 . В сильнощелочных растворах дважды отрицательный анион - OOC-CH ( NH
2) - ( CH
2) 2 -COO - преобладает. Радикал , соответствующий глутамата называется глутамил .
Химия [ править ]
Ионизация [ править ]
Когда глутаминовая кислота растворяется в воде, аминогруппа (- NH
2) может получить протон ( H+
), и / или карбоксильные группы могут терять протоны, в зависимости от кислотности среды.
В достаточно кислой среде аминогруппа приобретает протон, и молекула становится катионом с одним положительным зарядом, HOOC-CH ( NH+
3) - ( CH
2) 2 -COOH. [6]
При значениях pH от 2,5 до 4,1 [6] карбоновая кислота, более близкая к амину, обычно теряет протон, и кислота становится нейтральным цвиттерионом - OOC-CH ( NH+
3) - ( CH
2) 2 -COOH. Это также форма соединения в твердом кристаллическом состоянии. [7] [8] Изменение состояния протонирования происходит постепенно; две формы находятся в равных концентрациях при pH 2,10. [9]
При еще более высоком pH другая группа карбоновой кислоты теряет свой протон, и кислота существует почти полностью в виде глутамат- аниона - OOC-CH ( NH+
3) - ( CH
2) 2 -COO - с одним отрицательным зарядом в целом. Изменение состояния протонирования происходит при pH 4,07. [9] Эта форма, в которой оба карбоксилата не содержат протонов, является доминирующей в физиологическом диапазоне pH (7,35–7,45).
При еще более высоком pH аминогруппа теряет лишний протон, и преобладающим видом является дважды отрицательный анион - OOC-CH ( NH
2) - ( CH
2) 2 -COO - . Изменение состояния протонирования происходит при pH 9,47. [9]
Оптическая изомерия [ править ]
Углерода атом прилегает к аминогруппе является хиральным (подключен к четырем различным группам), так что глутаминовая кислота может существовать в двух оптических изомеров , д (-) и л (+). Л форма является одним из наиболее широко встречающихся в природе, но д форма встречается в некоторых специальных контекстах, например, клеточные стенки этих бактерий (которые могут его производство из л формы с ферментом глутаматом рацемазом ) и печенью из млекопитающих . [10] [11]
История [ править ]
Хотя они естественным образом присутствуют во многих продуктах питания, вклад глутаминовой кислоты и других аминокислот во вкус был научно идентифицирован только в начале двадцатого века. Вещество было обнаружено и идентифицировано в 1866 году немецким химиком Карлом Генрихом Риттхаузеном, который обработал пшеничный глютен (в честь которого он был назван) серной кислотой . [12] В 1908 году японский исследователь Кикунаэ Икеда из Императорского университета Токио обнаружил коричневые кристаллы, оставшиеся после испарения большого количества комбу.бульон в виде глутаминовой кислоты. Эти кристаллы, когда их попробовали, воспроизводили невыразимый, но неоспоримый аромат, который он обнаруживал во многих продуктах, особенно в морских водорослях. Профессор Икеда назвал этот аромат умами . Затем он запатентовал метод массового производства кристаллической соли глутаминовой кислоты, глутамата натрия . [13] [14]
Синтез [ править ]
Биосинтез [ править ]
| Реагенты | Товары | Ферменты |
|---|---|---|
| Глютамин + H 2 O | → Глу + NH 3 | GLS , GLS2 |
| NAcGlu + H 2 O | → Глю + ацетат | N- ацетил-глутамат-синтаза |
| α-кетоглутарат + НАДФ H + NH 4 + | → Глу + НАДФ + + Н 2 О | GLUD1 , GLUD2 [15] |
| α-кетоглутарат + α-аминокислота | → Глу + α-кетокислота | трансаминаза |
| 1-пирролин-5-карбоксилат + НАД + + H 2 O | → Глу + НАДН | ALDH4A1 |
| N-формино-L-глутамат + FH 4 | → Glu + 5-формимино-FH 4 | FTCD |
| НААГ | → Glu + NAA | GCPII |
Промышленный синтез [ править ]
Глутаминовая кислота производится в самых больших масштабах из всех аминокислот, с расчетным годовым производством около 1,5 миллионов тонн в 2006 году. [16] На смену химическому синтезу в 1950-х годах пришла аэробная ферментация сахаров и аммиака с организмом Corynebacterium glutamicum. (также известный как Brevibacterium flavum ), наиболее широко используемый в производстве. [17] Выделение и очистка могут быть достигнуты путем концентрирования и кристаллизации ; он также широко доступен в виде гидрохлоридной соли. [18]
Функция и использование [ править ]
Метаболизм [ править ]
Глутамат - ключевое соединение в клеточном метаболизме . У человека пищевые белки расщепляются на аминокислоты , которые служат метаболическим топливом для других функциональных ролей в организме. Ключевым процессом деградации аминокислот является трансаминирование , при котором аминогруппа аминокислоты переносится на α-кетокислоту, обычно катализируемую трансаминазой . Реакцию можно обобщить как таковую:
- R 1 -аминокислота + R 2 -α- кетокислота ⇌ R 1 -α-кетокислота + R 2 -аминокислота
Очень распространенной α-кетокислотой является α-кетоглутарат, промежуточный продукт в цикле лимонной кислоты . Трансаминирование α-кетоглутарата дает глутамат. Полученный продукт α-кетокислоты также часто является полезным, который может использоваться в качестве топлива или в качестве субстрата для дальнейших процессов метаболизма. Вот примеры:
- Аланин + α-кетоглутарат ⇌ пируват + глутамат
- Аспартат + α-кетоглутарат ⇌ оксалоацетат + глутамат
И пируват, и оксалоацетат являются ключевыми компонентами клеточного метаболизма, участвуя в качестве субстратов или промежуточных продуктов в фундаментальных процессах, таких как гликолиз , глюконеогенез и цикл лимонной кислоты .
Глутамат также играет важную роль в избавлении организма от избыточного или отработанного азота . Глутамат подвергается дезаминирования , окислительной реакции , катализируемой глутаматдегидрогеназы , [15] следующим образом :
- глутамат + H 2 O + NADP + → α-кетоглутарат + NADPH + NH 3 + H +
Аммиак (в виде аммония ) выводится преимущественно в виде мочевины , синтезируемой в печени . Таким образом, трансаминирование может быть связано с дезаминированием, что позволяет эффективно удалять азот из аминогрупп аминокислот через глутамат в качестве промежуточного соединения и, наконец, выводиться из организма в форме мочевины.
Глутамат также является нейромедиатором (см. Ниже), что делает его одной из самых распространенных молекул в головном мозге. Злокачественные опухоли головного мозга, известные как глиома или глиобластома, используют это явление, используя глутамат в качестве источника энергии, особенно когда эти опухоли становятся более зависимыми от глутамата из-за мутаций в гене IDH1 . [19] [20]
Нейротрансмиттер [ править ]
Глутамат является наиболее распространенным возбуждающим нейромедиатором в нервной системе позвоночных . [21] В химических синапсах глутамат хранится в пузырьках . Нервные импульсы вызывают высвобождение глутамата из пресинаптической клетки. Глутамат действует на ионотропные и метаботропные (связанные с G-белком) рецепторы. [21] В противоположной постсинаптической клетке рецепторы глутамата , такие как рецептор NMDA или рецептор AMPA , связывают глутамат и активируются. Из-за его роли в синаптической пластичности, глутамат участвует в когнитивных функциях, таких как обучение и память в головном мозге. [22] Форма пластичности, известная как долговременная потенциация, имеет место в глутаматергических синапсах в гиппокампе , неокортексе и других частях мозга. Глутамат работает не только как двухточечный передатчик, но также через синаптические перекрестные помехи между синапсами, в которых сумма глутамата, высвобождаемого из соседнего синапса, создает внесинаптическую передачу сигналов / объемную передачу . [23] Кроме того, глутамат играет важную роль в регуляции конусов роста исинаптогенез во время развития мозга, как первоначально описал Марк Маттсон .
Мозговые несинаптические глутаматергические сигнальные цепи [ править ]
Было обнаружено, что внеклеточный глутамат в мозге дрозофилы регулирует кластеризацию постсинаптических рецепторов глутамата посредством процесса, включающего десенсибилизацию рецепторов. [24] Ген, экспрессируемый в глиальных клетках, активно транспортирует глутамат во внеклеточное пространство , [24] в то время как в ядерном ядре, стимулирующем метаботропные рецепторы глутамата II группы, этот ген снижает уровень внеклеточного глутамата. [25] Это повышает вероятность того, что этот внеклеточный глутамат играет «эндокринную» роль как часть более крупной гомеостатической системы.
Предшественник ГАМК [ править ]
Глутамат также служит предшественником синтеза ингибирующей гамма-аминомасляной кислоты (ГАМК) в ГАМК-ергических нейронах. Эта реакция катализируется глутаматдекарбоксилазой (GAD), которая наиболее распространена в мозжечке и поджелудочной железе . [ необходима цитата ]
Синдром скованного человека - это неврологическое заболевание, вызванное антителами против GAD, которое приводит к снижению синтеза ГАМК и, следовательно, к нарушению двигательной функции, такой как жесткость мышц и спазм. Поскольку в поджелудочной железе много ГТР, в поджелудочной железе происходит прямое иммунологическое разрушение, и у пациентов возникает сахарный диабет. [ необходима цитата ]
Усилитель вкуса [ править ]
Глутаминовая кислота, входящая в состав белка, присутствует в пищевых продуктах, содержащих белок, но ее можно попробовать только тогда, когда она присутствует в несвязанной форме. Значительные количества свободной глутаминовой кислоты присутствует в широком разнообразии продуктов, включая сыры и соевый соус , и глутаминовая кислота отвечает за умы , один из пяти основных вкусов человеческого чувства вкуса . Глутаминовая кислота часто используется в качестве пищевой добавки и усилителя вкуса в виде ее натриевой соли , известной как глутамат натрия ( глутамат натрия ).
Питательный [ править ]
Все мясо, птица, рыба, яйца, молочные продукты и комбу являются отличными источниками глутаминовой кислоты. Некоторые богатые белком растительные продукты также служат его источниками. От 30% до 35% глютена (большая часть белка в пшенице) составляет глутаминовая кислота. Девяносто пять процентов пищевого глутамата метаболизируется клетками кишечника за первый проход. [26]
Рост растений [ править ]
Ауксигро - это препарат для выращивания растений, содержащий 30% глутаминовой кислоты.
ЯМР-спектроскопия [ править ]
В последние годы [ когда? ] было проведено много исследований по использованию остаточной диполярной связи (RDC) в спектроскопии ядерного магнитного резонанса (ЯМР). Производное глутаминовой кислоты, поли-γ-бензил-L-глутамат (PBLG), часто используется в качестве среды для выравнивания, чтобы контролировать масштаб наблюдаемых диполярных взаимодействий. [27]
Фармакология [ править ]
Лекарственный препарат фенциклидин (более известный как PCP) неконкурентно антагонизирует глутаминовую кислоту в отношении рецептора NMDA . По тем же причинам декстрометорфан и кетамин также обладают сильным диссоциативным и галлюциногенным действием («Ангельская пыль», как наркотик). Острое вливание препарата LY354740 (также известный как eglumegad , с агонистом из метаботропных глутаматных рецепторов , 2 и 3 ) приводило к заметному уменьшению йохимбина индуцированного ответа на стрессеу шляпных макак ( Macaca radiata ); хроническое пероральное введение LY354740 этим животным привело к заметному снижению исходных уровней кортизола (примерно на 50 процентов) по сравнению с необработанными контрольными субъектами. [28] Было также продемонстрировано, что LY354740 действует на метаботропный глутаматный рецептор 3 (GRM3) клеток коры надпочечников человека , подавляя альдостерон-синтазу , CYP11B1 , и производство стероидов надпочечников (например, альдостерона и кортизола ). [29] Глутамат плохо проникает через гематоэнцефалический барьер., но вместо этого транспортируется высокоаффинной транспортной системой. [30] [31] Он также может превращаться в глютамин .
См. Также [ править ]
- Аденозинмонофосфат
- Аджиномото
- Глутамат натрия
- Динатрия инозинат
- Глутаматный ароматизатор
- Монофосфат гуанозина
- Инозиновая кислота
- Каиновая кислота
- Глутамат калия
- Тянь Чу Ве-Цинь
Ссылки [ править ]
- ^ "L-глутаминовая кислота CAS #: 56-86-0" . www.chemicalbook.com .
- ^ Белиц, H.-D; Грош, Вернер; Шиберле, Питер (27 февраля 2009 г.). Пищевая химия . ISBN 978-3540699330.
- ^ "Аминокислотные структуры" . cem.msu.edu. Архивировано из оригинала на 1998-02-11.
- ^ «Номенклатура и символика аминокислот и пептидов» . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из оригинала 9 октября 2008 года . Проверено 5 марта 2018 .
- ^ Роберт Сапольски (2005), Биология и поведение человека: неврологические истоки индивидуальности (2-е издание); Обучающая компания . стр. 19–20 Путеводителя
- ^ a b Альберт Нойбергер (1936), "Константы диссоциации и структуры глутаминовой кислоты и ее сложных эфиров". Биохимический журнал , том 30, выпуск 11, статья CCXCIII, стр. 2085–2094. PMC 1263308 .
- ^ Rodante, F .; Марросу, Г. (1989). «Термодинамика вторых процессов диссоциации протонов девяти α-аминокислот и третьих процессов ионизации глутаминовой кислоты, аспарагиновой кислоты и тирозина». Thermochimica Acta . 141 : 297–303. DOI : 10.1016 / 0040-6031 (89) 87065-0 .
- ^ Lehmann, Mogens S .; Koetzle, Thomas F .; Гамильтон, Уолтер С. (1972). «Прецизионное определение структуры белков и нуклеиновых кислот с помощью дифракции нейтронов. VIII: кристаллическая и молекулярная структура β-формы аминокислоты-глутаминовой кислоты». Журнал кристаллов и молекулярной структуры . 2 (5): 225–233. DOI : 10.1007 / BF01246639 . S2CID 93590487 .
- ^ a b c Уильям Х. Браун и Лоуренс С. Браун (2008), Органическая химия (5-е издание). Cengage Learning. п. 1041. ISBN 0495388572 , 978-0495388579 .
- ^ Национальный центр биотехнологической информации, " D-глутамат ". База данных PubChem Compound , CID = 23327. Проверено 17 февраля 2017 г.
- ^ Лю, L; Йошимура, Т; Эндо, К; Кишимото, К; Fuchikami, Y; Manning, JM; Esaki, N; Сода, К. (1998). «Компенсация ауксотрофии по D-глутамату Escherichia coli WM335 геном D-аминокислотной аминотрансферазы и регуляция экспрессии murI». Биология, биотехнология и биохимия . 62 (1): 193–195. DOI : 10.1271 / bbb.62.193 . PMID 9501533 .
- ^ RHA Plimmer (1912) [1908]. RHA Plimmer; Ф.Г. Хопкинс (ред.). Химическая конституция белка . Монографии по биохимии. Часть I. Анализ (2-е изд.). Лондон: Longmans, Green and Co., стр. 114 . Проверено 3 июня 2012 года .
- ^ Рентон, Алекс (2005-07-10). «Если глутамат натрия так вреден для вас, почему не у всех в Азии болит голова?» . Хранитель . Проверено 21 ноября 2008 .
- ^ "Кикунаэ Икеда Глутамат натрия" . Патентное ведомство Японии . 2002-10-07. Архивировано из оригинала на 2007-10-28 . Проверено 21 ноября 2008 .
- ^ а б Грабовская, А .; Новицки, М .; Квинта, Дж. (2011). «Глутаматдегидрогеназа прорастающих семян тритикале: экспрессия генов, распределение активности и кинетические характеристики» . Acta Physiologiae Plantarum . 33 (5): 1981–1990. DOI : 10.1007 / s11738-011-0801-1 .
- ^ Альвизе Пероса; Фульвио Зеккини (2007). Методы и реагенты для зеленой химии: Введение . Джон Вили и сыновья. п. 25. ISBN 978-0-470-12407-9.
- ^ Майкл С. Фликингер (2010). Энциклопедия промышленной биотехнологии: биопроцесс, биоразделение и клеточная технология, набор из 7 томов . Вайли. С. 215–225. ISBN 978-0-471-79930-6.
- ^ Фоли, Патрик; Kermanshahi pour, Azadeh; Пляж, Эван С .; Циммерман, Джули Б. (2012). «Получение и синтез возобновляемых поверхностно-активных веществ». Chem. Soc. Ред . 41 (4): 1499–1518. DOI : 10.1039 / C1CS15217C . ISSN 0306-0012 . PMID 22006024 .
- ^ ван Лит, SA; Navis, AC; Verrijp, K; Никлоу, ИП; Bjerkvig, R; Wesseling, P; Топы, B; Molenaar, R; van Noorden, CJ; Лендерс, WP (август 2014 г.). «Глутамат как хемотаксическое топливо для диффузных клеток глиомы: они присоски глутамата?». Biochimica et Biophysica Acta (BBA) - Обзоры рака . 1846 (1): 66–74. DOI : 10.1016 / j.bbcan.2014.04.004 . PMID 24747768 .
- ^ ван Лит, SA; Molenaar, R; van Noorden, CJ; Лендерс, WP (декабрь 2014 г.). «Опухолевые клетки в поисках глутамата: альтернативное объяснение повышенной инвазивности мутантных глиом IDH1» . Нейроонкология . 16 (12): 1669–1670. DOI : 10.1093 / neuonc / nou152 . PMC 4232089 . PMID 25074540 .
- ^ а б Мелдрам, BS (2000). «Глутамат как нейромедиатор в головном мозге: Обзор физиологии и патологии» . Журнал питания . 130 (4S Доп.): 1007S – 1015S. DOI : 10.1093 / JN / 130.4.1007s . PMID 10736372 .
- ^ McEntee, WJ; Крук, TH (1993). «Глутамат: его роль в обучении, памяти и старении мозга». Психофармакология . 111 (4): 391–401. DOI : 10.1007 / BF02253527 . PMID 7870979 . S2CID 37400348 .
- ^ Окубо, Й .; Sekiya, H .; Namiki, S .; Sakamoto, H .; Iinuma, S .; Yamasaki, M .; Watanabe, M .; Hirose, K .; Иино, М. (2010). «Визуализация внесинаптической динамики глутамата в головном мозге» . Труды Национальной академии наук . 107 (14): 6526–6531. Bibcode : 2010PNAS..107.6526O . DOI : 10.1073 / pnas.0913154107 . PMC 2851965 . PMID 20308566 .
- ^ a b Огюстен Х, Грожан И, Чен К., Шэн К., Фезерстоун, DE (2007). «Невезикулярное высвобождение глутамата глиальными транспортерами xCT подавляет кластеризацию глутаматных рецепторов in vivo» . Журнал неврологии . 27 (1): 111–123. DOI : 10.1523 / JNEUROSCI.4770-06.2007 . PMC 2193629 . PMID 17202478 .
- ^ Чжэн Си; Бейкер Д.А.; Шен Х; Carson DS; Каливас П.В. (2002). «Метаботропные рецепторы глутамата группы II модулируют внеклеточный глутамат в прилежащем ядре». Журнал фармакологии и экспериментальной терапии . 300 (1): 162–171. DOI : 10,1124 / jpet.300.1.162 . PMID 11752112 .
- ^ Ридс, П.Дж.; и другие. (1 апреля 2000 г.). «Кишечный метаболизм глутамата» . Журнал питания . 130 (4s): 978S – 982S. DOI : 10.1093 / JN / 130.4.978S . PMID 10736365 .
- ↑ CM Thiele, Concepts Magn. Резон. А, 2007, 30А, 65–80
- ^ Coplan JD, Mathew SJ, Смит EL, Трост RC, Scharf Б.А., Мартинес J, Горман JM, Monn JA, Schoepp DD, Розенблюм Л.А. (июль 2001). «Эффекты LY354740, нового глутаматергического метаботропного агониста, на гипоталамо-гипофизарно-надпочечниковую ось и норадренергическую функцию приматов». CNS Spectr . 6 (7): 607-612, 617. DOI : 10,1017 / S1092852900002157 . PMID 15573025 .
- ^ Felizola SJ, Накамура Y, Сато Р, Р Моримото, Кикучи К, Т Накамура, Hozawa А, Ван L, Онодера Y, Исэ К, КМ Макнамара, Midorikawa S, S Сузуки, Sasano Н (январь 2014). «Рецепторы глутамата и регуляция стероидогенеза в надпочечниках человека: метаботропный путь». Молекулярная и клеточная эндокринология . 382 (1): 170–177. DOI : 10.1016 / j.mce.2013.09.025 . PMID 24080311 . S2CID 3357749 .
- ^ Смит, Квентин Р. (апрель 2000 г.). «Транспорт глутамата и других аминокислот через гематоэнцефалический барьер» . Журнал питания . 130 (4S Доп.): 1016S – 1022S. DOI : 10.1093 / JN / 130.4.1016S . PMID 10736373 .
- ^ Хокинс, Ричард А. (сентябрь 2009 г.). «Гематоэнцефалический барьер и глутамат» . Американский журнал клинического питания . 90 (3): 867S – 874S. DOI : 10.3945 / ajcn.2009.27462BB . PMC 3136011 . PMID 19571220 .
Эта организация не позволяет чистому глутамату проникать в мозг;
скорее, он способствует удалению глутамата и поддержанию низких концентраций глутамата в ECF.
Дальнейшее чтение [ править ]
| Викискладе есть медиафайлы по теме глутаминовой кислоты . |
- Нельсон, Дэвид Л .; Кокс, Майкл М. (2005). Принципы биохимии (4-е изд.). Нью-Йорк: В. Х. Фриман. ISBN 0-7167-4339-6.
Внешние ссылки [ править ]
| Поищите глутаминовую кислоту в Викисловаре, бесплатном словаре. |
- Глутаминовая кислота MS Spectrum