 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Гестанин, Гестанон, Перселин, Туринал, другие |
| Другие имена | Аллилоэстренол; SC-6393; Org AL-25; 3-декето-17α-аллил-19-нортестостерон; 17α-аллилестр-4-ен-17β-ол; 17α- (проп-2-ен-1-ил) эстр-4-ен-17β-ол |
Категория беременности |
|
| Пути администрирования | Устно |
| Класс препарата | Гестаген ; Прогестин |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетические данные | |
| Связывание с белками | «Значительный» [1] [2] (и низкое сродство к SHBG ) [3] |
| Метаболизм | Печень ( восстановление , гидроксилирование , конъюгация ; CYP3A4 ) [1] [2] [5] |
| Метаболиты | • 17α-Аллил-19-NT [3] [1] [2] |
| Ликвидация Период полураспада | «Несколько часов» или 10 часов [4] [1] [2] |
| Экскреция | Моча (в виде конъюгатов) [1] [2] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider |
|
| UNII |
|
| КЕГГ |
|
| ЧЭБИ |
|
| ЧЭМБЛ |
|
| Панель управления CompTox ( EPA ) |
|
| ECHA InfoCard | 100.006.440 |
| Химические и физические данные | |
| Формула | С 21 Н 32 О |
| Молярная масса | 300,486 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
| (проверять) | |
Аллилестренол , продаваемый, среди прочего, под торговыми марками Гестанин и Туринал , представляет собой прогестиновый препарат, который используется для лечения повторяющихся и угрожающих выкидышей, а также для предотвращения преждевременных родов у беременных . [6] [7] [8] Однако, за исключением случая доказанного дефицита прогестерона , его использование для таких целей больше не рекомендуется. [6] Он также используется в Японии для лечения доброкачественной гиперплазии предстательной железы (ДГПЖ) у мужчин. [9] [10] [11]Лекарство используется отдельно и не сочетается с эстрогенами . [12] Принимается внутрь . [13]
Побочные эффекты аллилестренола немногочисленны и не были четко определены, но предполагается, что они аналогичны побочным эффектам родственных лекарств. [14] аллилэстренол является прогестин, или синтетический прогестаген , и , следовательно , является агонистом из рецептора прогестерона , то биологическая мишень прогестагенов как прогестерон . [15] У него нет другой важной гормональной активности. [3] [16] Препарат представляет собой пролекарство из 17 & alpha; аллил-19-нортестостерона (3-ketoallylestrenol) в организме. [17] [18] [3]
Аллилестренол был впервые описан в 1958 году и был введен для медицинского применения в 1961 году. [19] [20] [21] [22] В прошлом он широко продавался во всем мире, но сегодня его доступность и использование относительно ограничены. [23] [6] [24] [25] Он по-прежнему доступен в нескольких европейских странах и в ряде азиатских стран. [23] [6] [24] [25]
Медицинское использование [ править ]
Аллилестренол используется для лечения повторяющихся и угрожающих выкидышей, а также для предотвращения преждевременных родов . [6] [7] Однако, за исключением случая доказанного дефицита прогестерона , его использование по таким показаниям больше не рекомендуется. [6] Аллилестренол является одним из немногих прогестагенов, которые обычно используются для таких целей, другие включают прогестерон , гидроксипрогестерона капроат и дидрогестерон . [8] Препарат также изучался при лечении гинекологических заболеваний, таких как аменорея., нерегулярные менструации и предменструальный синдром . [14] В отличие от других прогестинов, аллилестренол не использовался в гормональной контрацепции или в гормональной терапии менопаузы . В одном исследовании было обнаружено, что он неадекватен для трансформации эндометрия у женщин в сочетании с валератом эстрадиола . [26] С другой стороны, аллилестренол оказался эффективным при лечении приливов у женщин в постменопаузе. [27]
Аллилестренол обычно используется в Японии в высоких дозах, обычно от 50 до 100 мг / день, для лечения ДГПЖ у мужчин. [11] [28] [29] [30] [31] [32] [33] [34] [35] [9] [10] [36] [37] [38] [39] [40] [41 ] ] [42] [43] Родственные лекарства, которые аналогичным образом использовались для лечения аденомы простаты, особенно в Японии, включают ацетат хлормадинона , гестоноронкапроат и оксендолон . [33] [38] Аллилестренол также изучался при лечениирак простаты в Японии. [44] [28] Препарат изучался как блокатор полового созревания при лечении преждевременного полового созревания . [45]
Доступные формы [ править ]
Аллилестренол выпускается в форме таблеток для приема внутрь по 5 мг . [12] [46] [47] Обычно он используется в дозировке от 5 до 40 мг / день. [46] [47] В Японии для лечения аденомы простаты продаются пероральные таблетки аллилестренола 25 мг под торговой маркой Perselin. [37]
Побочные эффекты [ править ]
Побочные эффекты аллилестренола немногочисленны и не были четко определены, но предполагается, что они аналогичны побочным эффектам родственных лекарств (например, других прогестинов). [14] При использовании при высоких дозах при лечении доброкачественной гиперплазии простаты у мужчин, аллилэстренол может вызвать симптомы из гипогонадизма и сексуальной дисфункции . [31] [34] [35] Лекарство инделоксазин может противодействовать сексуальной дисфункции, связанной с аллилестренолом. [39] аллилэстренол не имеет андрогенных или другие офф-мишени гормональные побочные эффекты. [31] [3] [16]
Фармакология [ править ]
Фармакодинамика [ править ]
Прогестагенные и нецелевые действия [ править ]
Аллилэстренол является прогестагеном , или агонист из рецептора прогестерона (PR). [15] В нем отсутствует кетогруппа в положении C3 (часть важной структуры 3-кето-4-ена ), которая характерна для прогестагенов и считается необходимой для активности, и в связи с этим считается быть пролекарством из 17 & alpha; аллил-19-нортестостерона (3-ketoallylestrenol). [17] [18] [48] Аллилестренол является гораздо менее мощным гестагеном, чем многие другие производные 19-нортестостерона. [15] Эффективное подавление овуляции илиКонтрацептивная доза аллилестренола для женщин изучалась, хотя и ограниченно. [49] При приеме аллилестренола 20 мг / день овуляция произошла в 50% из 6 циклов, а при дозе 25 мг / день овуляция произошла в 0% из 3 циклов. [49] [50] Общая доза аллилестренола для трансформации эндометрия у женщин в течение всего цикла составляет от 150 до 250 мг. [51] В отличие от практически всех других производных 19-нортестостерона, аллилестренол считается чистым прогестогеном и, следовательно, лишен андрогенной , эстрогенной и глюкокортикоидной активности. [3] [16] Таким образом, кажется, что он имеет свойства, более похожие на свойства естественногопрогестерон . [3] [16]
Были изучены профили связывания и активности аллилестренола и его основного активного метаболита на рецепторах стероидных гормонов и родственных белках . [3] [17] аллилэстренол имеет меньше , чем 0,2% от аффинности в ОРГ-2058 и менее чем 2% от сродства прогестерона для ПР. [3] Точно так же он имеет менее 0,2% сродства тестостерона к рецептору андрогенов (AR), менее 0,2% сродства эстрадиола к рецептору эстрогена (ER), менее 0,2% сродства дексаметазона. длярецептор глюкокортикоидов (GR) и 0,9% сродства тестостерона к глобулину, связывающему половые гормоны (SHBG). [3] И наоборот, его метаболит 17α-аллил-19-нортестостерон имеет 24% сродства ORG-2058 и 186% сродства прогестерона к PR, 4,5% сродства тестостерона к AR, 9,8% сродства сродство дексаметазона к GR и 2,8% сродства тестостерона к SHBG, тогда как сродство эстрадиола к ER составляет менее 0,2%. [3] Сродство 17α-аллил-19-нортестостерона к AR было меньше, чем сродство норэтистерона и медроксипрогестерона ацетата.и его сродство к SHBG было намного ниже, чем сродство норэтистерона. [3] Эти данные могут помочь объяснить отсутствие тератогенного воздействия аллилестренола на наружные гениталии плодов самок и самцов крыс . [3]
| Сложный | PR | AR | ER | GR | МИСТЕР | ГСПГ | CBG |
|---|---|---|---|---|---|---|---|
| Аллилестренол | 0 | 0 | 0 | 0 | ? | 1 | ? |
| 17α-Аллил-19-NT | 186 | 5 | 0 | 10 | ? | 3 | ? |
| Примечания: Значения даны в процентах (%). Контрольными лигандами (100%) были P4 для PR , T для AR , E2 для ER , DEXA для GR , альдостерон для MR , T для SHBG и кортизол для CBG . Источники: [3] | |||||||
Антигонадотропные эффекты [ править ]
Как и другие гестагены, аллилестренол обладает сильным антигонадотропным действием. [52] Он способен значительно снизить циркулирующие концентрации лютеинизирующего гормона , тестостерона и дигидротестостерона у мужчин. [32] [34] [39] [40] Было обнаружено, что в дозировке 50 мг / день аллилестренол снижает уровень циркулирующего тестостерона на 78% у мужчин с ДГПЖ. [52] Это примерно максимальная способность прогестагенов подавлять уровень тестостерона у мужчин. [53] [54] [55]Соответственно, снижение уровня тестостерона и лютеинизирующего гормона при приеме аллилестренола у мужчин, как было обнаружено в исследовании, эквивалентно таковому при применении хлормадинона ацетата и оксендолона . [33] Тем не менее, другое исследование показало значительно более низкое снижение уровня тестостерона при приеме аллилестренола 50 мг / день по сравнению с 50 мг / день хлормадинона ацетатом примерно на 49–52% против 76–85%, соответственно. [34] Исследования на животных показывают, что аллилестренол оказывает положительное влияние на ДГПЖ благодаря своим антигонадотропным эффектам и последующему подавлению уровня андрогенов и ингибированию роста предстательной железы , как и другие прогестины. [52]Некоторые исследования показали, что аллилестренол менее эффективен при ДГПЖ, чем хлормадинона ацетат, но также вызывает меньше побочных эффектов и сексуальной дисфункции . [31] [34] [35] Аллилестренол при аденоме простаты ассоциируется со значительным снижением уровня простат-специфического антигена , что может маскировать выявление рака простаты. [52] [43]
Другая деятельность [ править ]
Аллилестренол не является значительным ингибитором 5α-редуктазы . [52] В одном исследовании, он показал около 80000 раз более низкую активность для ингибирования от 5 -редуктазы в пробирке , чем установленный 5α-редуктазы ингибитор эпристерид ( IC 50 = 11,3 нМ для эпристерид и 890 мкМ для аллилэстренол). [52] В другом исследовании было обнаружено 70% ингибирование 5α-редуктазы аллилестренолом в концентрации 60 мкМ. [52] Это различие могло быть связано с разными экспериментальными условиями, но все же намного меньше, чем у эпристерида. [52]
Фармакокинетика [ править ]
После перорального приема , пиковые уровни из аллилэстренол происходит после того, как от 2 до 4 часов. [1] [2] Препарат демонстрирует значительное связывание с белками плазмы . [1] [2] Он имеет относительно низкое сродство к SHBG, намного ниже, чем сродство норэтистерона. [3] Аллилестренол метаболизируется в печени путем восстановления , гидроксилирования и конъюгации . [1] [2] Известно , что быть субстратом из CYP3A4 . [5] Считается, что этопролекарство из 17 & alpha-аллил-19-нортестостерона (3-ketoallylestrenol), который, в соответствии, как известно , является активным метаболитом из аллилэстренола. [17] [18] биологический период полураспада по аллилэстренол было сообщено, что «несколько часов» или, предположительно , в его активной форме, как сообщается , около 10 часов. [1] [2] [4] В крови на неизмененный аллилестренол приходилось от 15 до 40% радиоактивности , на неконъюгированный метаболит приходилось от 4 до 10% радиоактивности, а остальная часть радиоактивности соответствовала конъюгированным метаболитам. [1] [2] Аллилестренол выводится в основном черезмоча , 44% через 24 часа и 67% через 4 дня. [1] [2] Он почти полностью выводится в виде конъюгатов, 75% из которых составляют сульфатные конъюгаты, а 24% - глюкуронидные конъюгаты. [1] [2]
Химия [ править ]
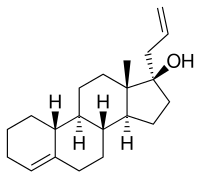
Аллилэстренол, известный также как 3-deketo-17 & alpha; аллил-19-нортестостерона или 17 & alpha; allylestr-4-ен-17b-ола, является синтетическим эстрана стероида и производного от тестостерона . [56] Он является членом подгруппы эстрана семейства прогестинов 19-нортестостерона [57], но, в отличие от большинства других прогестинов 19-нортестостерона, не является производным норэтистерона (17α-этинил-19-нортестостерон). [58] [3] [18] Это потому, что он имеет аллильную группу в положении C17α, а не обычную этинильную группу . [58] [3][18] Таким образом, наряду с альтреногестом (17α-аллил-19-нор-δ 9,11- тестостерон), аллилестренол является производным 17α-аллилтестостерона, а не 17α-этинилтестостерона . [58] [3] [18]
Аллилестренол также уникален среди большинства прогестинов 19-нортестостерона тем, что в нем отсутствует кетон в положении C3. [56] Он разделяет это свойство с линестренолом (17α-этинилэстр-4-ен-17β-ол), дезогестрелом (11-метилен-17α-этинил-18-метилэстр-4-ен-17β-ол) и анаболиком - андрогенный стероид (ААС) этилэстренол (17α-этилэстр-4-ен-17β-ол). [56] Аллилестренол представляет собой C17α-аллил и C3-декетопроизводное AAS нандролона (19-нортестостерон), а также C17α-аллил и C3-декето- аналог норметандрона AAS (17α-метил-19-нортестостерон) иноретандролон (17α-метил-19-нортестостерон). [56]
Синтез [ править ]
Опубликованы данные о химическом синтезе аллилестренола. [56] [19] [59] [60] [61]
История [ править ]
Аллилестренол был запатентован в 1958 году [19] и продается в медицинских целях с 1961 года. [20] [21] [22] Он был разработан Organon Laboratories . [22] [21]
Общество и культура [ править ]
Общие имена [ править ]
Аллилестренол - это общее название препарата и его INN , BAN и JAN , аллилестренол - его DCF, а аллилестреноло - его DCIT . [56] [25] [62] [24] Первоначально БАН был аллилоэстренолом , но со временем он был изменен. [56] [25] [24] Лекарство также известно под кодовым названием SC-6393 . [56] [25] [24]
Торговые марки [ править ]
Основные торговые марки аллилестренола включают гестанин, гестанон, перселин и туринал. [23] [6] [24] [25] [19] Он также продается под множеством других торговых марок, включая Alese, Alilestrenol, Allynol, Allytry, Alynol, Anin, Arandal, Astanol, Cobarenol, Crestanon, Elmolan. , Fetugard, Foegard, Fulterm, Gestanin, Gestanin, Gestanol, Gestanyn, Gestin, Geston, Gestormone, Gestrenol, Gravida, Gravidin, Gravinol, Gravion, Gravynon, Gynerol, Gynonies, Iugr, Lestron, Loestrol, Meinonies, Iugr, Lestron, Loestrol , Орагестон, Пелиас, Преабор, Прегнолин, Прегтенол, Прегулар, Прелаб, Премастон, Пренолин, Престренол, Профар, Прогестон, Протанон и Шегест. [23] [6] [24] [25] [19]
Доступность [ править ]
Аллилестренол широко продается во всем мире, в том числе в Европе , Южной , Восточной и Юго-Восточной Азии , Африке , Океании и Латинской Америке . [23] [6] [24] [25] Однако, хотя в прошлом он широко продавался, доступность аллилестренола сегодня относительно ограничена. [23] [6] [24] [25] Похоже, он все еще доступен в Бангладеш , Чешской Республике , Египте , Гонконге , Индии., Индонезия , Япония , Литва , Малайзия , Филиппины , Россия , Сингапур и Тайвань . [23] [6] [24] [25] Ранее аллилестренол также был доступен в Австралии , Австрии , Бельгии , Бразилии , Германии , Греции , Венгрии , Италии , Люксембурге , Мексике , Польше , Южной Африке., Испания , Швеция , Швейцария , Турция , Украина , Великобритания и Югославия (ныне Сербия и Черногория ). [23] [6] [24] [25] Однако, похоже, в этих странах он был прекращен. [23] [6] [24] [25] Похоже, он не продавался в США или Канаде . [23] [6] [24] [25]
Ссылки [ править ]
- ^ a b c d e f g h i j k l Bengtsson LP, Tausk M (сентябрь 1972 г.). Фармакология эндокринной системы и родственные препараты: прогестерон, гестагенные препараты и противозачаточные средства . Pergamon Press. С. 235–237.
- ^ Б с д е е г ч я J K L Thijssen JH (1967). Het Metabisme van progestatieve stoffen (Диссертация). Rijksuniversiteit te Utrecht.
- ^ a b c d e f g h i j k l m n o p q r Бергинк EW, Loonen PB, Kloosterboer HJ (август 1985). «Рецепторное связывание аллилестренола, прогестагена из ряда 19-нортестостерона без андрогенных свойств». Журнал стероидной биохимии . 23 (2): 165–8. DOI : 10.1016 / 0022-4731 (85) 90232-8 . PMID 3928974 .
- ↑ a b Saha A, Roy K, Kakali DE (2000). «Влияние аллилестренола на липиды крови в связи с его биологической активностью». Индийский журнал фармацевтических наук . 62 (2): 115.
- ^ a b «SuperCYP» .
- ^ Б с д е е г ч я J к л м н Свитмен, Шон С., под ред. (2009). «Половые гормоны и их модуляторы» . Мартиндейл: Полный справочник лекарств (36-е изд.). Лондон: Фармацевтическая пресса. п. 2082. ISBN 978-0-85369-840-1.
- ^ a b Кортес-Прието Дж, Бош А.О., Роча Дж. А. (1980). «Аллилестренол: трехлетний опыт применения гестанона при угрозе прерывания беременности и преждевременных родах». Клиническая терапия . 3 (3): 200–8. PMID 7459930 .
- ^ а б Хаас, Дэвид М .; Hathaway, Тейлор Дж .; Рэмси, Патрик С. (20 ноября 2019 г.). «Прогестаген для профилактики выкидыша у женщин с повторным невынашиванием неясной этиологии» . Кокрановская база данных систематических обзоров . 2019 (11). DOI : 10.1002 / 14651858.CD003511.pub5 . ISSN 1469-493X . PMC 6953238 . PMID 31745982 .
- ^ a b Канимото Ю., Окада К. (ноябрь 1991 г.). «[Антиандрогенная терапия доброкачественной гиперплазии предстательной железы - обзор препаратов, оценка клинических результатов]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 37 (11): 1423–8. PMID 1722627 .
- ^ а б Умеда К. (ноябрь 1991 г.). «[Клинические результаты и проблемы антиандрогенной терапии доброкачественной гипертрофии простаты]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 37 (11): 1429–33. PMID 1722628 .
- ^ a b Исидзука О, Нисидзава О, Хирао Y, Охшима S (ноябрь 2002 г.). «Доказательный метаанализ фармакотерапии доброкачественной гипертрофии простаты» . Международный журнал урологии . 9 (11): 607–12. DOI : 10.1046 / j.1442-2042.2002.00539.x . PMID 12534901 .
- ^ a b Мюллер (19 июня 1998 г.). Европейский индекс лекарств: Европейские регистрации лекарств, четвертое издание . CRC Press. С. 545–. ISBN 978-3-7692-2114-5.
- ↑ Сет (18 ноября 2009 г.). Учебник фармакологии . Эльзевир Индия. стр. 1–. ISBN 978-81-312-1158-8.
- ^ a b c Борглин, NE (1960). «Клиническая оценка прогестативного эффекта аллилестренола». Европейский журнал эндокринологии . 35 (4 доп.): NP – S15. DOI : 10.1530 / acta.0.XXXVS0NP . ISSN 0804-4643 .
- ^ a b c Филд-Ричардс S, Снайт L (январь 1961 г.). «Аллилестренол: новый пероральный гестаген». Ланцет . 1 (7169): 134–6. DOI : 10.1016 / s0140-6736 (61) 91310-1 . PMID 13699366 .
- ^ a b c d Madjerek, Z .; de Visser, J .; van der Vies, J .; Овербек, Джорджия (1960). "Аллилестренол, беременность, поддерживающая пероральный гестаген". Европейский журнал эндокринологии . XXXV (I): 8–19. DOI : 10.1530 / acta.0.XXXV0008 . ISSN 0804-4643 . PMID 13765069 .
- ^ a b c d McRobb L, Handelsman DJ, Kazlauskas R, Wilkinson S, McLeod MD, Heather AK (май 2008 г.). «Структура-активность отношений синтетических прогестинов в дрожжевом биоанализе андрогенов in vitro». Журнал стероидной биохимии и молекулярной биологии . 110 (1–2): 39–47. DOI : 10.1016 / j.jsbmb.2007.10.008 . PMID 18395441 .
- ^ a b c d e f Ф. Дж. Зелен (1990). Лечебная химия стероидов . Elsevier Science Limited. С. 108–109. ISBN 978-0-444-88727-6.
Другими примерами являются аллилестренол (42), пролекарство, преобразованное в аналог 3-кето (43), который используется при лечении угрозы прерывания беременности [78,79], и альтреногест (44), используемый у свиноматок и кобыл для подавления овуляция и эструс [80]. [...] Прогестины с 17a-аллильной боковой цепью: (42) аллилестренол, (43), (44) альтреногест.
- ^ a b c d e Издательство Уильяма Эндрю (22 октября 2013 г.). Энциклопедия фармацевтического производства, 3-е издание . Эльзевир. С. 170–. ISBN 978-0-8155-1856-3.
- ^ a b Филд-Ричардс S, Снайт L (январь 1961 г.). «Аллилестренол: новый пероральный гестаген». Ланцет . 1 (7169): 134–6. DOI : 10.1016 / S0140-6736 (61) 91310-1 . PMID 13699366 .
- ^ a b c Дж. А. Симпсон; ESC Weiner (1997). Серия дополнений к Оксфордскому словарю английского языка . Кларендон Пресс. С. 36–. ISBN 978-0-19-860027-5.
1961 Lancet 21 января 135/1 Аллилестренол («Гестанин», Органон) ... кажется, полностью лишен андрогенной активности. 1962 Med. Jrnl. Austral. 8 сентября 375/2 Каждая таблетка комбинированного гормонального препарата «Пременквил» содержит 5 мг. аллилоэстренола. [...]
- ^ a b c Medical Proceedings: Южноафриканский журнал по развитию медицинской науки . Джута и компания. 1962.
В Южной Африке только что выпущен новый безопасный гестаген для перорального приема «Органон» - Гестанин.
Гестанин - это аллилестренол, один из новой группы стероидов, синтезированных Органоном.
- ^ a b c d e f g h i j «Продукты Micromedex: пожалуйста, войдите» .
- ^ a b c d e f g h i j k l m «Аллилестренол» .
- ^ a b c d e f g h i j k l m Номинальный индекс 2000: Международный справочник по лекарственным средствам . Тейлор и Фрэнсис. Январь 2000. С. 29–. ISBN 978-3-88763-075-1.
- ^ Биркенфельд А, Навот D, Эзра Y, Рон А, Шенкер Ю.Г. (июль 1987). «Влияние валерата эстрадиола и аллилестренола на трансформацию эндометрия у женщин с гипергонадотропным гипогонадизмом». Европейский журнал акушерства, гинекологии и репродуктивной биологии . 25 (3): 221–9. DOI : 10.1016 / 0028-2243 (87) 90102-X . PMID 3609436 .
- ^ Barták А, Rozprávka М, Blovský J (октябрь 1992 г.). «[Линестренол и аллилестренол в терапии приливов в постменопаузе]». Ceskoslovenska Gynekologie (на чешском языке). 57 (8): 408–13. PMID 1473164 .
- ^ a b Яманака Х, Косаку Н., Макино Т, Шида К. (сентябрь 1983 г.). «[Фундаментальные и клинические исследования антипростатического действия аллилестренола]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 29 (9): 1133–45. PMID 6203385 .
- ^ Таджима А, Асо Y, Усияма Т, Хата М, Камбаяши Т, Оми Й, Масуда Х, Накахара М, Китагава М, Судзуки А (март 1986). «[Клинический эффект аллилестренола на доброкачественную гипертрофию простаты]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 32 (3): 477–85. PMID 2425610 .
- ^ Kohri K, Курите T, Iguchi M, Катаока K (март 1986). «[Клинические эффекты аллилестренола на гипертрофию простаты]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 32 (3): 486–92. PMID 2425611 .
- ^ a b c d Шида К., Коянаги Т., Кавакура К., Нисида Т., Кумамото Ю., Орикаса С., Сато С., Такеда М., Яманака Н., Симадзаки Дж. (апрель 1986 г.). «[Клинические эффекты аллилестренола на доброкачественную гипертрофию простаты двойным слепым методом]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 32 (4): 625–48. PMID 2426932 .
- ^ Б Охиямы M, T, Tanifuji Харагучи C, N, Фуджи Higaki Y, Yoshida H, K Имамура (апрель 1986 г.). «[Клиническое исследование аллилестренола (Org AL-25) на пациентах с гипертрофией предстательной железы - трансректальное ультразвуковое исследование и уродинамическое исследование]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 32 (4): 649–59. PMID 2426933 .
- ^ a b c Катаяма Т., Умеда К., Казама Т. (ноябрь 1986 г.). «[Гормональная среда и антиандрогенное лечение при доброкачественной гипертрофии простаты]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 32 (11): 1584–9. PMID 2435122 .
- ^ Б с д е е Кумамото Y, Y, Yamaguchi Sato Y, R, Suzuki Танда H, Като S, Мори K, Мацумото H, A Maki, Кадоно M (февраль 1990 г.). «[Влияние антиандрогенов на половую функцию. Двойные слепые сравнительные исследования аллилестренола и хлормадинона ацетата, часть I: мониторинг ночного набухания полового члена]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 36 (2): 213–26. PMID 1693037 .
- ^ a b c Кумамото Y, Ямагути Y, Сато Y, Судзуки Р., Танда Х, Като С., Мори К., Мацумото Х, Маки А, Кадоно М. (февраль 1990 г.). «[Влияние антиандрогенов на сексуальную функцию. Двойные слепые сравнительные исследования аллилестренола и хлормадинона ацетата. Часть II: Метод анкеты самооценки]» (PDF) . Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 36 (2): 227–44. PMID 1693038 .
- ^ Тсуджа У, Ariyoshi А, Накамур Н, Michinaga S, Томит Y, Ohmori А, Тахар Н, Ямашит Y, Фудзисав Y, Kajiwara я (август 1992 г.). «[Антиандрогенная терапия доброкачественной гипертрофии простаты: клинические эффекты аллилестренола оцениваются с помощью трансректального ультразвукового измерения]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 38 (8): 961–6. PMID 1384295 .
- ^ а б Фукуока Х., Ишибаши Й., Шиба Т., Тучия Ф., Саканиши С. (июль 1993 г.). «[Клиническое исследование аллилестренола (перселина) на пациентах с гипертрофией простаты]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 39 (7): 679–83. PMID 7689782 .
- ^ a b Игучи Х., Икеучи Т, Кай Й, Йошида Х (март 1994). «[Влияние антиандрогенной терапии гипертрофии простаты на липидный обмен]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 40 (3): 215–9. PMID 7513937 .
- ^ a b c Хорита Х, Кумамото Й, Сато Й, Судзуки Н., Вада Х, Сибуя А, Адачи Х, Курохата Т, Цукамото Т (май 1995 г.). «[Профилактическое действие инделоксазина гидрохлорида на сексуальную дисфункцию, вызванную антиандрогенергическим агентом (аллилестренолом)]». Nihon Hinyokika Gakkai Zasshi. Японский журнал урологии (на японском языке). 86 (5): 1044–50. DOI : 10,5980 / jpnjurol1989.86.1044 . PMID 7541089 .
- ↑ a b Ногучи К., Харада М., Масуда М., Такеда М., Киношита Ю., Фукусима С., Мияй К., Фукуока Н., Хосака М. (сентябрь 1998 г.). «Клиническое значение прерывания терапии аллилестренолом у пациентов с доброкачественной гипертрофией простаты» . Международный журнал урологии . 5 (5): 466–70. DOI : 10.1111 / j.1442-2042.1998.tb00389.x . PMID 9781436 .
- Перейти ↑ Noguchi K, Uemura H, Takeda M, Sekiguchi Y, Ogawa K, Hosaka M (сентябрь 2000 г.). «[Отскок специфического антигена простаты после прекращения антиандрогенной терапии доброкачественной гиперплазии предстательной железы]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 46 (9): 605–7. PMID 11107528 .
- Перейти ↑ Noguchi K, Takeda M, Hosaka M, Kubota Y (май 2002 г.). «[Клинические эффекты аллилестренола у пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ) оцениваются с помощью критериев эффективности лечения ДГПЖ]». Hinyokika Kiyo. Acta Urologica Japonica (на японском языке). 48 (5): 269–73. PMID 12094708 .
- ^ а б Ногучи К., Судзуки К., Тераниши Дж., Кондо К., Кишида Т., Сайто К., Уэмура Х., Кубота Y (июль 2006 г.). «Восстановление значения специфического антигена простаты в сыворотке крови после прекращения антиандрогенной терапии аллилестренолом при доброкачественной гиперплазии простаты». Hinyokika Kiyo. Acta Urologica Japonica . 52 (7): 527–30. PMID 16910584 .
- Перейти ↑ Takeuchi H (1981). «Терапевтический эффект одновременного приема 5-фторурацила и аллилестренола или гексэстрола в малых дозах на карциному простаты». Простата. Дополнение . 1 : 111–7. DOI : 10.1002 / pros.2990020518 . PMID 6281750 .
- Перейти ↑ Riquelme Moreno E, Montiel López P, Bravo Guerra R, Escobar Cauz G (июль 1972 г.). «[Контроль 5 случаев идиопатического преждевременного полового созревания с помощью аллилестренола]». Ginecologia y Obstetricia de Mexico (на испанском языке). 32 (189): 99–108. PMID 5057420 .
- ^ a b К.Д. Трипати (30 сентября 2013 г.). Основы медицинской фармакологии . JP Medical Ltd. стр. 318–. ISBN 978-93-5025-937-5.
- ^ a b Р. С. Сатоскар; С.Д. Бхандаркар и Нирмала Н. Реге (1973). Фармакология и фармакотерапия . Популярный Пракашан. стр. 941–. ISBN 978-81-7991-527-1.
- ^ Розенбаум H (март 1982 г.). «Взаимосвязь между химической структурой и биологическими свойствами прогестагенов». Американский журнал акушерства и гинекологии . 142 (6 Pt 2): 719–24. DOI : 10.1016 / S0002-9378 (16) 32477-2 . PMID 7065053 .
- ^ Б Endrikat, J Gerlinger C, Ричард S, P, Розенбаума Düsterberg B (декабрь 2011). «Дозы подавления овуляции прогестинов: систематический обзор доступной литературы и препаратов, продаваемых во всем мире». Контрацепция . 84 (6): 549–57. DOI : 10.1016 / j.contraception.2011.04.009 . PMID 22078182 .
- ↑ Грегори Пинкус (3 сентября 2013 г.). Контроль рождаемости . Эльзевир. С. 222–. ISBN 978-1-4832-7088-3.
- ^ Фреймут А. Лейденбергер; Томас Стровицки; Олаф Ортманн (29 августа 2009 г.). Klinische Endokrinologie für Frauenärzte . Springer-Verlag. С. 225–. ISBN 978-3-540-89760-6.
- ^ a b c d e f g h Ясуда Н., Фуджино К., Шираджи Т., Намбу Ф., Кондо К. (июль 1997 г.). «Влияние стероидного ингибитора 5альфа-редуктазы ONO-9302 и антиандрогенного аллилестренола на рост предстательной железы, а также уровни гормона в плазме и простате у крыс» . Японский журнал фармакологии . 74 (3): 243–52. DOI : 10.1254 / jjp.74.243 . PMID 9268084 .
- ^ Jacobi GH, Altwein JE, Kurth KH, Basting R, Hohenfellner R (июнь 1980). «Лечение распространенного рака предстательной железы парентеральным ципротерона ацетатом: рандомизированное исследование III фазы». Британский журнал урологии . 52 (3): 208–15. DOI : 10.1111 / j.1464-410X.1980.tb02961.x . PMID 7000222 .
- ^ Кнут UA, Hano R, Nieschlag Е (ноябрь 1984). «Влияние флутамида или ципротерона ацетата на гормоны гипофиза и яичек у нормальных мужчин». Журнал клинической эндокринологии и метаболизма . 59 (5): 963–9. DOI : 10,1210 / jcem-59-5-963 . PMID 6237116 .
- ^ Sander S, Ниссен-Мейер R, Aakvaag А (1978). «О гестагеновом лечении запущенной карциномы простаты». Скандинавский журнал урологии и нефрологии . 12 (2): 119–21. DOI : 10.3109 / 00365597809179977 . PMID 694436 .
- ^ a b c d e f g h Дж. Элкс (14 ноября 2014 г.). Словарь лекарств: химические данные: химические данные, структуры и библиографии . Springer. С. 31–. ISBN 978-1-4757-2085-3.
- ^ Анита М.В.; Сандхья Джайн; Neerja Goel (31 декабря 2017 г.). Использование прогестагенов в клинической практике акушерства и гинекологии . JP Medical Ltd. стр. 10–. ISBN 978-93-5270-218-3.
- ^ a b c Джеффри К. Аронсон (21 февраля 2009 г.). Побочные эффекты Мейлера эндокринных и метаболических препаратов . Эльзевир. С. 289–. ISBN 978-0-08-093292-7.
- ^ Gunnet JW, Dixon LA (2000). «Гормоны, половые гормоны». Энциклопедия химической технологии Кирка-Отмера . DOI : 10.1002 / 0471238961.19052407211414.a01 . ISBN 978-0471238966.
- ^ Die Gestagene . Springer-Verlag. 27 ноября 2013. с. 16. ISBN 978-3-642-99941-3.
- ^ Винтер MS, Siegman CM, Szpilfogel SA (1959). «17-алкилированный-3-дезоксо-19-нор-тестостерон». Chem. Инд . : 905.
- ↑ Morton IK, Hall JM (6 декабря 2012 г.). Краткий словарь фармакологических агентов: свойства и синонимы . Springer Science & Business Media. С. 11–. ISBN 978-94-011-4439-1.