 | |
 | |
| Идентификаторы | |
|---|---|
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.037.264 |
| Номер ЕС |
|
PubChem CID | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| H 8 N 2 Cl 6 Ir | |
| Молярная масса | 441,01 |
| Внешность | коричневые кристаллы |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
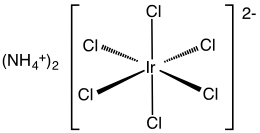
Гексахлориридат аммония (IV) представляет собой неорганическое соединение с формулой (NH 4 ) 2 [IrCl 6 ]. Это темно-коричневое твердое вещество является аммониевой солью комплекса иридия (IV) [IrCl 6 ] 2– . Это коммерчески важное соединение иридия [1], один из наиболее распространенных комплексов иридия (IV). Родственное, но плохо определенное соединение - тетрахлорид иридия , который часто используется как взаимозаменяемый. [2]
Структура [ править ]
Соединение охарактеризовано методом рентгеновской кристаллографии . Соль кристаллизуется в кубическом мотиве, подобном гексахлороплатинату аммония . Центры [IrCl 6 ] 2– имеют октаэдрическую молекулярную геометрию . [3]
Использует [ редактировать ]
Это ключевой промежуточный продукт при выделении иридия из руд. Большинство других металлов образуют нерастворимые сульфиды, когда водные растворы их хлоридов обрабатывают сероводородом , но [IrCl 6 ] 2- сопротивляется замещению лиганда. При нагревании в водороде твердая соль превращается в металл: [1]
- (NH 4 ) 2 [IrCl 6 ] + 2 H 2 → Ir + 6 HCl + 2 NH 3
Связь [ править ]
Электронная структура гексахлориридата (IV) аммония привлекла большое внимание. Его магнитный момент меньше расчетного для одного электрона. Этот результат интерпретируется как результат антиферромагнитного взаимодействия между центрами Ir, опосредованного взаимодействиями Cl --- Cl. Электронный спиновой резонанс , исследования показывают, что более половины спиновой плотности приходится на хлорид, поэтому описание комплекса как Ir (IV) является чрезмерным упрощением. [4]
Ссылки [ править ]
- ^ a b Renner, H .; Schlamp, G .; Kleinwächter, I .; Drost, E .; Lüschow, HM; Tews, P .; Panster, P .; Diehl, M .; и другие. (2002). «Металлы и соединения платиновой группы». Энциклопедия промышленной химии Ульмана . Вайли. DOI : 10.1002 / 14356007.a21_075 .
- ^ Томас РБ Митчелл (2001). «Хлорид иридия (IV)». e-EROS Энциклопедия реагентов для органического синтеза . DOI : 10.1002 / 047084289X.ri050 .
- ^ Бокий, ГБ; Усиков П.И. "Рентгенография структуры иридатов аммония-хлора (NH 4 ) 2 IrCl 6" Докл. Академии Наук СССР, 1940, т. 26, с. 782-с. 784.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 1121. ISBN 978-0-08-037941-8.