| Имена | |||
|---|---|---|---|
| Название ИЮПАК арсорат | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
PubChem CID | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
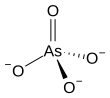
| AsO3- 4 | |||
| Молярная масса | 138,919 | ||
| Конъюгированная кислота | Мышьяковая кислота | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Арсенат ионов является , как O3-
4. Арсенат (соединение) любое соединение , которое содержит этот ион. Арсенаты являются соли или сложные эфиры из мышьяком кислоты . Атом мышьяка в арсенате имеет валентность 5 и также известен как пятивалентный мышьяк или As (V) . Арсенат во многом похож на фосфат , поскольку мышьяк и фосфор входят в одну группу (столбец) периодической таблицы . Арсенаты являются умеренными окислителями с электродным потенциалом +0,56 В для восстановления до арсенитов .
Возникновение [ править ]
Арсенаты в природе содержатся в различных минералах . Эти минералы могут содержать гидратированные или безводные арсенаты. В отличие от фосфатов, арсенаты не теряются из минерала при выветривании . Примеры минералов, содержащих арсенат, включают адамит , аларсит , аннабергит , эритрит и леграндит . [1] , где два иона арсената необходимы , чтобы сбалансировать заряд в формуле, его называют diarsenate например trizinc diarsenate, Zn 3 (ASO 4 ) 2 .
Ионы [ править ]
Слово арсенат происходит от мышьяковой кислоты H 3 AsO 4 . Эта умеренно сильная кислота превращается в дигидрогенарсенат ( H
2AsO-
4), арсенат водорода ( HAsO2-
4) и арсенат ( AsO3-
4) в зависимости от pH. Количественное соотношение между этими видами определяется константами кислотной диссоциации:
- H 3 AsO 4 + H 2 O ⇌ H 2 AsO-
4 + H 3 O + ( K 1 = 10 -2,19 ) - H 2 AsO-
4 + H 2 O ⇌ HAsO2-
4 + H 3 O + ( K 2 = 10 −6,94 ) - HAsO2-
4 + H 2 O ⇌ AsO3-
4 + H 3 O + ( K 3 = 10 −11,5 )
Эти значения аналогичны значениям для гидрофосфатов. В водном растворе, близком к нейтральному, преобладают арсенат водорода и дигидроарсенат.
Отравление арсенатом [ править ]
Арсенат может заменять неорганический фосфат на стадии гликолиза, при котором образуется 1,3-бисфосфоглицерат из глицеральдегид-3-фосфата . Вместо этого получается 1-арсено-3-фосфоглицерат , который нестабилен и быстро гидролизуется, образуя следующий промежуточный продукт на этом пути, 3-фосфоглицерат . Следовательно, гликолиз продолжается, но молекула АТФ , которая могла бы образоваться из 1,3-бисфосфоглицерата , теряется - арсенат является разобщителем гликолиза, что объясняет его токсичность. [2]
Как и с другими соединениями мышьяка, Арсенит связывается с липоевой кислотой , [3] ингибировать превращение пирувата в ацетил-КоА , блокирующий цикл Кребса и , следовательно , приводит к дальнейшему потере АТФ. [4]
См. Также [ править ]
- Категория: Арсенаты
Ссылки [ править ]
- ^ Mineralienatlas - Фосфат Mineralklasse, Арсенат, Ванадат . (на немецком)
- ^ Хьюз, Майкл Ф. (2002). «Токсичность мышьяка и потенциальные механизмы действия» (PDF) . Письма токсикологии (133): 4.[ постоянная мертвая ссылка ]
- ^ "Архивная копия" . Архивировано из оригинала 20 марта 2018 года . Проверено 4 февраля 2018 года .CS1 maint: заархивированная копия как заголовок ( ссылка )
- ^ Ким Геле; Селена Чоу; Уильям С. Беккет (1 октября 2009 г.), Тематическое исследование токсичности мышьяка , Агентство по токсическим веществам и реестру заболеваний