| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Бицикло [2.2.2] окта-2,5,7-триен [1] | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 8 Н 8 | |||
| Молярная масса | 104,15 | ||
| Плотность | 1,013 г / мл | ||
| Точка кипения | 153,7 ° С (308,7 ° F, 426,8 К) | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Баррелен представляет собой бициклическое органическое соединение с химической формулой C 8 H 8 и систематическим названием бицикло [2.2.2] окта-2,5,7-триен. Впервые синтезированный и описанный Говардом Циммерманом в 1960 году, название происходит от сходства с бочкой , в которой стержни представляют собой три этиленовых единицы, присоединенные к двум метиновым группам. Это формальный аддукт Дильса – Альдера бензола и ацетилена . Из-за необычной молекулярной геометрии это соединение представляет значительный интерес для химиков-теоретиков.
Иптицены с алкеновыми группами аренов являются родственными соединениями. Он также является исходным материалом для многих других органических соединений, таких как полубулвален .
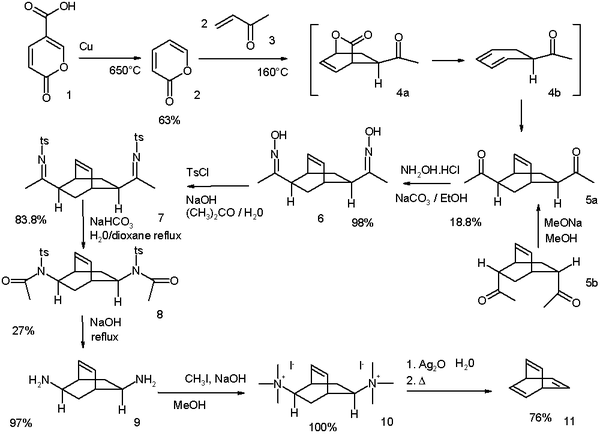
Оригинальный Циммерман, модифицированный в 1969 г. [2], начинается с кумаловой кислоты : [3]
С тех пор было разработано много альтернативных маршрутов, один из которых начинается с оксепина : [4] [5]
Также сообщалось об альтернативном пути, который позволяет синтезировать исходную систему баррелена и различные замещенные баррелены [6].
Реакции Баррелена [ править ]
Баррелен гидрируют газообразным водородом и катализатором Адамса в этаноле до полностью насыщенного бицикло [2.2.2] -октана . Бромирование с бромом в тетрахлорметане дает ди-бром - аддукт , потому что реакция сочетания вмешивается:
Эпоксидирование из barrelene с оксон дает trioxatrishomobarrelene [7] , который по перегруппировке с трифторидом бора (движущая сила: рельеф энергии деформации ) переходит в trioxatrishomocubane: [8]
Это соединение можно представить как кубан с тремя атомами кислорода, вставленными в три противоположных края, или как 9-краун-3, закрытый двумя метиновыми звеньями. Молекула является хиральной, и отдельные энантиомеры изолированы.
Некоторые баррелены были использованы в качестве мономера в метатезисной полимеризации с раскрытием цикла : [9] [10]
Катализатор представляет собой карбен Фишера ( молибденовый бис- (гексафтор-трет-бутокси) карбеновый катализатор ), и длинная алкильная цепь, присоединенная к мономеру, необходима для растворимости. Окисление полимера DDQ дает нафталиновую ветвь поли (п-фениленвинилена) .
Изопентановые растворы баррелена подвергаются фотолитической изомеризации, когда ацетон добавляют в качестве фотосенсибилизатора для получения полубулвалена . Продолжительное облучение приводит к дальнейшей изомеризации с образованием циклооктатетраена . [11]
Ссылки [ править ]
- ^ Международный союз чистой и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 1257. DOI : 10.1039 / 9781849733069 . ISBN 978-0-85404-182-4.
- ^ Синтез и физические свойства баррелена, уникальной молекулы типа Мебиуса. Говард Э. Циммерман, Гэри Л. Грюневальд, Роберт М. Пауфлер, Мейнард А. Шервин J. Am. Chem. Soc. ; 1969 ; 91 (9); 2330–2338. DOI : 10.1021 / ja01037a024
- ^ Схема реакции: декарбоксилирование из coumalic кислоты (1) происходит при температуре 650 ° C с медью с получением & alpha ; -пирона (2). Реакция с метилвинилкетоном (3) представляет собой тандем Дильса-Альдера / Дильса-Альдера последовательность / ретро Дильса-Альдера, что дает ди- кетона 5 в виде смеси двух изомеров . Можно превратить эндо-изомер 5b в экзо-изомер 5a путемпроцесса эпимеризации через енол . Кетоновые группы превращаются в оксимные группы в 6 реакцией с гидроксиламином, а затем втозилатные группы в 7 реакцией с тозилхлоридом . Основной Бекман перегруппировка принимает схему , чтобы дать амиду 8 и его гидролиз до ди- амина 9 происходит с гидроксидом натрия . Наконец, отщепление Хофмана через соль аммония 10 дает баррелен 11.
- ^ Barrelene, новый удобный синтез Серджио Коссу, Симоне Баттаджиа и Отторино Де Лучки J. Org. Chem. ; 1997 ; 62 (12) pp 4162–4163; DOI : 10.1021 / jo962267f
- ^ Шаг первый в этой реакции между оксепином (одним из возможных таутомеров ) с ( Z ) -1,2-бис (фенилсульфонил) этиленом является реакция Дильса-Альдера . Реагентами для деэпоксидирования являются гексахлорид вольфрама и бутиллитий . Вторая реакция элиминирования происходит с амальгамой натрия встиле олефинирования Джулии .
- ^ Синтез замещенных бицикло [2.2.2] октатриенов Майкл В. Вагаман, Эрика Беллманн, Мишель Кукулу и Роберт Х. Граббс J. Org. Chem. ; 1997 ; 62 (26) pp 9076–9082; DOI : 10.1021 / jo971039y
- ^ эндо, экзо, син-3,7,10-Триоксапентацикло [3.3.3.0 2,4 .0 6,8 .0 9,11 ] ундекан
- ^ 4,7,11-Triheterotrishomocubanes - Высоко симметричные киральные молекулы пропеллерной формы, полученные из Barrelene Sergei I. Kozhushkov et al. Европейский журнал органической химии, том 2006 , выпуск 11, страницы 2590 - 2600 Аннотация
- ^ Синтез поли (1,4-нафтиленвиниленов): метатезис-полимеризация бензобарреленов Lin Pu, Майкла В. Вагамана и макромолекул Роберта Х. Граббса ; 1996 ; 29 (4), стр. 1138–1143; (Статья) doi : 10.1021 / ma9500143
- ^ Синтез органических и водорастворимых поли (1,4-фениленвиниленов), содержащих карбоксильные группы: метатезисная полимеризация с раскрытием живого цикла (ROMP) 2,3-дикарбоксибарреленов Майкл В. Вагаман и макромолекулы Роберта Х. Граббса ; 1997 ; 30 (14) pp 3978–3985; (Статья) doi : 10.1021 / ma9701595
- ^ Циммерман, HE; Грюневальд, GL (1966). «Химия баррелена. III. Уникальная фотоизомеризация в семибулвален». Варенье. Chem. Soc. 88 (1): 183–184. DOI : 10.1021 / ja00953a045 .