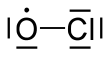Эта статья включает в себя список общих ссылок , но он остается в значительной степени непроверенным, поскольку в нем отсутствует достаточное количество соответствующих встроенных ссылок . ( Апрель 2020 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Окись хлора | |||
| Систематическое название ИЮПАК Хлороксиданил | |||
| Другие имена Оксид хлора (II) | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| Сокращения | ClO (.) | ||
| ЧЭБИ | |||
| ChemSpider | |||
| MeSH | Хлорсил | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| Cl O | |||
| Молярная масса | 51,45 г · моль -1 | ||
| Термохимия | |||
Std энтальпия формации (Δ F H ⦵ 298 ) | 101,8 кДж / моль [1] | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Окись хлора - это химический радикал с химической формулой . Он играет важную роль в процессе разрушения озонового слоя . В стратосфере , хлор атомы вступают в реакцию с озоном молекулами с образованием моноксида хлора и кислорода .
Эта реакция вызывает истощение озонового слоя. [1] В результате радикалы могут далее реагировать как таковые:
регенерация радикала хлора. Таким образом, вся реакция разложения озона катализируется хлором, так как в конечном итоге хлор остается неизменным. Общая реакция такова:
Это оказало значительное влияние на использование ХФУ в верхних слоях стратосферы, однако многие страны согласились запретить использование ХФУ. Нереактивная природа CFC позволяет им переходить в стратосферу, где они подвергаются фотодиссоциации с образованием радикалов Cl. Затем они легко образуют монооксид хлора, и этот цикл может продолжаться до тех пор, пока два радикала не прореагируют с образованием монооксида дихлора , завершая радикальную реакцию. Поскольку концентрация CFC в атмосфере очень мала, вероятность прекращения реакции чрезвычайно мала, а это означает, что каждый радикал может разлагать многие тысячи молекул озона.
Несмотря на то, что использование ХФУ было запрещено во многих странах, ХФУ могут оставаться в атмосфере около 50-500 лет. Это вызывает образование многих радикалов хлора и, следовательно, значительное количество молекул озона разлагается до того, как радикалы хлора смогут реагировать с монооксидом хлора с образованием моноксида дихлора .
Ссылки [ править ]
- ^ а б Эгон Виберг; Нильс Виберг; Арнольд Фредерик Холлеман (2001). Неорганическая химия . Академическая пресса. п. 462. ISBN. 0-12-352651-5.