| |||
| Имена | |||
|---|---|---|---|
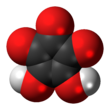
| Предпочтительное название IUPAC 4,5-дигидроксициклопент-4-ен-1,2,3-трион | |||
| Другие названия Крокиновая кислота | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.201.686 | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 5 Н 2 О 5 | |||
| Молярная масса | 142,07 | ||
| Температура плавления | > 300 ° C (572 ° F, 573 K) (разлагается) | ||
| Кислотность (p K a ) | 0,80, 2,24 | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Кроконовая кислота или 4,5-дигидроксициклопентенетрион представляет собой химическое соединение с формулой C
5ЧАС
2О
5или (C = O)
3(COH)
2. Он имеет циклопентеновую основную цепь с двумя гидроксильными группами, смежными с двойной связью, и тремя кетонными группами на оставшихся атомах углерода . Он чувствителен к свету [1], растворим в воде и этаноле [2] и образует желтые кристаллы, которые разлагаются при 212 ° C. [3]
Соединение является кислым и теряет протоны из гидроксильных групп (р К а1 =0,80 ± 0,08 и p K a2 =2,24 ± 0,01 при 25 ° С). [4] [5] Полученные анионы , гидрокроконат C
5HO-
5[1] и кроконат C
5О2-
5также довольно стабильны. В частности, кроконат-ион является ароматическим [6] и симметричным, так как двойная связь и отрицательные заряды становятся делокализованными по пяти единицам CO (с двумя электронами, правило Хюккеля означает, что это ароматическая конфигурация). В литиевых , натриевых и калиевых croconates кристаллизуются из воды , как дигидраты [7] , но оранжевая соль калия может быть обезвожена с образованием моногидрата . [1] [4] Кроконаты аммония , рубидия и цезия кристаллизуются в безводной форме. [7]Известны также соли бария , свинца , серебра и др. [ Указать ] . [1]
Croconic кислота также образует простые эфиры , такие как диметиловый croconate , где атом водорода гидроксильной группы , замещенной с помощью алкильной группы.
История [ править ]
Кроконовая кислота и дигидрат кроконата калия были открыты Леопольдом Гмелином в 1825 году, который назвал эти соединения от греческого κρόκος, что означает « крокус » или «яичный желток». [7] Структура кроконата аммония была определена Baenziger et al. в 1964 г. Структура K
2C
5О
5· 2H 2 O был определен Дуницем в 2001 году. [8]
Структура [ править ]
В твердом состоянии кроконовая кислота имеет своеобразную структуру, состоящую из гофрированных полосок, каждая «страница» которой представляет собой плоское кольцо из 4 молекул C
5О
5ЧАС
2удерживаются вместе водородными связями . [7] В диоксане он имеет большой дипольный момент 9–10 D , в то время как свободная молекула имеет диполь 7–7,5 D. [9] Твердое тело является сегнетоэлектрическим с точкой Кюри выше 400 K (127 ° C), действительно, органический кристалл с самой высокой спонтанной поляризацией (около 20 мкКл / см 2 ). Это связано с переносом протонов между соседними молекулами в каждом гофрированном листе, а не с вращением молекул. [9]
В твердых солях щелочных металлов кроконат-анионы и щелочные катионы образуют параллельные столбцы. [7] В смешанной соли K
3(HC
5О
5) (C
5О
5) · 2H 2 O , который формально содержит оба дианиона кроконата C
5О2-
5и один моноанион гидрокроконата ( HC
5О-
5), водород делится поровну двумя соседними кроконатными звеньями. [7]
Соли кроконат-аниона и его производных представляют интерес для исследований в области супрамолекулярной химии из-за их потенциала для эффектов π-стэкинга , когда взаимодействуют делокализованные электроны двух сложенных друг с другом кроконат-анионов. [10]
Инфракрасное и рамановское отнесения указывают на то, что выравнивание длин углерод-углеродных связей и, таким образом, электронная делокализация следует за увеличением размера противоионов для солей. [6] Этот результат приводит к дополнительной интерпретации, согласно которой степень ароматичности солей увеличивается в зависимости от размера противоиона. В том же исследовании представлены квантово-механические DFT- расчеты оптимизированных структур и колебательных спектров, которые согласуются с экспериментальными данными. Значения рассчитанных теоретических индексов ароматичности также увеличивались с увеличением размера противоиона.
В croconate образует анион гидратированные кристаллические координационные соединения с двухвалентных катионов из переходных металлов , с общей формулой M (С
5О
5) · 3Н 2 О ; где M обозначает медь (с образованием коричневого твердого вещества), железо (темно-фиолетовый), цинк (желтый), никель (зеленый), марганец (темно-зеленый) или кобальт (фиолетовый). Все эти комплексы имеют одинаковую орторомбическую кристаллическую структуру, состоящую из чередующихся цепочек ионов кроконата и металла. Каждый кроконат связан с предыдущим металлом одним атомом кислорода и со следующим металлом через два противоположных атома кислорода, оставляя два атома кислорода несвязанными. Каждый металл связан с тремя атомами кислорода кроконата и одной молекулой воды. [11] Кальцийтакже образует соединение с той же формулой (желтый), но имеет другую структуру. [11]
Кроконат-анион также образует соединения с трехвалентными катионами, такими как алюминий (желтый), хром (коричневый) и железо (пурпурный). Эти соединения также включают гидроксильные группы, а также гидратную воду и имеют более сложную кристаллическую структуру. [11] Не было обнаружено никаких признаков сэндвич-связей между делокализованными электронами и металлом (как это видно , например, в ферроцене ), [11] но анион может образовывать комплексы металлов с большим разнообразием схем связывания, включая от одного до всех пяти его атомов кислорода. [12] [13] [14]
См. Также [ править ]
- Кроконат фиолетовый
- Кроконат синий
- Родизоновая кислота
- Квадратная кислота
- Дельтовая кислота
- Циклопентанепентон (лейконовая кислота)
Ссылки [ править ]
- ^ a b c d Ямада, К .; Mizuno, N .; Хирата, Ю. (1958). «Состав кроконовой кислоты» . Бюллетень химического общества Японии . 31 (5): 543–549. DOI : 10.1246 / bcsj.31.543 .
- Перейти ↑ Miller, WA (1868). Элементы химии: теоретические и практические (4-е изд.). Лонгманс.[ требуется страница ]
- ^ Тернер, Э. Элементы химии . [ требуется страница ]
- ^ a b Schwartz, LM; Gelb, RI; Ярдли, Дж. О. (1975). «Водная диссоциация кроконовой кислоты». Журнал физической химии . 79 (21): 2246–2251. DOI : 10.1021 / j100588a009 .
- ^ Гелб, Род-Айленд; Шварц, Л. М.; Laufer, DA; Ярдли, Дж. О. (1977). «Строение водной кроконовой кислоты». Журнал физической химии . 81 (13): 1268–1274. DOI : 10.1021 / j100528a010 .
- ^ а б Георгопулос, SL; Diniz, R .; Йошида, штат Мичиган; Speziali, NL; Душ Сантуш, HF; Жункейра, GMA; де Оливейра, LFC (2006). "Колебательная спектроскопия и исследование ароматичности скваратных солей: теоретический и экспериментальный подход". Журнал молекулярной структуры . 794 (1–3): 63–70. Bibcode : 2006JMoSt.794 ... 63G . DOI : 10.1016 / j.molstruc.2006.01.035 .
- ^ a b c d e е Брага, Д .; Maini, L .; Грепиони, Ф. (2002). «Кроконовая кислота и кроконатные соли щелочных металлов: новые взгляды на старую историю». Химия - европейский журнал . 8 (8): 1804–1812. DOI : 10.1002 / 1521-3765 (20020415) 8: 8 <1804 :: АИД-CHEM1804> 3.0.CO; 2-С .
- ^ Дуниц, JD; Зайлер, П .; Czechtizky, W. (2001). «Кристаллическая структура дигидрата кроконата калия через 175 лет». Angewandte Chemie International Edition . 40 (9): 1779–1780. DOI : 10.1002 / 1521-3773 (20010504) 40: 9 <1779 :: АИД-ANIE17790> 3.0.CO; 2-6 . PMID 11353510 .
- ^ a b Horiuchi, S .; Tokunaga, Y .; Giovannetti, G .; Picozzi, S .; Itoh, H .; Shimano, R .; Kumai, R .; Токура, Ю. (2010). «Сегнетоэлектричество выше комнатной температуры в однокомпонентном молекулярном кристалле». Природа . 463 (7282): 789–92. Bibcode : 2010Natur.463..789H . DOI : 10,1038 / природа08731 . PMID 20148035 .
- ^ Фариа, LFO; Соареш, А.Л., младший; Diniz, R .; Йошида, штат Мичиган; Эдвардс, HGM; де Оливейра, LFC (2010). «Смешанные соли, содержащие кроконат фиолетовый, лантаноид и ионы калия: кристаллические структуры и спектроскопические характеристики супрамолекулярных соединений». Inorganica Chimica Acta . 363 (1): 49–56. DOI : 10.1016 / j.ica.2009.09.050 .
- ^ a b c d West, R .; Ниу, Хай (1963). «Новые ароматические анионы. VI. Комплексы кроконат-иона с некоторыми двухвалентными и трехвалентными металлами (Комплексы кроконатов двухвалентных переходных металлов и кроконатов трехвалентных металлов)». Журнал Американского химического общества . 85 (17): 2586. DOI : 10.1021 / ja00900a013 .
- ^ Карранса, Дж .; Sletten, J .; Lloret, F .; Юльве, М. (2009). «Комплексы марганца (II) с кроконатными и 2- (2-пиридил) имидазольными лигандами: синтезы, рентгеновские структуры и магнитные свойства». Inorganica Chimica Acta . 362 (8): 2636–2642. DOI : 10.1016 / j.ica.2008.12.002 .
- ^ Wang, C.-C .; Ke, M.-J .; Tsai, C.-H .; Chen, I.-H .; Lin, S.-I .; Lin, T.-Y .; Wu, L.-M .; Lee, G.-H .; Sheu, H.-S .; Федоров, В.Е. (2009). " [M (C
5О
5)
2(ЧАС
2O)
п] 2- как строительный блок для гетеро- и гомобиметаллических координационных полимеров: от одномерных цепей до трехмерных супрамолекулярных архитектур ». Выращивание кристаллов и дизайн . 9 (2): 1013–1019. Doi : 10.1021 / cg800827a . - ^ М., СК; Гош, AK; Zangrando, E .; Чаудхури, Н. Р. (2007). «Трехмерные супрамолекулярные сети Co (II) / Fe (II) с использованием дианиона кроконата и бипиридильного спейсера: синтез, кристаллическая структура и термическое исследование». Многогранник . 26 (5): 1105–1112. DOI : 10.1016 / j.poly.2006.09.100 .
Внешние ссылки [ править ]
- СМИ, связанные с кроконовой кислотой на Викискладе?