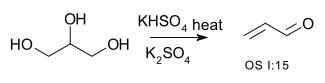
В химии , А реакция дегидратации (иначе реакция конденсации [1] ) является преобразованием , который включает в себя потерю воды из реагирующей молекулы или иона. Реакции дегидратации - обычные процессы, обратные реакции гидратации . Обычные дегидратирующие агенты, используемые в органическом синтезе, включают серную кислоту и оксид алюминия . Часто реакции дегидратации осуществляются при нагревании.
Реакции обезвоживания [ править ]
Классическим примером реакции дегидратации является этерификация Фишера , которая включает обработку карбоновой кислоты спиртом в присутствии дегидратирующего агента:
- RCO 2 H + R'OH ⇌ RCO 2 R '+ H 2 O
Два моносахарида , такие как глюкоза и фруктоза , могут быть соединены вместе (с образованием сахарозы ) с помощью дегидратационного синтеза. Новая молекула, состоящая из двух моносахаридов, называется дисахаридом .
Процесс гидролиза - это обратная реакция, что означает, что вода рекомбинирует с двумя гидроксильными группами, и дисахарид превращается в моносахариды.
В соответствующей реакции конденсации вода выделяется из двух разных реагентов.
В органическом синтезе есть много примеров реакций дегидратации, например дегидратации спиртов или сахаров.
| Реакция | Общее уравнение | Примеры |
|---|---|---|
| Превращение двух спиртов в простой эфир ( замещение ) | 2 R – OH → R – O – R + H 2 O | |
| Превращение кислоты и спирта в сложный эфир ( этерификация Фишера-Шпейера ) | R-COOH + R'-OH → R-COO-R '+ H 2 O | |
| Превращение спирта в алкен ( отщепление ) | R – CH 2– CHOH – R → R – CH = CH – R + H 2 O | например, преобразование глицерина в акролеин : [2] или обезвоживание 2-метил-циклогексан-1-ола , чтобы ( в основном) 1-метилциклогексен , [3] с помощью sulfurane Мартина [4] Превращение этанола в этен [5]
|
| Превращение двух карбоновых кислот в ацильный ангидрид | 2 RCOOH → (RCO) 2 O + Н 2 О | |
| Превращение амида в нитрил | RCONH 2 → R – CN + H 2 O | |
| Диенол-бензольная перегруппировка | 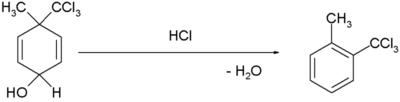 [6] [7] [6] [7] |
Другими примерами реакций синтеза дегидратации являются образование триглицеридов из жирных кислот и образование гликозидных связей между молекулами сахаридов, например образование мальтозы из двух молекул глюкозы.
См. Также [ править ]
Ссылки [ править ]
- ^ oktatási hivatal, OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM (2008). BIOLÓGIA ANGOL NYELVEN EMELT SZINTŰ ÍRÁSBELI VIZSGA 2008. május 16. 8:00 (PDF) . Венгрия: OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM. С. 3/20 I. Важность некоторых неорганических молекул в живом мире 10.
- ^ Х. Адкинс ; WH Hartung (1926). «Акролеин» . Органический синтез . 6 : 1. DOI : 10,15227 / orgsyn.006.0001 .; Сборник , 1 , стр. 15
- ^ Дж. Брент Фризен; Роберт Шретцман (2011). «Дегидратация 2-метил-1-циклогексанола: новые результаты популярного студенческого лабораторного эксперимента ». J. Chem. Educ. 88 (8): 1141–1147. Bibcode : 2011JChEd..88.1141F . DOI : 10.1021 / ed900049b .
- ↑ Роден, Брайан А. (2001). «Дифенилбис (1,1,1,3,3,3-гексафтор-2-фенил-2-пропокси) сульфуран». Энциклопедия реагентов для органического синтеза . DOI : 10.1002 / 047084289X.rd409 . ISBN 0471936235.
- ^ Циммерманн, Хайнц; Вальц, Роланд (2008). «Этилен». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a10_045.pub3 . ISBN 978-3527306732.
- ^ Х. Плиенингер; Гунда Кейлич (1956). "Die Dienol-Benzol-Umlagerung" [Диенол-бензольная перегруппировка]. Энгью. Chem. (на немецком). 68 (19): 618. DOI : 10.1002 / ange.19560681914 .
- ^ Маргарет Джевник Джентлс; Джейн Б. Мосс; Хершель Л. Херцог; Е.Б. Гершберг (1958). "Диенол-бензольная перегруппировка. Некоторая химия 1,4-Андростадиен-3,17-диона". Варенье. Chem. Soc. 80 (14): 3702–3705. DOI : 10.1021 / ja01547a058 .