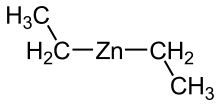 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК диэтилцинк | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.008.330 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| Номер ООН | 1366 |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| (C 2 H 5 ) 2 Zn | |
| Молярная масса | 123,50 г / моль |
| Плотность | 1,205 г / мл |
| Температура плавления | -28 ° С (-18 ° F, 245 К) |
| Точка кипения | 117 ° С (243 ° F, 390 К) |
| Реагирует бурно | |
| Опасности | |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H225 , H250 , H260 , H314 , H400 , H410 | |
| Р210 , Р222 , P223 , P231 + 232 , Р233 , Р240 , Р241 , P242 , P243 , P260 , P264 , P273 , P280 , P301 + 330 + 331 , P302 + 334 , P303 + 361 + 353 , Р304 + 340 , P305 + 351 + 338 , P310 , P321 , P335 + 334 , P363 , P370 + 378 , P391 , P402 + 404 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
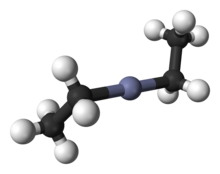
Диэтилцинк (C 2 H 5 ) 2 Zn, или DEZ, представляет собой высоко пирофорное и реакционноспособное цинкорганическое соединение, состоящее из цинкового центра, связанного с двумя этильными группами . Эта бесцветная жидкость - важный реагент в органической химии . Он коммерчески доступен в виде раствора в гексане , гептане или толуоле или в виде чистой жидкости.
Синтез [ править ]
Эдвард Франкланд впервые сообщил о соединении в 1848 году из цинка и этилиодида , первого обнаруженного цинкорганического соединения. [2] [3] Он улучшил синтез, используя диэтилртуть в качестве исходного материала. [4] Современный синтез состоит из реакции смеси 1: 1 этилйодида и этилбромида с парой цинк-медь , источником химически активного цинка. [5]
Структура [ править ]
Соединение кристаллизуется в тетрагональной объемноцентрированной элементарной ячейке с пространственной группой симметрии I4 1 мд. В твердом состоянии диэтилцинк показывает почти линейные центры Zn. Связи Zn-C имеют размер 194,8 (5) пм, в то время как угол C-Zn-C слегка изогнут на 176,2 (4) °. [6] Структура газовой фазы показывает очень похожее расстояние Zn-C (195,0 (2) пм). [7]
Использует [ редактировать ]
Несмотря на высокую пирофорность, диэтилцинк является важным химическим реагентом. Она используется в органическом синтезе в качестве источника этилового каа-на-дону в реакции присоединения к карбонильным группам. Например, асимметричное присоединение этильной группы к бензальдегиду [8] и иминам . [9] Кроме того, он обычно используется в сочетании с дииодметаном в качестве реагента Симмонса-Смита для преобразования алкенов в циклопропильные группы. [10] [11] Меньшенуклеофильный, чем родственные алкиллитиевые реактивы и реактивы Гриньяра , поэтому его можно использовать, когда требуется «более мягкий» нуклеофил. Он также широко используется в химии материаловедения в качестве источника цинка при синтезе наночастиц . В частности, при формировании оболочки из сульфида цинка для квантовых точек типа ядро / оболочка . [12] В химии полимеров его можно использовать как часть катализатора для реакции челночной полимеризации , в результате чего он участвует в живой полимеризации. [13]
Диэтилцинк используется не только в химии. Из-за своей высокой реакционной способности по отношению к воздуху он использовался в небольших количествах в качестве гиперголичного или «самовоспламеняющегося» жидкого ракетного топлива - он воспламеняется при контакте с окислителем, поэтому ракетный двигатель должен содержать только насос без источника искры для воспламенения. Диэтилцинк также исследовался Библиотекой Конгресса США как потенциальное средство массового нейтрализации кислотности книг, напечатанных на древесной целлюлозной бумаге. Теоретически пары диэтилцинка нейтрализуют кислотные остатки в бумаге, оставляя слегка щелочной оксид цинка.остатки. Хотя первоначальные результаты были многообещающими, проект был заброшен. Множество неблагоприятных результатов помешали внедрению метода. Наиболее печально известно, что последний прототип был поврежден в серии взрывов из-за контакта между следами диэтилцинка и водяного пара в камере. Это побудило авторов исследования с юмором прокомментировать:
Также установлено, что плотная или неплотная упаковка книг; количество щелочного резерва; реакции ДЭЗ с продуктами разложения, неизвестными химикатами и клеями для бумаги; фазы Луны и положения различных планет и созвездий не влияют на наблюдаемые побочные эффекты лечения ДЭЗ. [14]
В микроэлектронике диэтилцинк используется как легирующий агент . [ необходима цитата ]
Для защиты от коррозии в ядерных реакторах в свете вод реактор конструкции, обедненный оксид цинка получает путем первым прохождение через диэтилцинк обогащения центрифуги.
Пирофорность диэтилцинка может быть использована для проверки инертной атмосферы внутри перчаточного ящика . Концентрация кислорода всего несколько частей на миллион вызовет дымку бутылки с диэтилцинком при открытии. [15]
Безопасность [ править ]
Диэтилцинк бурно реагирует с водой и легко воспламеняется при контакте с воздухом. Поэтому с ним следует обращаться в инертной атмосфере .
Ссылки [ править ]
- ^ http://www.newenv.com/resources/nfpa_chemicals
- ↑ Э. Франкленд (1850). «О выделении органических радикалов» . Ежеквартальный журнал химического общества . 2 (3): 263. DOI : 10.1039 / QJ8500200263 .
- ^ Дитмар Сейферт (2001). «Алкилы цинка, Эдвард Франкленд и начало металлоорганической химии основной группы» . Металлоорганические соединения . 20 (14): 2940–2955. DOI : 10.1021 / om010439f .
- ^ Э. Франкланд , Б. Ф. Дуппа (1864). «О новой реакции для получения цинковых соединений алкил-радикала» . Журнал химического общества . 17 : 29–36. DOI : 10.1039 / JS8641700029 .
- ^ CR Ноллер (1943). «Диэтилцинк» . Органический синтез .; Сборник , 2 , стр. 184
- ^ Джон Bacsa; Феликс Ханке; Сара Хиндли; Раджеш Одедра; Джордж Р. Дарлинг; Энтони С. Джонс; Александр Штайнер (2011). «Твердотельные структуры диметилцинка и диэтилцинка» . Angewandte Chemie International Edition . 50 (49): 11685–11687. DOI : 10.1002 / anie.201105099 . PMC 3326375 . PMID 21919175 .
- ^ А. Хааланд; JC Green; GS McGrady; Эй Джей Даунс; Э. Гулло; MJ Lyall; Дж. Тимберлейк; А.В. Тутукин; HV Volden; К.-А. Остби (2003). «Длина, сила и полярность связей металл-углерод: соединения диалкилцинка изучены с помощью расчетов теории функционала плотности, газовой электронографии и фотоэлектронной спектроскопии». Dalton Transactions (22): 4356–4366. DOI : 10.1039 / B306840B .
- ^ Масато Китамура, Хиромаса Ока Сэйдзи Suga и Ryoji Нойори (2004). «Каталитическое энантиоселективное присоединение диалкилцинков к альдегидам с использованием (2S) - (-) - 3-экзо- (диметиламино) изоборнеола [(2S) -DAIB]: (S) -1-фенил-1-пропанол» . Органический синтез .CS1 maint: несколько имен: список авторов ( ссылка ); Сборник , 10 , стр. 635
- ↑ Жан-Николя Дерозье, Александр Коте, Алессандро А. Боэцио и Андре Б. Шаретт (2005). «Получение энантиомерно обогащенного (1S) -1-фенилпропан-1-амина гидрохлорида каталитическим добавлением диорганоцинковых реагентов к иминам» . Органический синтез . 83 : 5.CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Андре Б. Шаретт и Элен Лебель (2004). «(2S, 3S) - (+) - (3-Фенилциклопропил) метанол» . Органический синтез .; Сборник , 10 , стр. 613
- ^ Ёсихико Ито, Shotaro Фуджи, Масаси Nakatuska, Фумио Кавамото и Такео Saegusa (1988). «Расширение одноуглеродного кольца циклоалканонов до конъюгированных циклоалкенонов: 2-циклогептен-1-он» . Органический синтез .CS1 maint: несколько имен: список авторов ( ссылка ); Коллективный том , 6 , с. 327
- ^ Дмитрий В. Талапин; Иво Мекис; Стефан Гётцингер; Андреас Корновски; Оливер Бенсон; Хорст Веллер † (2004). "Нанокристаллы CdSe / CdS / ZnS и CdSe / ZnSe / ZnS ядро-оболочка-оболочка". Журнал физической химии B . 108 (49): 18826–18831. DOI : 10.1021 / jp046481g .
- ^ Мицуо Савамото; Тихиро Окамото; Тосинобу Хигашимура (1987). «Йодоводород / йодид цинка: новая инициирующая система для живой катионной полимеризации простых виниловых эфиров при комнатной температуре». Макромолекулы . 20 (11): 2693–2697. DOI : 10.1021 / ma00177a010 .
- ^ Кеннет Э. Харрис; Чандру Дж. Шахани (2004), Массовое снижение кислотности: инициатива по усовершенствованию процесса диэтилцинка (PDF) , Вашингтон, округ Колумбия : Библиотека Конгресса , архивировано из оригинала (PDF) 14 мая 2013 г.
- ^ Шрайвер, Duward F .; Дрездзон, Марк А. (1986). Манипуляции с воздухочувствительными соединениями . Джон Вили и сыновья. п. 57. ISBN 0-471-86773-X.
Внешние ссылки [ править ]
- Видео о воспламенении диэтилцинка в воздухе - Ноттингемский университет
