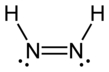| |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Диазин | |||
| Другие имена Диимид Диимин | |||
| Идентификаторы | |||
| |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| КЕГГ | |||
| MeSH | Диазин | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| H 2 N 2 | |||
| Молярная масса | 30,030 г · моль -1 | ||
| Внешность | Желтый газ | ||
| Температура плавления | -80 ° С (-112 ° F, 193 К) | ||
| Родственные соединения | |||
Другие анионы | diphosphene дифтордиазин | ||
Другие катионы | азосоединения | ||
Связанные бинарные азаны | аммиак диазан триазан | ||
Родственные соединения | isodiazene триазен тетразен | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
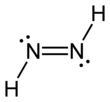
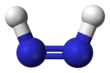
Диимид , также называемый диазеном или диимином , представляет собой соединение формулы (NH) 2 . Он существует в виде двух геометрических изомеров , E ( транс ) и Z ( цис ). Термин диазен чаще используется для органических производных диимида. Таким образом, азобензол является примером органического диазена.
Синтез [ править ]
Традиционный способ получения диимида включает окисление гидразина перекисью водорода или воздухом. [1] Альтернативно декарбоксилирование азодикарбоновой кислоты дает диимид: [2]
- (NCOOH) 2 → (NH) 2 + 2 CO 2
В настоящее время диимид получают путем термического разложения 2,4,6-триизопропилбензолсульфонилгидразида. [3]
Из-за своей нестабильности диимид образуется и используется на месте . Получают смесь цис ( Z- ) и транс ( E- ) изомеров. Оба изомера нестабильны и претерпевают медленное взаимопревращение. Транс - изомер является более стабильным, но цис - изомер является тот , который вступает в реакцию с ненасыщенными субстратами, следовательно , равновесие между ними смещается в цис - изомера из - за принципа Ле Шателье . Некоторые процедуры требуют добавления карбоновых кислот, которые катализируют цис-транс-изомеризацию. [4] Диимид легко разлагается. Даже при низких температурах более стабильныйтранс- изомер быстро претерпевает различные реакции диспропорционирования, в первую очередь с образованием гидразина и газообразного азота : [5]
- 2 HN = NH → H 2 N – NH 2 + N 2
Из-за этой конкурирующей реакции разложения для восстановления диимидом обычно требуется большой избыток реагента-предшественника.
Приложения к органическому синтезу [ править ]
Диимид иногда используется в качестве реагента в органическом синтезе . [4] Он гидрирует алкены и алкины с селективной доставкой водорода с одной стороны субстрата, что приводит к такой же стереоселективности, как и катализируемое металлами син- присоединение H 2 . Единственный побочный продукт - это азот. Хотя этот способ является громоздким, использование диимида позволяет избежать необходимости использования высоких давлений или использования газообразного водорода и металлических катализаторов, которые могут быть дорогими. [6] Механизм гидрирования включает шестичленное переходное состояние C 2 H 2 N 2 :
Избирательность [ править ]
Диимид полезен, потому что он селективно восстанавливает алкены и алкины и не реагирует со многими функциональными группами, которые могут мешать нормальному каталитическому гидрированию . Таким образом, пероксиды , алкилгалогениды и тиолы переносятся диимидом, но эти же группы обычно разрушаются металлическими катализаторами. Реагент предпочтительно восстанавливает алкины и беспрепятственные или напряженные алкены [1] до соответствующих алкенов и алканов. [4]
Связанные [ править ]
Двухкатионный форма, HNNH 2+ (diprotonated диазот), рассчитываются , чтобы иметь самую сильную известную химическую связь. Этот ион можно рассматривать как дважды протонированную молекулу азота. Порядок относительной прочности связи (RBSO) составляет 3,38. [7] FNNH 2+ и FNNF 2+ имеют связи немного меньшей прочности. [7]
Ссылки [ править ]
- ^ а б Оно, М .; Окамото, М. (1973). «цис-циклододецен» . Органический синтез .; Сборник , 5 , с. 281
- ^ Wiberg, E .; Холлеман, AF (2001). «1.2.7: Диимин, N 2 H 2 » . Неорганическая химия . Эльзевир . п. 628. ISBN 9780123526519.
- ^ Чемберлин, А. Ричард; Шеппек, Джеймс Э .; Сомоса, Альваро (2008). «2,4,6-Триизопропилбензолсульфонилгидразид». Энциклопедия реагентов для органического синтеза . DOI : 10.1002 / 047084289X.rt259.pub2 . ISBN 978-0471936237.
- ^ a b c Пасто, DJ (2001). «Диимиде». Энциклопедия реагентов для органического синтеза . Джон Вили и сыновья. DOI : 10.1002 / 047084289X.rd235 .
- ^ Виберг, Нильс; Холлеман, AF; Виберг, Эгон, ред. (2001). «1.2.7 Diimine N 2 H 2 [1.13.17]». Неорганическая химия . Академическая пресса. С. 628–632. ISBN 978-0123526519.
- ^ Миллер, CE (1965). «Гидрирование диимидом». Журнал химического образования . 42 (5): 254–259. DOI : 10.1021 / ed042p254 .
- ^ a b Калески, Роберт; Крака, Эльфи; Кремер, Дитер (12 сентября 2013 г.). «Выявление самых сильных связей в химии». Журнал физической химии . 117 (36): 8981–8995. DOI : 10.1021 / jp406200w . PMID 23927609 .