В океанической биогеохимии коэффициент f - это доля от общей первичной продукции, подпитываемой нитратами (в отличие от других азотных соединений, таких как аммоний ). Это соотношение было первоначально определено Ричардом Эппли и Брюсом Петерсоном в одной из первых работ, посвященных оценке мировой океанической продукции. [1] Эта фракция была первоначально считала важной , потому что она оказалась непосредственно связана с замиранием (экспорт) потоком из органического морского снега с поверхностью океана с помощью биологического насоса. Однако эта интерпретация основывалась на предположении о сильном разделении по глубине параллельного процесса, нитрификации , что ставится под сомнение более поздними измерениями. [2]
Обзор [ править ]
Гравитационное опускание организмов (или останков организмов) переносит углерод из поверхностных вод океана в его глубокие недра . Этот процесс известен как биологический насос, и количественная оценка его представляет интерес для ученых , поскольку он является важным аспектом Земля «s углеродного цикла . По сути, это связано с тем, что углерод, переносимый в глубокие глубины океана, изолирован от атмосферы, что позволяет океану действовать как резервуар углерода. Этот биологический механизм сопровождается физико-химическим механизмом, известным как насос растворимости, который также переносит углерод в глубину океана.
Измерение потока тонущего материала (так называемого морского снега) обычно выполняется с помощью ловушек для наносов, которые задерживают и удерживают материал, опускающийся в толщу воды . Однако это относительно сложный процесс, поскольку ловушки могут быть неудобными для развертывания или восстановления, и их необходимо оставлять на месте в течение длительного периода времени, чтобы интегрировать тонущий поток. Кроме того, известно, что они испытывают смещения и интегрируют как горизонтальные, так и вертикальные потоки из-за течений воды. [3] [4] По этой причине ученых интересуют свойства океана, которые можно легче измерить, и которые действуют в качестве косвенного признака опускающегося потока. Коэффициент f - один из таких прокси.
«Новая» и «регенерированная» продукция [ править ]
Биодоступный азот встречается в океане в нескольких формах, включая простые ионные формы, такие как нитрат (NO 3 - ), нитрит (NO 2 - ) и аммоний (NH 4 + ), а также более сложные органические формы, такие как мочевина ((NH 2 ) 2 CO). Эти формы используются автотрофным фитопланктоном для синтеза органических молекул, таких как аминокислоты (строительные блоки белков ). Выпас фитопланктона зоопланктоном и более крупными организмами переносит этот органический азот вверх по пищевой цепи.и по всей морской трофической сети .
Когда азотсодержащие органические молекулы в конечном итоге метаболизируются организмами, они возвращаются в водную толщу в виде аммония (или более сложных молекул, которые затем метаболизируются до аммония). Это называется регенерацией , поскольку аммоний может использоваться фитопланктоном и снова попадать в пищевую сеть. Таким образом, первичное производство с использованием аммония называется регенерированным производством . [5]
Однако аммоний также может быть окислен до нитрата (через нитрит) в процессе нитрификации. Это выполняется разными бактериями в два этапа:
- NH 3 + O 2 → NO 2 - + 3H + + 2e -
- NO 2 - + H 2 O → NO 3 - + 2H + + 2e -
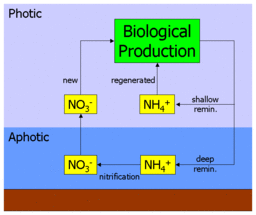
Важно отметить, что этот процесс, как полагают, происходит только в отсутствие света (или как некоторая другая функция глубины). В океане это приводит к вертикальному отделению нитрификации от первичной продукции и ограничивает ее афотической зоной . Это приводит к ситуации, когда любой нитрат в толще воды должен происходить из афотической зоны и должен происходить из органического материала, переносимого туда при опускании. Таким образом, при первичном производстве за счет нитратов используется «свежий» источник питательных веществ, а не регенерированный. Таким образом, производство нитратов относится к новому производству . [5]
Рисунок в начале этого раздела иллюстрирует это. Нитраты и аммоний потребляются первичными производителями, перерабатываются через пищевую сеть, а затем регенерируются в аммоний. Часть этого обратного потока выбрасывается на поверхность океана (где он снова становится доступным для поглощения), а часть возвращается на глубину. Аммоний, возвращенный на глубину, нитрифицируется до нитрата и, в конечном итоге, смешивается или поднимается на поверхность океана, чтобы повторить цикл.
Следовательно, значение нового производства заключается в его связи с проходящим материалом. В состоянии равновесия экспортный поток органического материала, тонущего в афотической зоне, уравновешивается восходящим потоком нитрата. Измеряя, сколько нитратов потребляется при первичном производстве по сравнению с регенерированным аммонием, можно косвенно оценить экспортный поток.
Кроме того, коэффициент f может также выявить важные аспекты функции местной экосистемы. [6] Высокие значения коэффициента f обычно связаны с продуктивными экосистемами, в которых преобладает крупный эукариотический фитопланктон (например, диатомовые водоросли ), который пасется крупным зоопланктоном (и, в свою очередь, более крупными организмами, такими как рыбы). Напротив, низкие значения f-отношения обычно связаны с низкой биомассой, олиготрофными пищевыми сетями, состоящими из небольшого прокариотического фитопланктона (такого как прохлорококк ), которые контролируются микрозоопланктоном. [7] [8]
Предположения [ править ]
Фундаментальным предположением в этой интерпретации f-отношения является пространственное разделение первичного производства и нитрификации. Действительно, в своей оригинальной статье Eppley & Peterson отметили, что: «Чтобы связать новое производство с экспортом, необходимо, чтобы нитрификация в эвфотической зоне была незначительной». [1] Однако последующие исследования распределения нитрификации показали, что нитрификация может происходить на меньших глубинах и даже в фотической зоне. [2] [9] [10]
Как показано на диаграмме рядом, если аммоний действительно нитрифицирован до нитрата в поверхностных водах океана, он по существу « замыкает » глубокий путь нитрата. На практике это привело бы к переоценке нового производства и более высокому коэффициенту f, поскольку часть якобы нового производства на самом деле будет подпитываться недавно нитрифицированным нитратом, который никогда не покидал поверхности океана. После включения измерений нитрификации в параметризацию экосистемная модель региона олиготрофного субтропического круговорота (в частности, участка BATS ) обнаружила, что ежегодно около 40% поверхностных нитратов недавно нитрифицировалось (почти до 90% летом). [11] Дальнейшее исследование, объединяющее географически разнообразные измерения нитрификации, обнаружило высокую изменчивость, но не взаимосвязано с глубиной, и применило это в модели глобального масштаба для оценки того, что до половины поверхностных нитратов поступает в результате поверхностной нитрификации, а не апвеллинга. [12]
Хотя измерения скорости нитрификации все еще относительно редки, они все же предполагают, что коэффициент f не является таким прямым показателем для биологического насоса, как когда-то считалось. По этой причине некоторые исследователи предложили проводить различие между коэффициентом f и отношением экспорта твердых частиц к первичному производству, которое они называют коэффициентом референдума . [8] Хотя количественно и отличается от f-соотношения, ре-соотношение показывает аналогичное качественное изменение между режимами высокой продуктивности / высокой биомассы / высокого экспорта и режимов низкой продуктивности / низкой биомассы / низкого экспорта.
Кроме того, еще одним процессом, который потенциально усложняет использование коэффициента f для оценки «новой» и «регенерированной» продукции, является диссимиляционное восстановление нитратов до аммония (DNRA). В условиях низкого кислорода, такие как минимум кислорода зоны и донных отложения, chemoorganoheterotrophic микроорганизмы используют нитрат в качестве акцептора электронов для дыхания , [13] восстанавливающего его в нитриты, а затем в аммоний. Поскольку, как и нитрификация, DNRA изменяет баланс в доступности нитрата и аммония, он может внести неточность в рассчитанный коэффициент f. Однако, поскольку возникновение DNRA ограничено анаэробными ситуациями, [14]его значение менее распространено, чем нитрификация, хотя оно может происходить в сочетании с первичными производителями. [15] [16]
См. Также [ править ]
- Биологический насос - биологически обусловленное улавливание углерода океаном из атмосферы во внутренние части океана и на морское дно.
- Нитрификация - биологическое окисление аммиака или аммония до нитрита с последующим окислением нитрита до нитрата.
- Первичное производство - синтез органических соединений из углекислого газа биологическими организмами.
Ссылки [ править ]
- ^ а б Эппли, RW; Петерсон, Б.Дж. (1979). «Поток твердых частиц органического вещества и новое образование планктона в глубинах океана». Природа . 282 (5740): 677–680. Bibcode : 1979Natur.282..677E . DOI : 10.1038 / 282677a0 .
- ^ a b Доре, Дж. Э .; Карл, DM (1996). «Нитрификация в эвфотической зоне как источник нитритов, нитратов и закиси азота на станции ALOHA» . Лимнол. Oceanogr . 41 (8): 1619–1628. Bibcode : 1996LimOc..41.1619D . DOI : 10,4319 / lo.1996.41.8.1619 . JSTOR 00243590 .
- ^ Thomas, S .; Ридд, П.В. (2004). «Обзор методов измерения кратковременного накопления наносов». Морская геология . 207 (1–4): 95–114. Bibcode : 2004MGeol.207 ... 95T . DOI : 10.1016 / j.margeo.2004.03.011 .
- ^ Бюсселер, КО ; и другие. (2007). «Оценка использования осадочных ловушек для оценки потоков частиц в верхних слоях океана» (PDF) . J. Mar. Res . 65 (3): 345–416. DOI : 10.1357 / 002224007781567621 . hdl : 1912/1803 . ISSN 0022-2402 .
- ^ а б Дагдейл, RC; Геринг, Дж. Дж. (1967). «Использование новых и регенерированных форм азота в первичной продуктивности» (PDF) . Лимнол. Oceanogr . 12 (2): 196–206. Bibcode : 1967LimOc..12..196D . DOI : 10,4319 / lo.1967.12.2.0196 . Архивировано из оригинального (PDF) 20 июля 2011 года.
- ^ Аллен, AE; Ховард-Джонс, MH; Бут, MG; Фришер, Мэн; Верити, PG; Бронк Д.А.; Сандерсон, член парламента (2002). «Важность гетеротрофной бактериальной ассимиляции аммония и нитратов в Баренцевом море летом». Журнал морских систем . 38 (1–2): 93–108. Bibcode : 2002JMS .... 38 ... 93A . DOI : 10.1016 / s0924-7963 (02) 00171-9 .
- ^ Законы, EA; Фальковски, П.Г .; Смит, Вашингтон; Ducklow, H .; Маккарти, Дж. Дж. (2000). «Влияние температуры на экспортную продукцию в открытом океане» . Глобальные биогеохимические циклы . 14 (4): 1231–1246. Bibcode : 2000GBioC..14.1231L . DOI : 10.1029 / 1999GB001229 .
- ^ а б Данн, JP; Армстронг, РА; Gnanadesikan, A .; Сармьенто, JL (2005). «Эмпирические и механистические модели коэффициента экспорта частиц» . Глобальные биогеохимические циклы . 19 (4): GB4026. Bibcode : 2005GBioC..19.4026D . DOI : 10.1029 / 2004GB002390 .
- ^ Raimbault, P .; Slawyk, G .; Boudjellal, B .; Коатаноан, С .; Conan, P .; Косте, В .; Garcia, N .; Moutin, T .; Пуджо-Пай, М. (1999). «Поглощение и экспорт углерода и азота в экваториальной части Тихого океана на 150 ° з. Д.: Свидетельство эффективного регенерированного производственного цикла» . J. Geophys. Res . 104 (C2): 3341–3356. Bibcode : 1999JGR ... 104.3341R . DOI : 10.1029 / 1998JC900004 .
- ^ Diaz, F .; Раймбо, П. (2000). «Регенерация азота и высвобождение растворенного органического азота весной в северо-западной прибрежной зоне Средиземного моря (Лионский залив): значение для оценки нового производства» . Mar. Ecol. Прог. Сер . 197 : 51–65. Bibcode : 2000MEPS..197 ... 51D . DOI : 10,3354 / meps197051 .
- ^ Мартин, AP; Пондавен, П. (2006). «Новое первичное производство и нитрификация в западной субтропической части Северной Атлантики: модельное исследование» . Глобальные биогеохимические циклы . 20 (4): н / д. Bibcode : 2006GBioC..20.4014M . DOI : 10.1029 / 2005GB002608 .
- ^ Yool, A .; Мартин, AP; Fernández, C .; Кларк, Д.Р. (2007). «Значение нитрификации для океанической новой продукции». Природа . 447 (7147): 999–1002. Bibcode : 2007Natur.447..999Y . DOI : 10,1038 / природа05885 . PMID 17581584 .
- ^ Крафт, Б. Strous, М. и Tegetmeyer, ОН (2011). «Микробное нитратное дыхание - гены, ферменты и распространение в окружающей среде». Журнал биотехнологии . 155 (1): 104–117. DOI : 10.1016 / j.jbiotec.2010.12.025 . PMID 21219945 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Lam, Филис и Kuypers, Марсель MM (2011). «Микробные азотные процессы в зонах минимального содержания кислорода». Ежегодный обзор морской науки . 3 : 317–345. Bibcode : 2011ARMS .... 3..317L . DOI : 10.1146 / annurev-marine-120709-142814 . PMID 21329208 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Камп, Аня; Пиво, Дирк де; Nitsch, Jana L .; Лавик, Гаут; Стиф, Питер (2011-04-05). «Диатомовые водоросли дышат нитратами, чтобы выжить в темноте и бескислородных условиях» . Труды Национальной академии наук . 108 (14): 5649–5654. Bibcode : 2011PNAS..108.5649K . DOI : 10.1073 / pnas.1015744108 . ISSN 0027-8424 . PMC 3078364 . PMID 21402908 .
- ^ Камп, Аня; Стиф, Питер; Knappe, Ян; Пиво, Дирк де (2013-12-02). «Ответ повсеместной пелагической диатомовой водоросли Thalassiosira weissflogii на темноту и аноксию» . PLOS ONE . 8 (12): e82605. Bibcode : 2013PLoSO ... 882605K . DOI : 10.1371 / journal.pone.0082605 . ISSN 1932-6203 . PMC 3846789 . PMID 24312664 .