 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК гексацианид железа (3+) | |
| Систематическое название ИЮПАК гексацианидоферрат (III) | |
| Другие имена гексацианид железа; гексацианидоферрат (3-); гексацианоферрат (III) | |
| Идентификаторы | |
3D модель ( JSmol ) | |
PubChem CID | |
CompTox Dashboard ( EPA ) | |
| |
| Характеристики | |
| [Fe (CN) 6 ] 3− | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
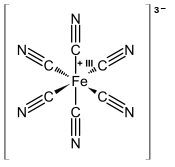
Феррицианид представляет собой анион [Fe (CN) 6 ] 3– . Его также называют гексацианоферрат (III), а в редкой, но систематической номенклатуре - гексацианидоферрат (III). Самая распространенная соль этого аниона - феррицианид калия , красный кристаллический материал, который используется в качестве окислителя в органической химии . [1]
Свойства [ править ]
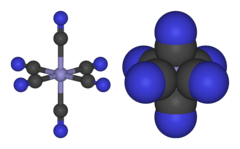
[Fe (CN) 6 ] 3– состоит из центра Fe 3+, связанного в октаэдрической геометрии с шестью цианидными лигандами . Комплекс имеет симметрию O h . Железо имеет низкое вращение и легко восстанавливается до родственного ферроцианид- иона [Fe (CN) 6 ] 4– , который является производным двухвалентного железа (Fe 2+ ). Эта окислительно-восстановительная пара обратима и не влечет за собой образования или разрыва связей Fe – C:
- [Fe (CN) 6 ] 3− + e - ⇌ [Fe (CN) 6 ] 4−
Эта окислительно-восстановительная пара является стандартом в электрохимии .
По сравнению с обычными цианиды , как цианид калия , феррицианиды гораздо менее токсичны из-за плотного трюме CN - к Fe 3+ . Однако они реагируют с минеральными кислотами с выделением высокотоксичного цианистого водорода .
Использует [ редактировать ]
Обработка феррицианида солями железа (II) дает блестящий, стойкий пигмент берлинский синий , традиционный цвет чертежей .
См. Также [ править ]
- Феррицианид калия
- Ферроцианид
Ссылки [ править ]
- ^ Gail, E .; Гос, С .; Kulzer, R .; Lorösch, J .; Rubo, A .; Sauer, M .; Kellens, R .; Редди, Дж .; Штайер, Н. "Циано-соединения, неорганические". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a08_159.pub3 .