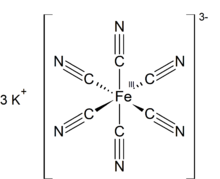 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гексацианоферрат (III) калия | |
| Другие имена Красный калия, прусский красный, феррицианид калия | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.033.916 |
| Номер ЕС |
|
| 21683 | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| K 3 [Fe (CN) 6 ] | |
| Молярная масса | 329,24 г / моль |
| Внешность | темно-красные кристаллы, иногда мелкие гранулы, порошок от оранжевого до темно-красного цвета |
| Плотность | 1,89 г / см 3 , твердый |
| Температура плавления | 300 ° С (572 ° F, 573 К) |
| Точка кипения | разлагается |
| 330 г / л («холодная вода») 464 г / л (20 ° C) 775 г / л («горячая вода») [1] | |
| Растворимость | мало растворим в спирте растворим в кислоте растворим в воде |
| + 2290,0 · 10 −6 см 3 / моль | |
| Структура | |
| моноклинический | |
| октаэдрический в Fe | |
| Опасности | |
| Паспорт безопасности | Паспорт безопасности |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
Положения об опасности GHS | H302 , H315 , H319 , H332 , H335 |
Меры предосторожности GHS | Р261 , Р264 , Р270 , Р271 , Р280 , Р301 + 312 , P302 + 352 , Р304 + 312 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P330 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 |
| NFPA 704 (огненный алмаз) |  1 0 0 |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 2970 мг / кг (мышь, перорально) |
| Родственные соединения | |
Другие анионы | Ферроцианид калия |
Другие катионы | Берлинская лазурь |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Феррицианид калия - это химическое соединение с формулой K 3 [Fe (CN) 6 ]. Эта ярко-красная соль содержит октаэдрически координированный ион [Fe (CN) 6 ] 3– . [2] Он растворим в воде, и его раствор имеет зеленовато-желтую флуоресценцию . Он был обнаружен в 1822 году Леопольда Гмелина , [3] [4] и был первоначально использован в производстве красителей ультрамарин.
Подготовка [ править ]
Калий феррицианида производится путем пропускания хлора через раствор из ферроцианида калия . Феррицианид калия выделяется из раствора:
- 2 K 4 [Fe (CN) 6 ] + Cl 2 → 2 K 3 [Fe (CN) 6 ] + 2 KCl
Структура [ править ]
Как и другие цианиды металлов, твердый феррицианид калия имеет сложную полимерную структуру. Полимер состоит из октаэдрических центров [Fe (CN) 6 ] 3–, сшитых ионами K + , которые связаны с лигандами CN . [5] Связи K + --- NCFe разрываются, когда твердое вещество растворяется в воде.
Приложения [ править ]
Компаунд также используется для упрочнения железа и стали , в гальванике , крашении шерсти , в качестве лабораторного реагента и в качестве мягкого окислителя в органической химии .
Чертеж и фотография [ править ]
Соединение широко используется в рисовании чертежей и в фотографии ( процесс цианотипирования ). Некоторые процессы тонирования фотопечати включают использование феррицианида калия.
Феррицианид калия использовался в качестве окислителя для удаления серебра с цветных негативов и позитивов во время обработки, этот процесс называется отбеливанием. Поскольку отбеливатели на основе феррицианида калия являются экологически опасными, недолговечными и способны выделять газообразный цианистый водород при смешивании с высокими концентрациями и объемами кислоты, отбеливатели с использованием ЭДТА трехвалентного железа использовались в обработке цвета с момента появления в 1972 году процесса Kodak C-41 . В цветной литографии феррицианид калия используется для уменьшения размера цветных точек без уменьшения их количества, как своего рода ручная цветокоррекция, называемая точечным травлением. Он также используется в черно-белой фотографии с тиосульфатом натрия.(гипо) для уменьшения плотности негатива или желатинового серебра, смесь известна как восстановитель Фармера; это может помочь компенсировать проблемы, связанные с передержкой негатива, или сделать светлые участки на отпечатке ярче. [6]
Реагент в органическом синтезе [ править ]
Феррицианид калия используется в качестве окислителя в органической химии. [7] [8] Это окислитель для регенерации катализатора при дигидроксилировании Шарплесса . [9] [10]
Датчики и индикаторы [ править ]
Феррицианид калия также является одним из двух соединений, присутствующих в индикаторном растворе ферроксила (наряду с фенолфталеином ), который становится синим ( берлинская лазурь ) в присутствии ионов Fe 2+ , и поэтому его можно использовать для обнаружения окисления металлов, которое приведет к ржавчине. Можно подсчитать количество молей ионов Fe 2+ с помощью колориметра из-за очень интенсивного цвета берлинской лазурь .
В физиологических экспериментах феррицианид калия обеспечивает средство, увеличивающее окислительно-восстановительный потенциал раствора (E ° '~ 436 мВ при pH 7). Таким образом, он может окислять восстановленный цитохром c (E ° ~ 247 мВ при pH 7) в изолированных митохондриях. Дитионит натрия обычно используется в качестве восстанавливающего химического вещества в таких экспериментах (E ° '~ -420 мВ при pH 7).
Феррицианид калия используется для определения потенциала восстановления трехвалентного железа в образце (экстракт, химическое соединение и т. Д.). [11] Такое измерение используется для определения антиоксидантных свойств образца.
Феррицианид калия является компонентом амперометрических биосенсоров в качестве агента переноса электронов, заменяющего естественный агент переноса электронов фермента, такой как кислород, как и фермент глюкозооксидаза . Он входит в состав имеющихся в продаже глюкометров для диабетиков .
Другое [ править ]
Феррицианид калия объединяется с гидроксидом калия (или гидроксидом натрия в качестве заменителя) и водой для получения травителя Мураками. Этот травитель используется металлографами для обеспечения контраста между связующей и карбидной фазами в цементированных карбидах.
Берлинская лазурь [ править ]
Берлинская лазурь , темно-синий пигмент в синей печати, образуется в результате реакции K 3 [Fe (CN) 6 ] с ионами двухвалентного железа (Fe 2+ ), а также K 4 [Fe (CN) 6 ] с солями трехвалентного железа. [12]
В гистологии феррицианид калия используется для обнаружения двухвалентного железа в биологической ткани. Феррицианид калия реагирует с двухвалентным железом в кислотном растворе с образованием нерастворимого синего пигмента, обычно называемого синим Тернбулла или берлинской лазурью . Для обнаружения трехвалентного (Fe 3+ ) железа вместо этого в методе окрашивания берлинской лазурью Перлса используется ферроцианид калия . [13] Материал, образующийся в реакции синего Тернбулла, и соединение, образующееся в реакции берлинской синей, одинаковы. [14] [15]
Безопасность [ править ]
Феррицианид калия имеет низкую токсичность, его основная опасность заключается в том, что он вызывает легкое раздражение глаз и кожи. Однако в очень сильно кислых условиях выделяется высокотоксичный цианистый водород в соответствии с уравнением:
- 6 H + + [Fe (CN) 6 ] 3− → 6 HCN + Fe 3+ [16]
См. Также [ править ]
- Феррицианид
- Ферроцианид
- Ферроцианид калия
Ссылки [ править ]
- ^ Квонг, Х.-Л. (2004). «Феррицианид калия». В пакете, Л. (ред.). Энциклопедия реагентов для органического синтеза . Нью-Йорк: J. Wiley & Sons. DOI : 10.1002 / 047084289X .
- ^ Шарп, AG (1976). Химия цианокомплексов переходных металлов . Лондон: Academic Press.
- ^ Гмелин, Леопольд (1822). "Ueber ein besonderes Cyaneisenkalium и über eine neue Reihe von blausauren Eisensalzen" [Об особом цианате калия и железе и о новой серии солей железа циановой кислоты]. Journal für Chemie und Physik (на немецком языке). 34 : 325–346.
- ^ Ihde, AJ (1984). Развитие современной химии (2-е изд.). Нью-Йорк: Dover Publications. п. 153.
- ^ Фиггис, Б.Н.; Gerloch, M .; Мейсон Р. «Кристаллография и парамагнитная анизотропия феррицианида калия» Труды Лондонского королевского общества, серия A: математические и физические науки 1969, вып. 309, с. 91-118. DOI : 10.1098 / rspa.1969.0031
- ^ Stroebel, L .; Закия, RD (1993). «Фермерский редуктор» . Фокальная энциклопедия фотографии . Focal Press. п. 297. ISBN. 978-0-240-51417-8.
- ^ Прилл, EA; McElvain, SM (1935). «1-Метил-2-Пиридон». Органический синтез . 15 : 41. DOI : 10,15227 / orgsyn.015.0041 .
- ^ Вюрфель, Хендрик; Якоби, Дёрте (2018). «Синтезы замещенных 2-цианобензотиазолов». Органический синтез . 95 : 177–191. DOI : 10.15227 / orgsyn.095.0177 .
- ^ Гонсалес, Хавьер; Ауригемма, Кристина; Трусдейл, Ларри (2002). «Синтез (+) - (1S, 2R) - и (-) - (1R, 2S) - транс -2-фенилциклогексанола посредством асимметричного дигидроксилирования Шарплесса (AD)». Органический синтез . 79 : 93. DOI : 10,15227 / orgsyn.079.0093 .
- ^ Ой, Рю; Шарплесс, К. Барри (1996). «3 - [(1S) -1,2-дигидроксиэтил] -1,5-дигидро-3H-2,4-бензодиоксепин». Органический синтез . 73 : 1. DOI : 10,15227 / orgsyn.073.0001 .
- Перейти ↑ Nakajima, Y., Sato, Y., & Konishi, T. (2007). Антиоксидантные небольшие фенольные ингредиенты в Inonotus obliquus (человек) Pilat (Chaga). Химический и фармацевтический бюллетень, 55 (8), 1222–1276.
- ^ Данбар, КР; Хайнц, РА (1997). «Химия соединений цианидов переходных металлов: современные перспективы». Прогресс в неорганической химии . Прогресс в неорганической химии. 45 . С. 283–391. DOI : 10.1002 / 9780470166468.ch4 . ISBN 9780470166468.
- Перейти ↑ Carson, FL (1997). Гистотехнология: текст для самообучения (2-е изд.). Чикаго: Американское общество клинических патологов. С. 209–211. ISBN 978-0-89189-411-7.
- ^ Tafesse, F. (2003). «Сравнительные исследования берлинской синей или диакватетраамин-кобальта (III), способствующей гидролизу 4-нитрофенилфосфата в микроэмульсиях» (PDF) . Международный журнал молекулярных наук . 4 (6): 362–370. DOI : 10.3390 / i4060362 .
- ^ Verdaguer, M .; Galvez, N .; Garde, R .; Деспланш, К. (2002). "Электроны в действии в аналогах берлинской лазурки" (PDF) . Интерфейс электрохимического общества . 11 (3): 28–32. DOI : 10.1002 / chin.200304218 .
- ^ "MSDS для феррицианида калия" (PDF) .
Внешние ссылки [ править ]
- Международная карта химической безопасности 1132
- Национальный реестр загрязнителей - информационный бюллетень по цианидным соединениям