| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Фуран [1] | |||
| Систематическое название ИЮПАК 1,4-эпоксибута-1,3-диен 1-оксациклопента-2,4-диен | |||
| Другие названия Оксол Окса [5] аннулен 1,4- Эпокси -1,3-бутадиен 5-Оксациклопента-1,3-диен 5-Оксацикло-1,3-пентадиен Фурфуран Дивиниленоксид | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.390 | ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 4 Н 4 О | |||
| Молярная масса | 68,075 г · моль -1 | ||
| Появление | Бесцветная летучая жидкость | ||
| Плотность | 0,936 г / мл | ||
| Температура плавления | -85,6 ° С (-122,1 ° F, 187,6 К) | ||
| Точка кипения | 31,3 ° С (88,3 ° F, 304,4 К) | ||
| -43,09 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Паспорт безопасности | Pennakem | ||
| R-фразы (устаревшие) | R26 / 27/28 , R45 | ||
| S-фразы (устаревшие) | S16 , S37 , S45 , S28 | ||
| NFPA 704 (огненный алмаз) |  3 4 1 | ||
| точка возгорания | -36 ° С (-33 ° F, 237 К) | ||
самовоспламенения температуру | 390 ° С (734 ° F, 663 К) | ||
| Пределы взрываемости | Нижняя: 2,3% Верхняя: 14,3% при 20 ° C | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | > 2 г / кг (крыса) | ||
| Родственные соединения | |||
Родственные гетероциклы | Пиррол Тиофен | ||
Родственные соединения | Тетрагидрофуран (THF) 2,5-Диметилфуран Бензофуран Дибензофуран | ||
| Состав | |||
Группа точек | C 2v | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
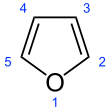
Фуран - это гетероциклическое органическое соединение , состоящее из пятичленного ароматического кольца с четырьмя атомами углерода и одним атомом кислорода . Химические соединения, содержащие такие кольца, также называют фуранами.
Фуран - бесцветная, легковоспламеняющаяся , легколетучая жидкость с температурой кипения, близкой к комнатной. Он растворим в обычных органических растворителях , включая спирт , эфир и ацетон , и мало растворим в воде . [2] Его запах «сильный, эфирный, похожий на хлороформ ». [3] Он токсичен и может быть канцерогенным для человека. Фуран используется в качестве отправной точки для других специальных химикатов . [4]
История [ править ]
Название «фуран» происходит от латинского furfur , что означает отруби . [5] ( Фурфурол получают из отрубей.) Первым описанным производным фурана была 2-фурановая кислота , произведенная Карлом Вильгельмом Шееле в 1780 году. Другое важное производное, фурфурол , было описано Иоганном Вольфгангом Доберейнером в 1831 году и охарактеризовано девятью годами позже пользователя John Stenhouse . Сам фуран был впервые получен Генрихом Лимприхтом в 1870 году, хотя он назвал его «тетрафенол» (как если бы это был четырехуглеродный аналог фенола , C 6 H 6 O).[6] [7]
Производство [ править ]
В промышленности фуран производится декарбонилированием фурфурола , катализируемым палладием , или окислением 1,3-бутадиена, катализируемым медью : [4]
В лаборатории фуран можно получить из фурфурола окислением до 2-фурановой кислоты с последующим декарбоксилированием . [8] Он также может быть получен непосредственно термическим разложением из пентозов отработанных материалов, а также целлюлозных твердых частицами, особенно сосновое дерево.
Синтез фуранов [ править ]
Синтез Собачонка-Бенари является классическим способом синтеза фуранов, хотя многие Синтезы были разработаны. [9] Одним из простейших методов синтеза фуранов является реакция 1,4-дикетонов с пентоксидом фосфора (P 2 O 5 ) в синтезе Паала-Кнорра . Реакция образования тиофена 1,4-дикетонов с реактивом Лавессона также приводит к образованию фуранов в качестве побочных продуктов. Существует множество способов синтеза замещенных фуранов. [10]
Химия [ править ]
Фуран является ароматическим , потому что один из одиноких пар из электронов на атоме кислорода делокализован в кольцо, создавая 4 п +-ароматическую систему (см правила Хюккеля ) , похожей на бензол . Из-за ароматичности молекула плоская и не имеет дискретных двойных связей . Другая неподеленная пара электронов атома кислорода проходит в плоскости плоской кольцевой системы. Зр 2 гибридизации , чтобы позволить одной из одиноких пар кислорода проживать в р орбитальных и , таким образом , чтобы позволить ему взаимодействовать в пределах системы П .
Из-за своей ароматичности поведение фурана совершенно не похоже на поведение более типичных гетероциклических эфиров, таких как тетрагидрофуран .
- Он значительно более активен, чем бензол, в реакциях электрофильного замещения из-за электронодонорных эффектов гетероатома кислорода. Исследование вкладчиков резонанса показывает повышенную электронную плотность кольца, что приводит к увеличению скорости электрофильного замещения. [11]
- Фуран служит диеном в реакциях Дильса-Альдера с электронодефицитными диенофилами, такими как этил ( E ) -3-нитроакрилат. [12] Продукт реакции представляет собой смесь изомеров, предпочтительно эндо- изомер :
- Реакция Дильса-Альдера фурана с аринами дает соответствующие производные дигидронафталина , которые являются полезными промежуточными продуктами в синтезе других полициклических ароматических соединений . [13]
- Гидрирование фуранов последовательно дает дигидрофураны и тетрагидрофураны .
- В реакции Ахматовича фураны превращаются в дигидропирановые соединения.
- Пиррол может быть получен промышленным способом путем взаимодействия фурана и аммиака в присутствии твердых кислотных катализаторов , таких как SiO 2 и Al 2 O 3 . [14]
Безопасность [ править ]
Фуран содержится в термически обработанных коммерческих пищевых продуктах и производится путем термического разложения натуральных компонентов пищи. [15] [16] Его можно найти в жареном кофе , растворимом кофе и обработанном детском питании . [16] [17] [18] Исследования показали , что кофе , приготовленный в эспрессо мейкер , и кофе из капсул содержат более фуран , чем из традиционных производителей капельного кофе , хотя они по- прежнему в безопасных пределах здоровья. [19]
Воздействие фурана в дозах, примерно в 2000 раз превышающих прогнозируемый уровень воздействия на человека из пищевых продуктов, увеличивает риск гепатоцеллюлярных опухолей у крыс и мышей и опухолей желчных протоков у крыс. [20] Таким образом, фуран внесен в список возможных канцерогенов для человека . [20]
См. Также [ править ]
- BS 4994 - Фурановая смола как термореактивный стеклопластик для оборудования химических производств
- Фуранокумарин
- Фуранофлавоноид
- Фураноза
- Фурантетракарбоновая кислота
- Простые ароматические кольца
- Фурановые жирные кислоты
- Тетрагидрофуран
Ссылки [ править ]
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 392. DOI : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
- ^ Якубке, Ганс Дитер; Jeschkeit, Ганс (1994). Краткая энциклопедия химии . Вальтер де Грюйтер. С. 1–1201 . ISBN 0-89925-457-8.
- ^ Публикация DHHS (NIOSH) № 2016–171 , стр. 2, по состоянию на ноябрь 2019 г.
- ^ a b Hoydonckx, HE; Ван Рейн, ВМ; Van Rhijn, W .; Де Вос, Германия; Джейкобс, П.А. "Фурфурол и производные". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a12_119.pub2 .
- ^ Сеннинг, Александр (2006). Словарь химиоэтимологии Эльзевьера . Эльзевир. ISBN 0-444-52239-5.
- ^ Лимприхт, Х. (1870). "Ueber das Tetraphenol C 4 H 4 O" . Berichte der Deutschen Chemischen Gesellschaft . 3 (1): 90–91. DOI : 10.1002 / cber.18700030129 .
- ^ Родд, Эрнест Гарри (1971). Химия углеродных соединений: современный всеобъемлющий трактат . Эльзевир.
- Перейти ↑ Wilson, WC (1941). «Фуран» . Органический синтез .; Сборник , 1 , стр. 274
- ^ Хоу, XL; Cheung, HY; Hon, TY; Kwan, PL; Lo, TH; Тонг, SY; Вонг, HN (1998). «Региоселективный синтез замещенных фуранов». Тетраэдр . 54 (10): 1955–2020. DOI : 10.1016 / S0040-4020 (97) 10303-9 .
- ^ Катрицки, Алан Р. (2003). «Синтез 2,4-дизамещенных фуранов и 4,6-диарил-замещенных 2,3-бензо-1,3a, 6a-триазапентален» (PDF) . Arkivoc . 2004 (2): 109. DOI : 10,3998 / ark.5550190.0005.208 .
- ^ Bruice, Paula Y. (2007). Органическая химия (5-е изд.). Река Аппер Сэдл, Нью-Джерси: Пирсон Прентис Холл. ISBN 978-0-13-196316-0.
- ^ Masesane, I .; Бацанов, А .; Howard, J .; Modal, R .; Сталь, П. (2006). «Оксанорборненовый подход к 3-гидрокси, 3,4-дигидрокси и 3,4,5-тригидроксипроизводным 2-аминоциклогексанкарбоновой кислоты» . Журнал органической химии Бейльштейна . 2 (9): 9. DOI : 10,1186 / 1860-5397-2-9 . PMC 1524792 . PMID 16674802 .
- ^ Филатов, М.А.; Балущев, С .; Илиева И.З .; Enkelmann, V .; Митева, Т .; Ландфестер, К .; Алещенков С.Е .; Чепраков, А.В. (2012). «Тетраарилтетраантра [2,3] порфирины: синтез, структура и оптические свойства» (PDF) . J. Org. Chem . 77 (24): 11119–11131. DOI : 10.1021 / jo302135q . PMID 23205621 . Архивировано из оригинального (PDF) на 19 февраля 2020 года.
- ^ Harreus, Альбрехт Людвиг. «Пиррол». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a22_453 .
- ^ Anese, M .; Manzocco, L .; Calligaris, S .; Николи, MC (2013). «Промышленно применимые стратегии по снижению содержания акриламида, фурана и 5-гидроксиметилфурфурола в пищевых продуктах» (PDF) . Журнал сельскохозяйственной и пищевой химии . 61 (43): 10209–14. DOI : 10.1021 / jf305085r . PMID 23627283 . Архивировано из оригинального (PDF) 08.08.2017.
- ^ a b Moro, S .; Чипман, Дж. К.; Wegener, JW; Hamberger, C .; Декант, В .; Малли А. (2012). «Фуран в термически обработанных пищевых продуктах: образование, воздействие, токсичность и аспекты оценки риска» (PDF) . Молекулярное питание и пищевые исследования . 56 (8): 1197–1211. DOI : 10.1002 / mnfr.201200093 . hdl : 1871/41889 . PMID 22641279 .
- ^ Европейское агентство по безопасности пищевых продуктов (2011). «Обновленная информация об уровнях фурана в пищевых продуктах по результатам мониторинга 2004–2010 гг. И оценка воздействия» . Журнал EFSA . 9 (9): 2347. DOI : 10,2903 / j.efsa.2011.2347 .
- ^ Waizenegger, J .; Winkler, G .; Кубалла, Т .; Ruge, W .; Керстинг, М .; Alexy, U .; Лахенмайер, DW (2012). «Анализ и оценка риска фурана в кофейных продуктах, предназначенных для подростков». Пищевые добавки и загрязняющие вещества: Часть A . 29 (1): 19–28. DOI : 10.1080 / 19440049.2011.617012 . PMID 22035212 . S2CID 29027966 .
- ^ «Эспрессо: кофе в капсулах содержит больше фурана, чем остальной» . Science Daily . 14 апреля 2011 г.
- ^ а б Бахия, Н .; Аппель, К.Е. (2010). «Токсичность и канцерогенность фурана в рационе человека» (PDF) . Архив токсикологии . 84 (7): 563–578. DOI : 10.1007 / s00204-010-0531-у . PMID 20237914 . S2CID 19389984 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме Фурана . |
- Современные синтетические методы