 | |
 | |
| Имена | |
|---|---|
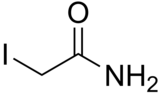
| Предпочтительное название IUPAC 2-йодацетамид | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.005.119 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 2 H 4 I N O | |
| Молярная масса | 184,964 г · моль -1 |
| Появление | белые кристаллы (желтый цвет указывает на присутствие йода) |
| Температура плавления | 94 ° С (201 ° F, 367 К) |
| Опасности | |
| Паспорт безопасности | MSDS 1 , MSDS 2 |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
2-Йодацетамид представляет собой алкилирующий агент, используемый для целей картирования пептидов . Его действие аналогично действию йодацетата . Он обычно используется для ковалентного связывания с тиоловой группой цистеина, поэтому белок не может образовывать дисульфидные связи . [1] [2] Также используется в исследованиях убиквитина в качестве ингибитора ферментов деубиквитиназы (DUB), поскольку он алкилирует остатки цистеина в активном центре DUB.
Ингибитор пептидазы [ править ]
Йодацетамид является необратимым ингибитором всех цистеинпептидаз, причем механизм ингибирования происходит за счет алкилирования каталитического остатка цистеина (см. Схему). По сравнению с его кислотным производным, йодацетатом, йодацетамид вступает в реакцию значительно быстрее. Это наблюдение противоречит стандартной химической реакционной способности, однако наличие благоприятного взаимодействия между положительным ионом имидазолия каталитического гистидина и отрицательно заряженной карбоксильной группой йодацетата является причиной повышенной относительной активности йодацетамида. [3]
Масс-спектрометрия белков [ править ]
Он обычно используется во время пробоподготовки для de novo (пептидного) секвенирования с помощью масс-спектрометрии белков , но недавние критики предлагают избегать его использования [4]
Ссылки [ править ]
- ^ Смайт CV (1936). «Реакции йодацетата и йодацетамида с различными сульфгидрильными группами, с уреазой и дрожжевыми препаратами» . J. Biol. Chem . 114 (3): 601–12. DOI : 10.1016 / S0021-9258 (18) 74789-3 .
- ^ Энсон ML (1940). «Реакции йода и йодацетамида с нативным яичным альбумином» . J. Gen. Physiol . 23 (3): 321–31. DOI : 10,1085 / jgp.23.3.321 . PMC 2237930 . PMID 19873158 .
- Перейти ↑ Polgar, L (1979). «Влияние изотопа дейтерия на ацилирование папаина. Доказательства отсутствия общего основного катализа и для группы, уходящей ферментом. Взаимодействие». Евро. J. Biochem . 98 (2): 369–374. DOI : 10.1111 / j.1432-1033.1979.tb13196.x . PMID 488108 .
- ^ Мюллер (2017). «Систематическая оценка восстановления белков и алкилирования выявляет массивные неспецифические побочные эффекты йодсодержащих реагентов» . Молекулярная и клеточная протеомика . 16 (7): 1173–1187. DOI : 10.1074 / mcp.M116.064048 . PMC 5500753 . PMID 28539326 .
Внешние ссылки [ править ]
- MEROPS онлайн база данных для пептидазы и их ингибиторов: [1]
