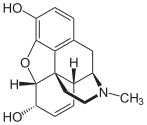
Алкалоиды изохинолина являются натуральными продуктами группы алкалоидов , которые химически получены из изохинолина . Они составляют самую большую группу среди алкалоидов. [1]
Изохинолиновые алкалоиды можно дополнительно классифицировать на основе их различных основных химических структур. Наиболее распространенными структурными типами являются бензилизохинолины и апорфины. [2] Согласно современным данным, в настоящее время известно около 2500 изохинолиновых алкалоидов, которые в основном образуются растениями. [3]
Известные примеры [ править ]
Встречаемость в природе [ править ]
Изохинолиновые алкалоиды в основном образуются в семействах растений Papaveraceae , Berberidaceae , Menispermaceae , Fumariaceae и Ranunculaceae .
Опийный мак, который принадлежит к семейству Papavaraceae, представляет большой интерес, поскольку в его латексе можно найти изохинолиновые алкалоиды морфин, кодеин, папаверин, носкапин и тебаин. [3] Помимо опийного мака, есть и другие растения мака, такие как чистотел, в котором содержатся изохинолиновые алкалоиды. Их латекс содержит берберин, который также встречается в других семействах растений, таких как Berberidaceae. [4] Примером Berberidaceae с ингредиентом берберина является Berberis vulgaris . [5]
Алкалоид тубокурарин содержится в волосатых хрящах дерева. Там тубокурарин извлекается из коры и корней. [6]
Опийный мак : содержит морфин, кодеин и папаверин.
Чистотел : содержит берберин
Барбарис обыкновенный : содержит берберин
Биологический эффект [ править ]
В целом алкалоиды изохинолина могут иметь разные эффекты. Алкалоиды опия могут обладать седативными , психотропными или обезболивающими свойствами. [7] Морфин и кодеин действительно используются в качестве анальгетиков. [8]
Папаверин, напротив, обладает спазмолитическим действием, если он поступает из гладкой мускулатуры, как в случае желудочно-кишечного тракта или кровеносных сосудов у людей . Вот почему он используется как спазмолитическое средство. [9]
Тубокурарин нарушает передачу раздражителей в нервной системе, поэтому в пораженном организме может возникнуть паралич . [10]
Ссылки [ править ]
- ^ Gerhard Habermahl, Питер Е. Хамманн Ганс С. Кребса, Waldemar Терн: Naturstoffe. Springer-Verlag, Берлин / Гейдельберг 2008, ISBN 978-3-540-73733-9 , DOI: 10.1007 / 978-3-540-73733-9 , S. 176–187.
- ^ Беттина Рафф: Chemische und biochemische Methoden zur stereoselektiven Synthese von komplexen Naturstoffen. Verlag Logos, Берлин 2012 г., ISBN 978-3-8325-3121-8 , S. 8. ( [1] , стр. 8, в Google Книгах )
- ^ а б Дженнифер М. Файнфилд, Дэвид Х. Шерман, Мартин Крейтман, Роберт М. Уильямс: Enantiomere Naturstoffe: Vorkommen und Biogense. В: Angewandte Chemie. Wiley-VCH, Weinheim 2012, DOI: 10.1002 / ange.201107204 , S. 4905–4915.
- ^ A. Husemann, T. Husemann: Die Pflanzenstoffe в химическом, физиологическом, фармакологическом и токсикологическом Hinsicht. Берлин 1871, С. 245–253. (Digitalisat Bayerische Staatsbibliothek) .
- ↑ Запись на Берберин . в: Römpp Online . Георг Тиме Верлаг, получено 13. декабря 2017 г.
- ^ Рудольф Гензель, Йозеф Хёльцль: Lehrbuch der Pharmazeutischen Biologie. Springer-Verlag, Берлин / Гейдельберг / Нью-Йорк 2012, 1996, ISBN 3-642-64628-X , DOI : 10.1007 / 978-3-642-60958-9 , S. 302.
- ^ Rainer Nowack: Notfallhandbuch Giftpflanzen: Ein Bestimmungsbuch für Ärzte унд Апотекер . Springer-Verlag, Берлин / Гейдельберг 1998, DOI: 10.1007 / 978-3-642-58885-3 , S. 258.
- ^ Йенс Фракенпол: Морфин и опиоид-анальгетика. В: Chemie unserer Zeit. WILEY-VCH, Weinheim, 2000, DOI: 10.1002 / 1521-3781 (200004) 34 , S. 99–112.
- ^ Франц фон Брухгаузен, Герд Даннхардт, Зигфрид Эбель, Август-Вильгельм Фрам, Эберхард Хакенталь, Ульрике Хольцграбе: Hagers Handbuch der Pharmazeutischen Praxis. 5. Auflage. Springer-Verlag, Берлин / Гейдельберг 1994, DOI: 10.1007 / 978-3-642-57880-9 , S. 16.
- ^ Хайнц Люльманн, Клаус Мор, Лутц Хайн: Pharmakologie und Toxikologie. 16. Auflage. Георг-Тим Верлаг, Штутгарт / Нью-Йорк 2006, ISBN 3-13-368516-3 , S. 255–258.