| Имена | |||
|---|---|---|---|
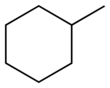
| Название ИЮПАК метилциклогексан | |||
| Другие имена Гексагидротолуолдиизоцианата Cyclohexylmethane Толуол hexahydride | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.296 | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 7 H 14 | |||
| Молярная масса | 98,189 г · моль -1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | обморок, бензол -как [1] | ||
| Плотность | 0,77 г / см 3 | ||
| Температура плавления | -126,3 ° С (-195,3 ° F, 146,8 К) | ||
| Точка кипения | 101 ° С (214 ° F, 374 К) | ||
| 0,014 г / л при 25 ° C [2] | |||
| Давление газа | 37 мм рт. Ст. (20 ° C) [1] 49,3 гПа при 20,0 ° C | ||
| -78,91 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Основные опасности | серьезная пожарная опасность | ||
| Паспорт безопасности | [2] | ||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасность | ||
| H225 , H304 , H315 , H336 , H410 [2] | |||
| Р210 , Р235 , Р301 + 310 , P331 , P370 + 378 , P403 [2] | |||
| NFPA 704 (огненный алмаз) |  3 1 0 | ||
| точка возгорания | −4 ° C (25 ° F, 269 K) [2] закрытый стакан | ||
самовоспламенения температуру | 283 ° С (541 ° F, 556 К) [2] | ||
| Пределы взрываемости | 1,2% -6,7% [1] [2] | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 2250 мг / кг (мышь, перорально) [3] | ||
ЛК 50 ( средняя концентрация ) | 10172 частей на миллион (мышь, 2 часа) 10 000-12 500 частей на миллион (мышь, 2 часа) 15227 частей на миллион (кролик, 1 час) [3] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 500 частей на миллион (2000 мг / м 3 ) [1] | ||
REL (рекомендуется) | TWA 400 частей на миллион (1600 мг / м 3 ) [1] | ||
IDLH (Непосредственная опасность) | 1200 страниц в минуту [1] | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Метилциклогексан представляет собой органическое соединение с молекулярной формулой CH 3 C 6 H 11 . Классифицируется как насыщенный углеводород , это бесцветная жидкость со слабым запахом. Метилциклогексан используется в качестве растворителя . Оно главным образом преобразуется в нафты реформаторов в толуоле . [4] Метилциклогексан также используется в некоторых корректирующих жидкостях (таких как White-Out) в качестве растворителя.
Производство и использование [ править ]
Его также можно получить гидрированием толуола:
- CH 3 C 6 H 5 + 3 H 2 → CH 3 C 6 H 11
Метилциклогексан, как компонент смеси, обычно дегидрируется до толуола, что увеличивает октановое число бензина. [4]
- Превращение метилциклогексана в толуол - классическая реакция ароматизации . Этот процесс, катализируемый платиной (Pt), широко применяется при производстве бензина из нефти. [5]
Он также является одним из основных веществ в суррогатных смесях авиационного топлива , например, для реактивного топлива А. [6] [7]
Растворитель [ править ]
Метилциклогексан используется в качестве органического растворителя со свойствами, подобными родственным насыщенным углеводородам, таким как гептан . [8] Он также является растворителем во многих типах корректирующих жидкостей.
Структура [ править ]
Метилциклогексан представляет собой монозамещенный циклогексан, поскольку он имеет одно разветвление через присоединение одной метильной группы к одному атому углерода циклогексанового кольца. Как и все циклогексаны, он может быстро превращаться между двумя конформерами стульев . Наименьшая энергетическая форма этого монозамещенного метилциклогексана возникает, когда метильная группа занимает экваториальное, а не аксиальное положение . Это равновесие воплощено в понятии стоимости A . В аксиальном положении метильная группа испытывает стерическое сжатие (стерическое напряжение) из-за присутствия аксиальных атомов водорода на одной стороне кольца (известное как 1,3-диаксиальные взаимодействия). Существует два таких взаимодействия, при этом каждая попарная комбинация метил / водород дает примерно 7,61 кДж / моль энергии деформации. Экваториальная конформация не испытывает такого взаимодействия и поэтому является энергетически благоприятной конформацией.
Воспламеняемость и токсичность [ править ]
Метилциклогексан легко воспламеняется.
Кроме того, он считается «очень токсичным для водных организмов». [9] Обратите внимание, в то время как метилциклогексан является подструктура из 4-methylcyclohexanemethanol (MCHM), он отличается по своей физической, химической и биологической (экологические, метаболические и токсикологические свойства). [10]
Ссылки [ править ]
- ^ a b c d e f Карманный справочник NIOSH по химической опасности. «# 0406» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b c d e f g h Sigma-Aldrich Co. , Метилциклогексан . Проверено 21 ноября 2017.
- ^ a b «Метилциклогексан» . Немедленно опасные для жизни или здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б М. Ларри Кэмпбелл. «Циклогексан» в Энциклопедии промышленной химии Ульмана, Wiley-VCH, Weinheim, 2012. doi : 10.1002 / 14356007.a08_209.pub2
- ^ Гэри, JH; Хандверк, GE (1984). Технология и экономика нефтепереработки (2-е изд.). Марсель Деккер, Inc. ISBN 0-8247-7150-8.
- ^ Тим Эдвардс, Мередит Колкет, Ник Чернански, Фред Драйер, Фокион Эголфопулос, Дэн Френд, Эд Лоу, Дэйв Ленхерт, Питер Линдстедт, Хайнц Питч, Адель Сарофим, Кэл Сешадри, Митч Смук, Вин Цанг и Скип Уильямс, 2007, AIAA2007- 770: Разработка экспериментальной базы данных и кинетических моделей для суррогатного реактивного топлива, 45-е совещание и выставка AIAA Aerospace Sciences, 8-11 января 2007 г., Рино, Невада, DOI 10.2514 / 6.2007-770, см. [1] , по состоянию на 27 мая 2014 г.
- ^ Мередит Колкет, Тим Эдвардс, Фред Драйер, Скип Уильямс, Николас Сернанский, Дэвид Миллер, Фокион Эгольфопулос, Фредерик Драйер и Джозетт Беллан, 2008, AIAA 2008-972: Идентификация целевых данных валидации для разработки суррогатных реактивных топлив, 46-я AIAA Aerospace Science Meeting and Exhibit, 8-11 января 2007 г., Рино, Невада, DOI 10.2514 / 6.2008-972, см. [2] , по состоянию на 27 мая 2014 г.
- ^ D. Брайс-Смит и ET Blues "Несольватированный хлорид н-бутилмагния" Org. Synth. 1967, 47, 113. DOI : 10,15227 / orgsyn.047.0113
- ^ Chevron Phillips, 2014, «Паспорт безопасности материала: метилциклогексан (версия 1.5)», см. [3] , по состоянию на 23 мая 2014 г.
- ↑ CDC, 2014, «Метилциклогексан», Карманный справочник NIOSH по химической опасности, см. [4] , по состоянию на 27 мая 2014 года.