 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / П æ п д г ə л oʊ п / [1] |
| Торговые наименования | • Дека-дураболин (как ND ) • Дураболин (как NPP ) • Многие другие (см. Здесь ) |
| Другие имена | • 19-нортестостерон [2] [3] • 10-нортестостерон • Эстр-4-ен-17β-ол-3-он • Эстренолон • Эстренолон • 19-норандрост-4-ен-17β-ол-3-он • Норандростенолон [2] • Нортестрионат [2] • Нортестонат [2] • Норандрун • SG-4341 [2] [3] |
Категория беременности |
|
| Пути администрирования | • IM инъекции ( сложные эфиры ) • SC инъекций ( сложные эфиры ) • Глазные капли ( NS ) |
| Класс препарата | Андроген ; Анаболический стероид ; Прогестаген |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетические данные | |
| Биодоступность | • Орально : <3% (свиньи) [4] • Внутримышечно : высокое [5] |
| Метаболизм | Печень ( уменьшение ) [6] [8] |
| Метаболиты | • 5α-дигидронандролон [6] [7] • 19-норандростерон [6] • 19-норэтиохоланолон [6] • Конъюгаты [8] |
| Ликвидация Период полураспада | • Нандролон: <4,3 часа [6] • ND ( IM ): 6–12 дней [6] [7] [9] • NPP : 2,7 дня [9] |
| Продолжительность действия | • ND ( IM ): 2–3 недели [7] [10] • NPP ( IM ): 5–7 дней [7] [9] |
| Экскреция | Моча [6] |
| Идентификаторы | |
Название ИЮПАК
| |
| Количество CAS |
|
| PubChem CID |
|
| IUPHAR / BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| ЧЭБИ |
|
| ЧЭМБЛ |
|
| Панель управления CompTox ( EPA ) |
|
| ECHA InfoCard | 100.006.457 |
| Химические и физические данные | |
| Формула | С 18 Н 26 О 2 |
| Молярная масса | 274,404 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
| (проверять) | |
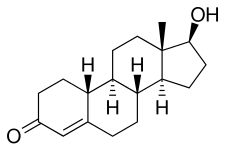
Нандролон , также известный как 19-нортестостерон , представляет собой андроген и анаболический стероид (AAS), который используется в форме сложных эфиров, таких как деканоат нандролона (торговая марка Deca-Durabolin ) и фенилпропионат нандролона (торговая марка Durabolin ). [2] [11] [7] [12] Эфиры нандролона используются при лечении анемии , кахексии (синдрома истощения), остеопороза , рака груди и по другим показаниям. [7] Они не используютсявнутрь, а вместо этого вводятся путем инъекции в мышцы или жир . [7] [12] [13]
Побочные эффекты нандролона эфиров включают симптомы из маскулинизации , как акне , повышенный рост волос , голос меняется , и снижение полового влечения в связи с его способностью подавлять эндогенный синтез тестостерона, не являясь сам по себе является достаточным андрогенов. [7] Они являются синтетические андрогены и анаболические стероиды и , следовательно , являются агонисты по андрогенного рецептора (AR), по биологической мишени андрогенов , таких как тестостерон и дигидротестостерон (ДГТ). [7] [14]Нандролон обладает сильными анаболическими эффектами и слабыми андрогенными эффектами, что придает им легкий профиль побочных эффектов и делает их особенно подходящими для использования женщинами и детьми. [7] [14] [15] Существуют метаболиты нандролона, которые действуют в организме как пролекарства длительного действия [7], такие как 5α-дигидронандролон .
Сложные эфиры нандролона были впервые описаны и представлены для медицинского применения в конце 1950-х годов. [7] Они являются одними из наиболее широко используемых ААС во всем мире. [7] В дополнение к их медицинскому применению, эфиры нандролона используются для улучшения телосложения и работоспособности и считаются наиболее широко используемыми ААС для таких целей. [7] [16] Во многих странах наркотики являются контролируемыми веществами, поэтому немедицинское использование, как правило, является незаконным. [7]
Медицинское использование [ править ]
Сложные эфиры нандролона используются клинически, хотя все реже, для людей в катаболических состояниях с сильными ожогами, раком и СПИДом, и офтальмологический состав был доступен для поддержки заживления роговицы. [17] : 134
Положительные эффекты эфиров нандролона включают рост мышц, стимуляцию аппетита и увеличение производства красных кровяных телец , [ необходима медицинская ссылка ] и плотность костей . [18] Клинические исследования показали, что они эффективны при лечении анемии , остеопороза и рака груди .
Сульфат нандролона использовался в составе глазных капель в качестве офтальмологического лекарства. [2] [11]
Немедицинское использование [ править ]
Нандролона эфиры используются для physique- и целей , улучшающих по конкурентным спортсменов , культуристов и пауэрлифтеров . [7]
Побочные эффекты [ править ]
Побочные эффекты эфиров нандролона включают, среди прочего, маскулинизацию . [7] У женщин нандролон и сложные эфиры нандролона вызывают повышение либидо , акне , рост волос на лице и теле , изменение голоса и увеличение клитора . [19] Однако, как сообщается, маскулинизирующий эффект нандролона и его эфиров слабее, чем у тестостерона . [19] Нандролон также вызывает рост полового члена у мальчиков препубертатного возраста. [19] Аменорея и меноррагия были зарегистрированы как побочные эффекты нандролона ципионата . [19]
Теоретически нандролон может вызывать эректильную дисфункцию как побочный эффект, хотя в настоящее время нет клинических доказательств, подтверждающих это мнение. [20] Побочные эффекты высоких доз нандролона могут включать сердечно-сосудистую токсичность, а также гипогонадизм и бесплодие . [ необходима цитата ] Нандролон не может вызывать выпадение волос на коже головы , хотя это тоже теоретически. [20]
Фармакология [ править ]
Фармакодинамика [ править ]
| Медикамент | Соотношение а |
|---|---|
| Тестостерон | ~ 1: 1 |
| Андростанолон ( ДГТ ) | ~ 1: 1 |
| Метилтестостерон | ~ 1: 1 |
| Метандриол | ~ 1: 1 |
| Флуоксиместерон | 1: 1–1: 15 |
| Метандиенон | 1: 1–1: 8 |
| Дростанолон | 1: 3–1: 4 |
| Метенолон | 1: 2–1: 30 |
| Оксиметолон | 1: 2–1: 9 |
| Оксандролон | 1: 3–1: 13 |
| Станозолол | 1: 1–1: 30 |
| Нандролон | 1: 3–1: 16 |
| Этилэстренол | 1: 2–1: 19 |
| Норетандролон | 1: 1–1: 20 |
| Примечания: У грызунов. Сноски: а = отношение андрогенной активности к анаболической. Источники: см. Шаблон. | |
Нандролон является агонистом в АРЕ, биологическая мишень из андрогенов , таких как тестостерон и дигидротестостерон . В отличие от тестостерона и некоторых других ААС, нандролон не усиливал в андрогенных тканях , таких как головы , кожи и простаты , поэтому вредные эффекты в этих тканях уменьшается. [21] Это связано с тем, что нандролон метаболизируется 5α-редуктазой в гораздо более слабый лиганд AR 5α-дигидронандролон (DHN), который имеет пониженное сродство к рецептору андрогенов (AR) по сравнению с нандролоном.in vitro и более слабая агонистическая активность AR in vivo . [21] Отсутствие алкилирования на 17α-углероде резко снижает гепатотоксический потенциал нандролона. [ необходима медицинская цитата ] Эффекты эстрогена, возникающие в результате реакции с ароматазой , также уменьшаются из-за уменьшения взаимодействия ферментов [22], но такие эффекты, как гинекомастия и снижение либидо, могут все же возникать при достаточно высоких дозах. [ необходима цитата ]
Помимо своей агонистической активности против AR, в отличие от многих других AAS, нандролон также является мощным гестагеном . [23] Он связывается с рецептором прогестерона примерно с 22% сродства прогестерона . [23] Прогестагенная активность нандролона усиливает его антигонадотропные эффекты [24] [7], поскольку антигонадотропное действие является известным свойством прогестагенов. [25] [26]
| Сложный | PR | AR | ER | GR | МИСТЕР | ГСПГ | CBG |
|---|---|---|---|---|---|---|---|
| Нандролон | 20 | 154–155 | <0,1 | 0,5 | 1.6 | 1–16 | 0,1 |
| Тестостерон | 1.0–1.2 | 100 | <0,1 | 0,17 | 0,9 | 19–82 | 3–8 |
| Эстрадиол | 2,6 | 7.9 | 100 | 0,6 | 0,13 | 8,7–12 | <0,1 |
| Примечания: Значения даны в процентах (%). Контрольными лигандами (100%) были прогестерон для PR , тестостерон для AR , эстрадиол для ER , дексаметазон для GR , альдостерон для MR , дигидротестостерон для SHBG и кортизол для CBG . Источники: см. Шаблон. | |||||||
Анаболическая и андрогенная активность [ править ]
Нандролон имеет очень высокое соотношение анаболической и андрогенной активности. [14] Фактически, нандролоноподобные ААС, такие как сам нандролон и тренболон , обладают одним из самых высоких соотношений анаболического и андрогенного действия среди всех ААС. [24] Это объясняется тем фактом, что в то время как тестостерон усиливается за счет преобразования в дигидротестостерон (ДГТ) в андрогенных тканях, обратное верно для нандролона и подобных ААС (т.е. других производных 19-нортестостерона). [14] Таким образом, нандролоноподобные ААС, а именно сложные эфиры нандролона, являются наиболее часто используемыми ААС в клинических условиях, в которых желательны анаболические эффекты; например, при лечении СПИД- ассоциированныхкахексия , сильные ожоги и хроническая обструктивная болезнь легких . [24] Однако ААС с очень высоким соотношением анаболического и андрогенного действия, такие как нандролон, по-прежнему обладают значительными андрогенными эффектами и могут вызывать симптомы маскулинизации, такие как гирсутизм и снижение голоса у женщин и детей при длительном применении. [14]
| Сложный | rAR (%) | час (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| Тестостерон | 38 | 38 | ||||||
| 5α-дигидротестостерон | 77 | 100 | ||||||
| Нандролон | 75 | 92 | ||||||
| 5α-дигидронандролон | 35 год | 50 | ||||||
| Этилэстренол | ND | 2 | ||||||
| Норетандролон | ND | 22 | ||||||
| 5α-дигидроноретандролон | ND | 14 | ||||||
| Метриболон | 100 | 110 | ||||||
| Источники: см. Шаблон. | ||||||||
Фармакокинетика [ править ]
Изучена пероральная активность нандролона. [27] [28] [29] [30] [31] [32] С пероральным введением нандролона у грызунов, это было около одной десятой потенции из подкожной инъекции нандролона. [27] [33] [19]
Нандролон имеет очень низкое сродство к глобулину, связывающему половые гормоны сыворотки крови человека (SHBG), около 5% от сродства тестостерона и 1% от DHT. [34] Он метаболизируется с помощью фермента 5 -редуктазы , среди других. [35] [ требуется дополнительное цитирование ] Нандролон менее подвержен метаболизму 5α-редуктазой и 17β-гидроксистероиддегидрогеназой, чем тестостерон . [35] Это приводит к тому, что он меньше трансформируется в так называемых «андрогенных» тканях, таких как кожа , волосяные фолликулы., и предстательной железе и в почках соответственно. [35] Метаболиты нандролона включают 5α-дигидронандролон , 19-норандростерон и 19-норэтиохоланолон , и эти метаболиты могут быть обнаружены в моче . [36]
Было обнаружено, что однократные внутримышечные инъекции 100 мг нандролона фенилпропионата или нандролона деканоата вызывают анаболический эффект в течение 10–14 дней и 20–25 дней соответственно. [37] И наоборот, неэтерифицированный нандролон использовался внутримышечно один раз в день. [19] [33]
- Уровни гормонов с эфирами нандролона при внутримышечной инъекции
Уровни нандролона после однократной внутримышечной инъекции 50, 100 или 150 мг нандролона деканоата в масляном растворе у мужчин. [38]
Уровни нандролона после однократной внутримышечной инъекции 100 мг нандролона деканоата или нандролона фенилпропионата в 4 мл или 1 мл раствора арахисового масла в ягодичную или дельтовидную мышцу у мужчин. [39]
Уровни нандролона при однократной внутримышечной инъекции 50 мг нандролона деканоата или нандролона гексилоксифенилпропионата в масляном растворе у мужчин. [40]
Нормализованная по дозе экспозиция нандролона (уровень в сыворотке, разделенная на введенную дозу) с нандролона деканоатом в масляном растворе путем внутримышечной или подкожной инъекции у мужчин. [41] [42]
Химия [ править ]
Нандролон, также известный как 19-нортестостерон (19-NT) или как эстренолон, а также эстра-4-ен-17β-ол-3-он или 19-норандрост-4-ен-17β-ол-3-он, [43] является естественным эстрана (19-норандростан) стероида и производного от тестостерона (андрост-4-ен-17β-ол-3-он). [2] [11] Это, в частности, деметилированный ( нор ) C19 аналог тестостерона. [2] [11] нандролон является эндогенным промежуточным в производстве из эстрадиола из тестостероначерез ароматазу у млекопитающих, включая человека, и присутствует в организме естественным образом в следовых количествах. [44] Его можно обнаружить во время беременности у женщин. [45] Сложные эфиры нандролона имеют сложный эфир, такой как деканоат или фенилпропионат, присоединенный в положении C17β. [2] [11]
Производные [ править ]
Эфиры [ править ]
Разнообразные сложные эфиры нандролона продаются и используются в медицине. [2] [11] Наиболее часто используемые сложные эфиры - это деканоат нандролона и, в меньшей степени, фенилпропионат нандролона . Примеры других сложных эфиров нандролона, которые были проданы и использованы в медицине, включают нандролон циклогексилпропионат , нандролон ципионат , нандролон гексилоксифенилпропионат , нандролона лаурат , нандролон сульфат и нандролона ундеканоат . [2] [11] [7]
Анаболические стероиды [ править ]
Нандролон является исходным соединением большой группы ААС. Известные примеры включают в себя не-17 & alpha; алкилирует тренболон и 17 & alpha; алкилирует этилэстренол (ethylnandrol) и metribolone (R-1881), а также 17 & alpha; алкилирует дизайнер стероиды norboletone и tetrahydrogestrinone (ГТГ). Ниже приводится список производных нандролона, которые были разработаны как ААС: [7]
|
|
Прогестины [ править ]
Нандролон вместе с этистероном (17α-этинилтестостероном) также является исходным соединением большой группы прогестинов , производных норэтистерона (17α-этинил-19-нортестостерон). [46] [47] Это семейство подразделяется на две группы: эстраны и гонаны . [46] В estranes включает норэтистерон (норэтиндрон), норэтистерон ацетат , норэтистерон энантат , линестренол , etynodiol диацетат и noretynodrel , в то время как gonanes включают норгестрел ,левоноргестрел , дезогестрел , этоногестрел , гестоден , норгестимат , диеногест (на самом деле производное 17α-цианометил-19-нортестостерона) и норэлгестромин . [46]
Синтез [ править ]
Разработка AJ Birch метода восстановления ароматических колец до соответствующих дигидробензолов в контролируемых условиях открыла удобный путь к соединениям, родственным предполагаемому 19-норпрогестерону .
Эта реакция, теперь известен как сокращения Birch , [51] типична для лечения монометилового эфира эстрадиола ( 1 ) с раствором металлического лития в жидком аммиаке в присутствии спирта в качестве источника протонов. Составляющие исходной реакции 1,4-диметалирования наиболее электронодефицитных положений ароматического кольца - в случае эстрогена положения 1 и 4. Rxn промежуточного продукта с источником протонов приводит к дигидробензолу; Особым достоинством этой последовательности в стероидах является тот факт, что двойное связывание в точке 2 фактически превращается в фрагмент енольного эфира. Обработка этого продукта ( 2 ) слабой кислотой, щавелевой кислотойнапример, приводит к гидролизу енольного эфира с образованием β, γ-неконъюгированного кетона 3 . Гидролиз в более тяжелых условиях ( минеральные кислоты ) приводит к миграции / конъюгации олефина с образованием нандролона ( 4 ).
Эфиры [ править ]
- Обработка 4 декановым ангидридом и пиридином дает деканоат нандролона . [52]
- Ацилирование 4 фенилпропионилхлоридом дает фенпропионат нандролона . [53]
Обнаружение в биологических жидкостях [ править ]
Использование нандролона непосредственно обнаруживается в волосах или косвенно в моче при тестировании на наличие 19-норандростерона , метаболита . Международный олимпийский комитет установил предел 2,0 мкг / л 19-норандростерон в моче как верхний предел, [54] , за которой спортсмен подозревается в легировании . В крупнейшем исследовании нандролона, проведенном с участием 621 спортсмена на Олимпийских играх 1998 года в Нагано , ни один спортсмен не тестировал более 0,4 мкг / л. 19-Норандростерон был идентифицирован как следовое загрязнение в коммерческих препаратах андростендиона , которые до 2004 года продавались без рецепта в качестве пищевой добавки в США.[55] [56] [57] [58]
В 1999 году произошло несколько случаев заражения нандролоном в легкой атлетике , среди которых были такие известные спортсмены, как Мерлен Отти , Дитер Бауман и Линфорд Кристи . [59] Однако в следующем году метод определения нандролона в то время оказался ошибочным. Марк Ричардсон , британский олимпийский эстафетный бегун, у которого был положительный результат теста на это вещество, сдал значительное количество образцов мочи в контролируемой среде и дал положительный результат теста на лекарство, продемонстрировав возможность ложных срабатываний, что привело к пересмотру его конкурентоспособной запретить. [60]
Чрезмерное потребление незаменимой аминокислоты лизина (как указано при лечении герпеса) якобы показало ложноположительные результаты у некоторых и было названо американским шприцем С. Дж. Хантером причиной положительного результата теста, хотя в 2004 году он признался в федеральном суде. жюри, что он вводил нандролон. [61] Возможной причиной неверных результатов анализа мочи является присутствие метаболитов из других ААС, хотя современный анализ мочи обычно позволяет определить точный используемый ААС, анализируя соотношение двух оставшихся метаболитов нандролона. В результате многочисленных отмененных вердиктов процедура тестирования была пересмотрена UK Sport.. 5 октября 2007 года трехкратная олимпийская чемпионка по легкой атлетике Мэрион Джонс призналась в употреблении наркотика и в 2000 году была приговорена к шести месяцам тюремного заключения за ложь перед федеральным большим жюри [62].
Масс-спектрометрия также используется для обнаружения небольших образцов нандролона в образцах мочи, поскольку он имеет уникальную молярную массу.
История [ править ]
Нандролон был впервые синтезирован в 1950 году. [2] [43] [17] : 130 [63] Он был впервые представлен как фенилпропионат нандролона в 1959 году, а затем как деканоат нандролона в 1962 году, за которым последовали дополнительные эфиры. [64]
Общество и культура [ править ]
Общие имена [ править ]
Нандролон - это общее название препарата и его МНН , БАН , DCF и DCIT . [2] [11] [3] [65] Официальные общие названия сложных эфиров нандролона включают нандролонциклогексилпропионат ( BANM ), нандролонциклотат ( USAN ), нандролон деканоат ( USAN , USP , BANM , JAN ), нандролона лаурат ( BANM ), фенпропионат нандролона (USP ) и фенилпропионат нандролона ( BANM , JAN ). [2] [11] [3] [65]
Допинг в спорте [ править ]
Нандролон, вероятно, был одним из первых ААС, который использовался в качестве допингового агента в спорте в 1960-х годах. Он был запрещен на Олимпийских играх с 1974 года. [17] : 128 Известно много случаев применения допинга в спорте с использованием эфиров нандролона профессиональными спортсменами .
Исследование [ править ]
Эфиры нандролона изучались по нескольким показаниям. Они интенсивно изучались на предмет остеопороза , увеличения поглощения кальция и снижения потери костной массы, но вызывали вирилизацию примерно у половины женщин, принимавших их, и в большинстве случаев отказались от этого применения, когда стали доступны более эффективные препараты, такие как бисфосфонаты . [20] Они также изучались в клинических испытаниях при хронической почечной недостаточности , апластической анемии и в качестве мужских контрацептивов . [17] : 134
Ссылки [ править ]
- ^ «Значение нандролона в Кембриджском словаре английского языка» .
- ^ a b c d e f g h i j k l m n o Elks J, Ganellin CR, eds. (2014). Словарь лекарств: химические данные: химические данные, структуры и библиографии . Нью-Йорк: Спрингер. С. 660–. ISBN 978-1-4757-2085-3. OCLC 1079003025 .
- ^ a b c d Мортон И.К., Холл Дж. М. (6 декабря 2012 г.). Краткий словарь фармакологических агентов: свойства и синонимы . Springer Science & Business Media. ISBN 978-94-011-4439-1.
- ^ МакЭвой JD, Маквей CE, McCaughey WJ (декабрь 1998). «Остатки эфиров нортестостерона в местах инъекций. Часть 1. Биодоступность при пероральном введении». Аналитик . 123 (12): 2475–8. DOI : 10.1039 / a804919j . PMID 10435281 .
- ^ Becker KL (2001). Принципы и практика эндокринологии и обмена веществ . Липпинкотт Уильямс и Уилкинс. С. 1185–. ISBN 978-0-7817-1750-2.
- ^ a b c d e f g "Дека-дураболин" (PDF) . Шеринг-Плау . Архивировано из оригинального (PDF) 18 декабря 2010 года.
- ^ Б с д е е г ч я J к л м п о р Q R сек т Ллевеллин W (2011). Анаболики . Molecular Nutrition Llc. С. 402–412, 460–467, 193–194. ISBN 978-0-9828280-1-4.
- ^ a b Thomas JA (6 декабря 2012 г.). Наркотики, спортсмены и физическая подготовка . Springer Science & Business Media. С. 27–29. ISBN 978-1-4684-5499-4.
- ^ a b c Minto CF, Howe C, Wishart S, Conway AJ, Handelsman DJ (апрель 1997 г.). «Фармакокинетика и фармакодинамика эфиров нандролона в масляном носителе: влияние сложного эфира, места инъекции и объема инъекции». Журнал фармакологии и экспериментальной терапии . 281 (1): 93–102. PMID 9103484 .
- ^ "Дека-дураболин" (PDF) . Merck Sharp & Dohme (Австралия) .
- ^ a b c d e f g h i Номинальный индекс 2000: Международный справочник по лекарственным средствам . Тейлор и Фрэнсис. Январь 2000. С. 716–. ISBN 978-3-88763-075-1.
- ^ a b Sneader W (23 июня 2005 г.). Открытие наркотиков: история . Джон Вили и сыновья. С. 206–. ISBN 978-0-471-89979-2.
- Перейти ↑ Singh GK, Turner L, Desai R, Jimenez M, Handelsman DJ (июль 2014 г.). «Фармакокинетико-фармакодинамическое исследование подкожной инъекции депо деканоата нандролона с использованием проб сухих пятен крови в сочетании с тандемными масс-спектрометрическими анализами жидкостной хроматографии при сверхвысоком давлении» . Журнал клинической эндокринологии и метаболизма . 99 (7): 2592–8. DOI : 10.1210 / jc.2014-1243 . PMID 24684468 .
- ^ a b c d e Кичман А.Т. (июнь 2008 г.). «Фармакология анаболических стероидов» . Британский журнал фармакологии . 154 (3): 502–21. DOI : 10.1038 / bjp.2008.165 . PMC 2439524 . PMID 18500378 .
- ^ Kochakian CD (6 декабря 2012). Анаболически-андрогенные стероиды . Springer Science & Business Media. С. 401–. ISBN 978-3-642-66353-6.
- ^ Jameson JL, Де Гроот LJ (25 февраля 2015). Эндокринология: электронная книга для взрослых и детей . Elsevier Health Sciences. С. 2388–. ISBN 978-0-323-32195-2.
- ^ а б в г Хеммерсбах П., Große J (2009). «Нандролон: многогранный допинговый агент». В Thieme D, Hemmersbach P (ред.). Допинг в спорте . Берлин: Springer. С. 127–154. ISBN 978-3-540-79088-4.
- ^ Handelsman DJ (2013). «Физиология андрогенов, фармакология и злоупотребления» . В Де Гроот LJ (ред.). Эндотекст . 4.1.2 Фармакологическая андрогенная терапия - через книжную полку NCBI.
И тестостерон, и его неароматизируемое производное нандролон вызывают повышенную плотность костей у мужчин с остеопорозом, вызванным глюкокортикоидами, с минимальными краткосрочными побочными эффектами.
- ^ a b c d e f Camerino B, Sala G (1960). "Анаболические стероиды". Fortschritte der Arzneimittelforschung / Progress in Drug Research / Progrès des recherches Pharmaceutiques . Fortschritte der Arzneimittelforschung. Прогресс в исследованиях лекарств. Progres des Recherches Pharmaceutiques . 2 . С. 71–134. DOI : 10.1007 / 978-3-0348-7038-2_2 . ISBN 978-3-0348-7040-5. PMID 14448579 .
- ^ a b c Пан М.М., Ковач-младший (апрель 2016 г.). «Помимо тестостерона ципионата: доказательства использования нандролона для улучшения мужского здоровья и благополучия» . Трансляционная андрология и урология . 5 (2): 213–9. DOI : 10,21037 / tau.2016.03.03 . PMC 4837307 . PMID 27141449 .
- ^ a b Бергинк EW, Janssen PS, Turpijn EW, van der Vies J (июнь 1985). «Сравнение рецепторных связывающих свойств нандролона и тестостерона в условиях in vitro и in vivo». Журнал стероидной биохимии . 22 (6): 831–6. DOI : 10.1016 / 0022-4731 (85) 90293-6 . PMID 4021486 .
- ^ Brueggemeier RW (16 сентября 2006). «Половые гормоны (мужские): аналоги и антагонисты». В Мейерс Р.А. (ред.). Энциклопедия молекулярной клеточной биологии и молекулярной медицины (аннотация). Джон Вили и сыновья . DOI : 10.1002 / 3527600906.mcb.200500066 . ISBN 978-3527600908.
- ^ a b Kuhl H (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние разных путей введения». Климактерический . 8 Дополнение 1: 3–63. DOI : 10.1080 / 13697130500148875 . PMID 16112947 . S2CID 24616324 .
- ^ a b c de Souza GL, Hallak J (декабрь 2011 г.). «Анаболические стероиды и мужское бесплодие: всесторонний обзор» . BJU International . 108 (11): 1860–5. DOI : 10.1111 / j.1464-410X.2011.10131.x . PMID 21682835 . S2CID 29035729 .
- ^ Couzinet B, Young J, Brailly S, Шансон P, Томас JL, Schaison G (декабрь 1996). «Антигонадотропная активность прогестинов (производных 19-нортестостерона и 19-норпрогестерона) не опосредуется через рецептор андрогенов» . Журнал клинической эндокринологии и метаболизма . 81 (12): 4218–23. DOI : 10,1210 / jcem.81.12.8954018 . PMID 8954018 .
- ^ Мове-Джарвис, П. «Прогестерон и прогестины: общий обзор». (1983): 1-16.
- ^ a b Camerino B, Sciaky R (1975). «Состав и эффекты анаболических стероидов». Фармакология и терапия. Часть B . 1 (2): 233–75. DOI : 10.1016 / 0306-039X (75) 90007-0 . PMID 817322 .
- ^ Хольткамп DE, Heming AE, Мансор LF (1955). «Сравнение перорального и подкожного введения в анаболической и андрогенной эффективности 19-нортестостерона и тестостерона». Журнал клинической эндокринологии и метаболизма . 15 (7): 848. DOI : 10,1210 / jcem-15-7-834 . ISSN 0021-972X .
- ^ Фурман RH, Говард Р., Смит CW, Норсиа LN (январь 1956). «Сравнение эффектов перорального метилтестостерона, 19-нортестостерона и 17-метил-19-нортестостерона на липиды и липопротеины сыворотки» . Журнал лабораторной и клинической медицины . 48 (5): 808–809.
- ^ Фурман RH, Говард RP, Норсиа LN, Keaty EC (январь 1958). «Влияние андрогенов, эстрогенов и родственных стероидов на липиды и липопротеины сыворотки». Американский журнал медицины . 24 (1): 80–97. DOI : 10.1016 / 0002-9343 (58) 90364-4 . PMID 13498038 .
- ^ МакЭвой JD, Маквей CE, McCaughey WJ (декабрь 1998). «Остатки эфиров нортестостерона в местах инъекций. Часть 1. Биодоступность при пероральном введении». Аналитик . 123 (12): 2475–8. DOI : 10.1039 / a804919j . PMID 10435281 .
- Перейти ↑ Arnold A, Potts GO (январь 1964). «Устные анаболические и андрогенные эффекты 19-нортестостерона и 17α-метил-19-нортестостерона» . Труды Федерации . 23 (2): 412.
- ^ a b Baker WH, Henneman PH, Baggett B, Engel LL, Tibbetts D, Brown M (январь 1955 г.). «Метаболический эффект 19-нортестостерона» . Журнал клинической эндокринологии и метаболизма . 15 (7): 848–849. DOI : 10,1210 / jcem-15-7-834 . ISSN 0021-972X .
- ^ Saartok T, Дахлберг E, Густафссон JA (июнь 1984). «Относительное сродство связывания анаболических андрогенных стероидов: сравнение связывания с рецепторами андрогенов в скелетных мышцах и простате, а также с глобулином, связывающим половые гормоны». Эндокринология . 114 (6): 2100–6. DOI : 10,1210 / эндо-114-6-2100 . PMID 6539197 .
- ^ a b c Бергинк EW, Гилен JA, Turpijn EW (1985). «Метаболизм и связывание рецепторов нандролона и тестостерона в условиях in vitro и in vivo». Acta Endocrinologica. Дополнение . 271 (3_Suppla): 31–7. DOI : 10.1530 / acta.0.109S0031 . PMID 3865479 .
- ^ Mottram DR (12 ноября 2010). Наркотики в спорте . Рутледж. С. 63–. ISBN 978-1-135-25825-2.
- ↑ Dorfman RI (5 декабря 2016 г.). Стероидная активность у экспериментальных животных и человека . Elsevier Science. С. 68–. ISBN 978-1-4832-7300-6.
- ^ Bagchus WM, Смитс JM, Verheul HA, De Jager-Van Der Veen SM, Порт A, Geurts TB (2005). «Фармакокинетическая оценка трех различных внутримышечных доз деканоата нандролона: анализ образцов сыворотки и мочи у здоровых мужчин». J. Clin. Эндокринол. Метаб . 90 (5): 2624–30. DOI : 10.1210 / jc.2004-1526 . PMID 15713722 .
- ^ Минто CF, Howe C, Wishart S, Conway AJ, Handelsman DJ (1997). «Фармакокинетика и фармакодинамика эфиров нандролона в масляном носителе: влияние сложного эфира, места инъекции и объема инъекции». J. Pharmacol. Exp. Ther . 281 (1): 93–102. PMID 9103484 .
- ^ Belkien л, Schürmeyer Т, Hano Р, Гуннарссон ПО, Nieschlag Е (май 1985 г.). «Фармакокинетика эфиров 19-нортестостерона у нормальных мужчин». J. Steroid Biochem . 22 (5): 623–9. DOI : 10.1016 / 0022-4731 (85) 90215-8 . PMID 4010287 .
- ^ Kalicharan RW, Schot Р, Vromans Н (февраль 2016). «Фундаментальные представления о абсорбции лекарств из парентерального масляного депо». Eur J Pharm Sci . 83 : 19–27. DOI : 10.1016 / j.ejps.2015.12.011 . PMID 26690043 .
- ^ Kalicharan, Raween Wikesh (2017). Новые взгляды на абсорбцию лекарств из нефтебаз (тезис). Утрехтский университет.
- ^ a b Schnitzer R (1 января 1967 г.). Экспериментальная химиотерапия . Elsevier Science. С. 165–. ISBN 978-0-323-14611-1.
- ^ Bricout V, Райт F (июнь 2004). «Обновленная информация о нандролоне и норстероидах: насколько эти вещества являются эндогенными или ксенобиотическими?». Европейский журнал прикладной физиологии . 92 (1–2): 1–12. DOI : 10.1007 / s00421-004-1051-3 . PMID 15042372 . S2CID 6472015 .
- Перейти ↑ Lippi G, Franchini M, Banfi G (май 2011 г.). «Биохимия и физиология допинга анаболических андрогенных стероидов» . Миниобзоры по медицинской химии . 11 (5): 362–73. DOI : 10.2174 / 138955711795445952 . PMID 21443514 . S2CID 3862299 .
- ^ a b c Шиндлер AE, Campagnoli C, Druckmann R, Huber J, Pasqualini JR, Schweppe KW, Thijssen JH (декабрь 2003 г.). «Классификация и фармакология прогестинов». Maturitas . 46 Приложение 1: S7 – S16. DOI : 10.1016 / j.maturitas.2003.09.014 . PMID 14670641 .
- ^ Meikle AW (24 апреля 2003). Эндокринная заместительная терапия в клинической практике . Springer Science & Business Media. С. 489–. ISBN 978-1-59259-375-0.
Estranes. Прогестагены эстрана и гонана являются производными 19-нортестостерона, гестагенного исходного соединения, используемого в оральных контрацептивах в США. Эстраны характеризуются наличием этинильной группы в положении 17 и отсутствием метильной группы между кольцами A и B (см. Рис. 10). Эстрановые прогестагены, которые структурно связаны с норэтиндроном (норэтинодрел, линестренол, норэтиндронацетат, этинодиолдиацетат), превращаются в это исходное соединение. Норэтиндрон является вторым наиболее часто используемым прогестагеном в Соединенных Штатах для ЗГТ. Гонаны. Гонаны разделяют структурные модификации, обнаруженные в эстранах, а также обладают этинильной группой в положении 13 и кетогруппой в положении 3 (см. Фиг. 11). Норгестрел был синтезирован в 1963 году и представляет собой рацемическую смесь правовращающей и левовращающей форм.Левоноргестрел, левовращающая форма, обеспечивает биологическую активность. Гонаны третьего поколения (дезогестрел, гестоден и норгестимат) были разработаны для уменьшения нежелательных побочных эффектов прогестагенов, [...]
- ^ Уайлдс А.Л., Нельсон Н.А. (1953). «Легкий синтез 19-нортестостерона и 19-норандростендиона из эстрона». Журнал Американского химического общества . 75 (21): 5366–5369. DOI : 10.1021 / ja01117a065 .
- ^ Ueberwasser Н, Гейслер К, Kalvoda Дж, Meystre СН, Wieland , Р, О Anner, Веттштайн А (1963). "19-Norsteroide II. Ein einfaches Herstellungsverfahren für 19-Norandrostan-Derivate. Über Steroide, 193. Mitteilung". Helvetica Chimica Acta . 46 : 344–352. DOI : 10.1002 / hlca.19630460135 .
- ↑ Симидзу I, Наито Y, Цудзи J (1980). «Синтез оптически активного (+) - 19-нортестостерона путем асимметричной реакции бис-аннулирования». Буквы тетраэдра . 21 (5): 487–490. DOI : 10.1016 / S0040-4039 (00) 71440-7 .
- ^ Birch AJ (1950). «Восстановление органических соединений металл-аммиачными растворами». Ежеквартальные обзоры, Химическое общество . 4 : 69. DOI : 10.1039 / QR9500400069 .
- ^ США 2998423 , DeWytt ED, Overbeek O, Overbeek Г.А., выданный в 1961 году, назначен Organon .
- ^ СН 206119 , выданный в 1939 году, назначен Gesellschaft für Industrie Chemische Базель
- ^ «Разъяснение по поводу тестирования нандролона» . Всемирное антидопинговое агентство. 2005-05-30. Архивировано из оригинала на 2012-09-15 . Проверено 31 января 2012 .
- ^ Брессон M, Cirimele V, Villain M, Кинц P (май 2006). «Допинг-контроль метандиенона с использованием волос, анализируемых методом газовой хроматографии-тандемной масс-спектрометрии». Журнал хроматографии. B, Аналитические технологии в биомедицине и науках о жизни . 836 (1–2): 124–8. DOI : 10.1016 / j.jchromb.2006.03.040 . PMID 16597518 .
- ^ Уэки М, Ikekita А, Такао Y (2000). «[Метаболит нандролона в моче олимпийского спортсмена Нагано]». Яп. J. For. Tox. (на японском языке). 18 : 198–199.
- ^ Катлин Д.Х., Ледер Б.З., Аренс Б., Старчевич Б., Хаттон К.К., Грин Г.А., Финкельштейн Дж.С. (2000). «Следы контаминации андростендиона, отпускаемого без рецепта, и положительные результаты анализа мочи на метаболит нандролона» . ДЖАМА . 284 (20): 2618–21. DOI : 10,1001 / jama.284.20.2618 . PMID 11086369 .
- ^ BASELT RC (2008). Удаление токсичных лекарств и химических веществ в человеке (8-е изд.). Фостер-Сити, Калифорния: биомедицинские публикации. С. 1078–1080. ISBN 978-0-9626523-7-0.
- ^ Барон, Питер (2000-09-19). Проблема с наркотиками: Бауманн должен бороться до конца . Дейли телеграф . Проверено 13 ноября 2010.
- ^ Richardson M (2004-02-19). «Легкая атлетика: Марк Ричардсон объясняет, что он чувствовал на своем дисциплинарном слушании» . Легкая атлетика . Лондон: Гардиан . Проверено 13 ноября 2010 .
Это был такой устрашающий состав, с которым я когда-либо сталкивался на легкоатлетических трассах.
- ^ "Следите за тем, чтобы звезда Мэрион Джонс признала употребление стероидов" . Национальное общественное радио. 2007-10-05 . Проверено 9 ноября 2009 .
- ↑ Спортивное антидопинговое управление Великобритании (январь 2000 г.). Обзор нандролона (PDF) (Отчет). Великобритания Спорт . Архивировано из оригинального (PDF) 04.04.2005 . Проверено 2 февраля 2013 .
- ^ Birch AJ (1950). «80. Гидроароматические стероидные гормоны. Часть I. 10-Нортестостерон». Журнал химического общества (возобновленный) : 367. DOI : 10.1039 / jr9500000367 . ISSN 0368-1769 .
- ^ Сводный список продуктов, потребление и / или продажа которых были запрещены, изъяты, строго ограничены или не одобрены правительствами . Публикации Организации Объединенных Наций. 1983. С. 154–. ISBN 978-92-1-130230-1.
- ^ а б «Нандролон» .
Дальнейшее чтение [ править ]
- Geusens P (сентябрь 1995 г.). «Деканоат нандролона: фармакологические свойства и терапевтическое применение при остеопорозе». Клиническая ревматология . 14 Дополнение 3: 32–9. DOI : 10.1007 / bf02210686 . PMID 8846659 . S2CID 24365057 .
- Кичман А.Т. (июнь 2008 г.). «Фармакология анаболических стероидов» . Британский журнал фармакологии . 154 (3): 502–21. DOI : 10.1038 / bjp.2008.165 . PMC 2439524 . PMID 18500378 .
- Хеммерсбах П., Гросс Дж. (2010). «Нандролон: многогранный допинг». Допинг в спорте . Handb Exp Pharmacol . Справочник по экспериментальной фармакологии. 195 . С. 127–54. DOI : 10.1007 / 978-3-540-79088-4_6 . ISBN 978-3-540-79087-7. PMID 20020363 .
- Velema MS, Kwa BH, de Ronde W (март 2012 г.). «Следует ли учитывать андрогенные анаболические стероиды в схеме лечения отдельных пациентов с хронической обструктивной болезнью легких?». Современные взгляды на легочную медицину . 18 (2): 118–24. DOI : 10.1097 / MCP.0b013e32834e9001 . PMID 22189453 . S2CID 6155275 .
- Busardò FP, Frati P, Sanzo MD, Napoletano S, Pinchi E, Zaami S, Fineschi V (январь 2015 г.). «Влияние деканоата нандролона на центральную нервную систему» . Современная нейрофармакология . 13 (1): 122–31. DOI : 10.2174 / 1570159X13666141210225822 . PMC 4462037 . PMID 26074747 .
- Ву С., Ковач-младший (октябрь 2016 г.). «Новое использование анаболических андрогенных стероидов, нандролона и оксандролона в управлении мужским здоровьем». Текущие отчеты урологии . 17 (10): 72. DOI : 10.1007 / s11934-016-0629-8 . PMID 27535042 . S2CID 43199715 .
- Пан М.М., Ковач-младший (апрель 2016 г.). «Помимо тестостерона ципионата: доказательства использования нандролона для улучшения мужского здоровья и благополучия» . Трансляционная андрология и урология . 5 (2): 213–9. DOI : 10,21037 / tau.2016.03.03 . PMC 4837307 . PMID 27141449 .