| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК никелоцен | |||
| Другие имена Бис (циклопентадиенил) никель (II) | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.013.672 | ||
| Номер ЕС |
| ||
| 3412 | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1325 3082 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 10 H 10 Ni | |||
| Молярная масса | 188,88 г / моль | ||
| Внешность | Зеленые кристаллы | ||
| Плотность | 1,47 г / см 3 | ||
| Температура плавления | От 171 до 173 ° C (от 340 до 343 ° F, от 444 до 446 K) | ||
| нерастворимый | |||
| Структура | |||
| Д 5ч , Д 5д | |||
| 0 Д | |||
| Опасности | |||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасность | ||
| H228 , H302 , H317 , H350 | |||
| Р201 , Р202 , Р210 , Р240 , Р241 , Р261 , Р264 , Р270 , P272 , P280 , P281 , P301 + 312 , P302 + 352 , P308 + 313 , P321 , P330 , P333 + 313 , P363 , P370 + 378 , P405 , P501 | |||
| NFPA 704 (огненный алмаз) | |||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 490 мг кг -1 (перорально, крыса) 600 мг кг -1 (перорально, мышь) | ||
| Родственные соединения | |||
Родственные соединения | CoCp 2 , FeCp 2 | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
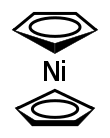
Никелоцен представляет собой никелевоорганическое соединение с формулой Ni ( η 5 -C 5 H 5 ) 2 . Это ярко-зеленое парамагнитное твердое вещество, также известное как бис (циклопентадиенил) никель или NiCp 2 , представляет непреходящий академический интерес [1], хотя пока не имеет известных практических применений.
Структура и связь [ править ]
Ni (C 5 H 5 ) 2 принадлежит к группе металлоорганических соединений, называемых металлоценами . Металлоцены обычно имеют структуру, в которой ион металла расположен между двумя параллельными циклопентадиенильными (Cp) кольцами. В твердом состоянии молекула имеет симметрию D 5d , при этом два кольца расположены в шахматном порядке . [2]
Центр Ni имеет формальный заряд +2, а кольца Cp обычно обозначают как циклопентадиенильные анионы (Cp - ), связанные с циклопентадиеном путем депротонирования. По структуре похож на ферроцен . С точки зрения его электронной структуры, три пары d-электронов на никеле отнесены к трем d-орбиталям, участвующим в связывании Ni – Cp: d xy , d x 2 - y 2 , d z 2 . Два оставшихся d-электрона находятся на орбиталях d yz и d xz , что приводит к парамагнетизму молекулы, что проявляется в необычно сильном полевом химическом сдвиге, наблюдаемом в ее 1 HСпектр ЯМР . Никелоцен с 20 валентными электронами имеет наибольшее количество электронов среди металлоценов переходных металлов. Кобальтоцен Co (C 5 H 5 ) 2 с 19 валентными электронами, однако, является более сильным восстановителем, что свидетельствует о том, что энергия электронов, а не их количество, определяет окислительно-восстановительный потенциал.
Подготовка [ править ]
Никелоцен был впервые получен Э. О. Фишером в 1953 году, вскоре после открытия ферроцена , первого металлоценового соединения. [3] Он был приготовлен в однореакторной реакции путем депротонирования циклопентадиена этилмагнийбромидом и добавления безводного ацетилацетоната никеля (II) . [4] Современный синтез включает обработку безводных источников NiCl 2 (таких как гексаамминеникель хлорид ) циклопентадиенилом натрия : [5]
- [Ni (NH 3 ) 6 ] Cl 2 + 2 NaC 5 H 5 → Ni (C 5 H 5 ) 2 + 2 NaCl + 6 NH 3
Свойства [ править ]
Как и многие металлоорганические соединения, Ni (C 5 H 5 ) 2 не переносит длительного воздействия воздуха до заметного разложения. [6] Образцы обычно обрабатываются безвоздушным способом .
Большинство химических реакций никелоцена характеризуются его тенденцией давать 18-электронные продукты с потерей или модификацией одного Cp-кольца.
- Ni (C 5 H 5 ) 2 + 4 PF 3 → Ni (PF 3 ) 4 + органические продукты
Реакция со вторичными фосфинами происходит по аналогичной схеме:
- 2 Ni (C 5 H 5 ) 2 + 2 PPh 2 H → [Ni 2 (PPh 2 ) 2 (C 5 H 5 ) 2 ] + 2 C 5 H 6
Никелоцен можно окислить до соответствующего катиона, который содержит Ni (III).
Газообразный Ni (C 5 H 5 ) 2 разлагается до никелевого зеркала при контакте с горячей поверхностью, высвобождая углеводородные лиганды в виде газообразных побочных продуктов. Этот процесс рассматривался как средство получения никелевых пленок.
Никелоцен реагирует с азотной кислотой с образованием нитрозила циклопентадиенил никеля , высокотоксичного никелевоорганического соединения.
Ссылки [ править ]
- ^ Elschenbroich, C. (2006). Металлоорганические соединения . Вайнхайм: Wiley-VCH. ISBN 978-3-527-29390-2.
- ^ П. Зайлер; Дж. Д. Дуниц (1980). «Структура никелоцена при комнатной температуре и 101 К». Acta Crystallogr . B36 : 2255–2260. DOI : 10.1107 / S0567740880008539 .
- ^ Фишер, EO; Пфаб, В. (1952). "Zur Kristallstruktur der Di-Cyclopentadienyl-Verbindungen des zweiwertigen Eisens, Kobalts und Nickels" [О кристаллической структуре бисциклопентадиенильных соединений двухвалентного железа, кобальта и никеля]. Z. Naturforsch. B . 7 : 377–379.
- ^ Wilkinson, G .; Pauson, PL; Хлопок, FA (1954). «Бис-циклопентадиенильные соединения никеля и кобальта». Варенье. Chem. Soc. 76 (7): 1970–4. DOI : 10.1021 / ja01636a080 .
- ^ Джиролами, GS; Раухфус, ТБ; Angelici, RJ (1999). Синтез и техника в неорганической химии . Милл-Вэлли, Калифорния: Университетские научные книги. ISBN 0935702482.
- ^ Яворска-Августиняк, Анна; Войтчак, Ян (1979). «Комплексы с переносом заряда кобальтоцена и никелоцена с тетрахлорметаном». Monatshefte für Chemie . 110 (5): 1113–1121. DOI : 10.1007 / BF00910959 .
Внешние ссылки [ править ]
- Монография МАИР «Никель и никелевые соединения»
- Национальный реестр загрязнителей - Информационный бюллетень по никелю и соединениям