
Нитрозо относится к функциональной группе в органической химии, в которой группа NO присоединена к органическому фрагменту . Таким образом, различные нитрозогруппы могут быть классифицированы как C- нитрозосоединения (например, нитрозоалканы; R-N = O), S- нитрозосоединения ( нитрозотиолы ; RS-N = O), N- нитрозосоединения (например, нитрозамины , R 1 N (-R 2 ) -N = O) и O -нитрозосоединения ( алкилнитриты ; RO-N = O).
Синтез [ править ]
Нитрозосоединения можно получить восстановлением нитросоединений [1] или окислением гидроксиламинов . [2] Орто-нитрозофенолы могут быть получены по реакции Баудиша . В перегруппировке Фишера – Хеппа ароматические 4-нитрозоанилины получают из соответствующих нитрозаминов .
Свойства [ править ]
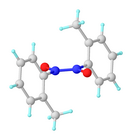
Нитрозоарены обычно участвуют в равновесии мономер-димер. Димеры, которые часто имеют бледно-желтый цвет, часто предпочтительны в твердом состоянии, тогда как темно-зеленые мономеры предпочтительны в разбавленном растворе или при более высоких температурах. Они существуют как цис- и транс- изомеры. [4]
Из-за стабильности свободных радикалов оксида азота нитрозоорганилы имеют тенденцию иметь очень низкую энергию диссоциации связи C – N: нитрозоалканы содержат БДЭ порядка 30-40 ккал / моль, а нитрозоарены содержат БДЭ порядка 50-60. ккал / моль. Как следствие, они обычно чувствительны к теплу и свету. Соединения, содержащие связи O– (NO) или N– (NO), обычно имеют даже более низкие энергии диссоциации связи. Например, N- нитрозодифениламин Ph 2 N – N = O имеет энергию диссоциации связи N – N всего 23 ккал / моль. [5] Нитрозоорганические соединения служат лигандами для переходных металлов. [6]
Реакции [ править ]
Многая реакция существует , которые делают использование промежуточного нитрозо соединения, такие как реакция Barton и реакция Дэвиса-Бейрут , а также в синтезе индолов , например: Байер-Emmerling синтеза индолов , Бартоль индол синтез . В реакции Сэвилля ртуть используется для замены нитрозила из тиоловой группы.
Нитрозирование против нитрозилирования [ править ]
Нитрит может вступать в реакции двух типов в зависимости от физико-химической среды.
- Нитрозилирование представляет собой добавление нитрозильного иона NO - к металлу (например, железу) или тиолу, что приводит к нитрозильному железу Fe – NO (например, в нитрозилированном геме = нитрозилгеме) или S- нитрозотиолам (RSNO).
- Нитрозирование - это добавление иона нитрозония NO + к амину –NH 2, что приводит к нитрозамину . Это преобразование происходит при кислом pH, особенно в желудке, как показано в уравнении образования N- фенилнитрозамина:
- НЕТ-
2+ H + ⇌ HONO - HONO + H + ⇌ H 2 O + NO +
- C 6 H 5 NH 2 + NO + → C 6 H 5 N (H) NO + H +
- НЕТ-
Многие первичные алкил- N- нитрозосоединения, такие как CH 3 N (H) NO, имеют тенденцию быть нестабильными в отношении гидролиза до спирта. Производные вторичных аминов (например, (CH 3 ) 2 NNO, полученный из диметиламина ) более устойчивы. Именно эти N- нитрозамины являются канцерогенами у грызунов.
Нитрозил в неорганической химии [ править ]
Нитрозилы представляют собой неорганические соединения, содержащие группу NO, например, непосредственно связанные с металлом через атом N, образуя фрагмент металл-NO. Альтернативно, примером неметалла является обычный реагент нитрозилхлорид (Cl-N = O). Оксид азота - стабильный радикал , имеющий неспаренный электрон. Восстановление оксида азота дает анион нитрозила , NO - :
- НЕТ + е - → НЕТ -
Окисление NO дает катион нитрозония NO + :
- НЕТ → НЕТ + + е -
Оксид азота может служить лигандом, образующим нитрозильные комплексы металлов или просто нитрозилы металлов. Эти комплексы можно рассматривать как аддукты NO + , NO - или как некоторый промежуточный случай.
В еде [ править ]
В пищевых продуктах и в желудочно-кишечном тракте нитрозирование и нитрозилирование не имеют таких же последствий для здоровья потребителей.
- В консервированном мясе : Мясо обработанного отверждения содержат нитриты и имеет рН от 5 примерно, где почти всех нитрит присутствует в виде NO-
2(99%). В копченое мясо также добавляют аскорбат натрия (или эриторбат, или витамин С). Как продемонстрировал С. Мирвиш, аскорбат ингибирует нитрозирование аминов до нитрозамина, поскольку аскорбат реагирует с NO.-
2сформировать NO. [7] [8] Аскорбат и pH 5, таким образом, способствуют нитрозилированию гемового железа, образуя нитрозилгем, красный пигмент, когда он входит в состав миоглобина, и розовый пигмент, когда он выделяется при варке. Он вносит свой вклад в «привкус бекона» вяленого мяса: таким образом, нитрозилгем считается преимуществом для мясной промышленности и потребителей. [9] - В желудке : выделяемый хлористый водород создает кислую среду (pH 2), а проглоченный нитрит (с пищей или слюной) приводит к нитрозированию аминов, что приводит к нитрозаминам (потенциальным канцерогенам). Нитрозирование является низким, если концентрация амина низкая (например, диета с низким содержанием белка, отсутствие ферментированной пищи) или если концентрация витамина С высокая (например, диета с высоким содержанием фруктов). Затем образуются S- нитрозотиолы, устойчивые при pH 2.
- В толстой кишке : нейтральный pH не способствует нитрозированию. В стуле не образуется нитрозамин, даже после добавления вторичного амина или нитрита. [10] Нейтральный pH способствует высвобождению NO - из S- нитрозотиолов и нитрозилированию железа. Ранее названные NOC ( N- нитрозосоединения), измеренные командой Бингхэма в стуле добровольцев, питавшихся красным мясом [11], были, согласно Бингхэму и Кунле, в основном не- N- нитрозо ATNC (кажущееся общее количество нитрозосоединений), например S -нитрозотиолы и нитрозильное железо (как нитрозилгем). [12]
См. Также [ править ]
- Нитрозамин , функциональная группа с NO, присоединенным к амину, такая как R 2 N – NO
- Нитрозобензол
- Оксид азота
- Нитроксил
Ссылки [ править ]
- ^ Г. Х. Коулман; CM Макклоски; Ф. А. Стюарт (1945). «Нитрозобензол». Орг. Synth . 25 : 80. DOI : 10,15227 / orgsyn.025.0080 .
- ^ Calder, A .; Forrester, AR; Хепберн, ИП "2-Метил-2-нитрозопропан и его димер" . Органический синтез . 52 : 77.; Коллективный том , 6 , с. 803
- ^ E.Bosch (2014). «Структурный анализ метилзамещенных нитрозобензолов и нитрозоанизолов» . J. Chem. Cryst . 98 (2): 44. DOI : 10.1007 / s10870-013-0489-8 . S2CID 95291018 .
- ^ Beaudoin, D .; Wuest, JD (2016). «Димеризация ароматических C-нитрозосоединений». Химические обзоры . 116 (1): 258–286. DOI : 10.1021 / cr500520s . PMID 26730505 .
- Перейти ↑ Luo, Yu-Ran (2007). Всеобъемлющий справочник по энергии химических связей . Бока-Ратон, Флорида: Тейлор и Фрэнсис. ISBN 9781420007282.
- ^ Пилато, RS; McGettigan, C .; Geoffroy, GL; Рейнгольд, AL; Гейб, SJ (1990). " Трет -Butylnitroso комплексов. Структурная характеристика W (CO) 5 (N (O) бу- трет ) и [КЗСС (СО) (PPh 3 ) (N (O) бу- трет )] + ". Металлоорганические соединения . 9 (2): 312–17. DOI : 10.1021 / om00116a004 .
- ^ Мирвиш, СС; Wallcave, L; Иген, М; Шубик П. (июль 1972 г.). «Аскорбат-нитритная реакция: возможные средства блокирования образования канцерогенных N- нитрозосоединений». Наука . 177 (4043): 65–8. Bibcode : 1972Sci ... 177 ... 65M . DOI : 10.1126 / science.177.4043.65 . PMID 5041776 . S2CID 26275960 .
- ^ Мирвиш, SS (октябрь 1986). «Влияние витаминов C и E на образование N- нитрозосоединений, канцерогенез и рак». Рак . 58 (8 Suppl): 1842–50. DOI : 10.1002 / 1097-0142 (19861015) 58: 8+ <1842 :: помощь-cncr2820581410> 3.0.co; 2- # . PMID 3756808 .
- ^ Honikel, KO (2008). «Использование контроля нитратов и нитритов при переработке мясных продуктов». Мясная наука . 78 (1–2): 68–76. DOI : 10.1016 / j.meatsci.2007.05.030 . PMID 22062097 .
- ^ Ли, L; Арчер, MC; Брюс, WR (октябрь 1981 г.). «Отсутствие летучих нитрозаминов в кале человека». Cancer Res . 41 (10): 3992–4. PMID 7285009 .
- ^ Bingham, SA; Пигнателли, В; Поллок-младший; и другие. (Март 1996 г.). « Объясняет ли повышенное эндогенное образование N- нитрозосоединений в толстой кишке человека связь между красным мясом и раком толстой кишки?» . Канцерогенез . 17 (3): 515–23. DOI : 10.1093 / carcin / 17.3.515 . PMID 8631138 .
- ^ Kuhnle, GG; Рассказ, ГВт; Реда, Т; и другие. (Октябрь 2007 г.). «Диета-индуцированное эндогенное образование нитрозосоединений в желудочно-кишечном тракте». Свободный Радич. Биол. Med . 43 (7): 1040–7. DOI : 10.1016 / j.freeradbiomed.2007.03.011 . PMID 17761300 .