Фосфонат
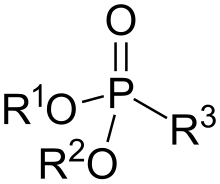
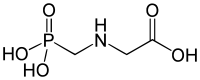
Фосфонаты или фосфоновые кислоты представляют собой фосфорорганические соединения , содержащие группы C-PO(OH) 2 или C-PO(OR) 2 (где R = алкил , арил ). Фосфоновые кислоты, с которыми обычно обращаются в виде солей, обычно представляют собой нелетучие твердые вещества, плохо растворимые в органических растворителях, но растворимые в воде и обычных спиртах. Многие коммерчески важные соединения представляют собой фосфонаты, в том числе глифосат (активная молекула гербицида «Раундап») и этефон , широко используемый регулятор роста растений. Бисфосфонаты являются популярными препаратами для лечения остеопороза . [1]
В биологии и медицинской химии фосфонатные группы используются в качестве стабильных биоизотеров фосфата, например, в противовирусном аналоге нуклеотидов, тенофовире , одном из краеугольных камней анти- ВИЧ - терапии. И есть указание на то, что производные фосфонатов являются «многообещающими лигандами для ядерной медицины ». [2]
Фосфонаты имеют тетраэдрические центры фосфора. Они структурно тесно связаны с фосфористой кислотой (и часто получаются из нее) . [3]
Большинство процессов начинается с фосфористой кислоты (также известной как фосфоновая кислота, H 3 PO 3 ), использующей ее реакционноспособную связь P-H. [1] [3]
Фосфоновую кислоту можно алкилировать в условиях Манниха с образованием аминометилированных фосфонатов, которые можно использовать в качестве комплексообразователей. Одним из примеров является промышленное получение нитрилотриса (метиленфосфоновой кислоты) :
Фосфоновая кислота также может быть алкилирована производными акриловой кислоты с получением карбоксифункционализированных фосфоновых кислот. Эта реакция является вариантом присоединения Михаэля :