| |||
| Имена | |||
|---|---|---|---|
| Другие имена Тиокиси фосфора Фосфор (V) оксид Фосфорная ангидрид тетрафосфора decaoxide тетрафосфора decoxide | |||
| Идентификаторы | |||
| |||
3D модель ( JSmol ) |
| ||
| ЧЭБИ | |||
| ChemSpider | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| P 4 O 10 | |||
| Молярная масса | 283,9 г моль -1 | ||
| Внешность | белый порошок очень расплывчатый без запаха | ||
| Плотность | 2,39 г / см 3 | ||
| Температура плавления | 340 ° С (644 ° F, 613 К) | ||
| Точка кипения | 360 ° C (возвышенные) | ||
| экзотермический гидролиз | |||
| Давление газа | 1 мм рт. Ст. При 385 ° C (стабильная форма) | ||
| Опасности | |||
| Паспорт безопасности | MSDS | ||
| NFPA 704 (огненный алмаз) | |||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Пятиокись фосфора представляет собой химическое соединение с молекулярной формулой P 4 O 10 (общее название происходит от эмпирической формулы P 2 O 5 ). Это белое кристаллическое твердое вещество представляет собой ангидрид из фосфорной кислоты . Это мощный осушающий и обезвоживающий агент .
Структура [ править ]
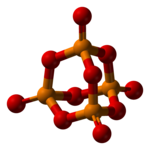
Пятиокись фосфора кристаллизуется по крайней мере в четырех формах или полиморфах . Наиболее известная из них, метастабильная форма [1] (показана на рисунке), состоит из молекул P 4 O 10 . Слабые силы Ван-дер-Ваальса удерживают эти молекулы вместе в гексагональной решетке (однако, несмотря на высокую симметрию молекул, кристаллическая упаковка не является плотной упаковкой [2] ). Структура каркаса P 4 O 10 напоминает адамантан с точечной группой симметрии T d . [3] Он тесно связан с соответствующим ангидридом фосфористой кислоты., П 4 О 6 . Последний лишен терминальных оксогрупп. Его плотность составляет 2,30 г / см 3 . Кипит при 423 ° C при атмосферном давлении; при более быстром нагревании он может сублимироваться. Эта форма может быть получена путем быстрой конденсации паров пятиокиси фосфора, и в результате получается чрезвычайно гигроскопичное твердое вещество. [4]
Другие полиморфы являются полимерными, но в каждом случае атомы фосфора связаны тетраэдром атомов кислорода, один из которых образует концевую связь P = O, включающую передачу концевых p-орбитальных электронов кислорода в разрыхляющую фосфорно-кислородную единицу. облигации. Макромолекулярная форма может быть получена путем нагревания соединения в герметичной пробирке в течение нескольких часов и выдерживания расплава при высокой температуре перед охлаждением расплава до твердого состояния. [4] метастабильной орторомбической «О» -форма (плотность 2,72 г / см 3 , температура плавления 562 ° С) принимает слоистую структуру , состоящую из взаимосвязанных P 6 O 6 колец, а не в отличие от структуры , принятой некоторыми поли силикатов. Стабильная форма - это фаза с более высокой плотностью, также орторомбическая, так называемая O 'форма. Он состоит из трехмерного каркаса плотностью 3,5 г / см 3 . [1] [5] Оставшийся полиморф представляет собой стекло или аморфную форму; это может быть получено путем сплавления любых других.
Подготовка [ править ]
P 4 O 10 получают сжиганием тетрафосфора при достаточной подаче кислорода:
- Р 4 + 5 О 2 → Р 4 О 10
На протяжении большей части 20-го века пятиокись фосфора использовалась как источник концентрированной чистой фосфорной кислоты . В термическом процессе пятиокись фосфора, полученная сжиганием белого фосфора, растворялась в разбавленной фосфорной кислоте с получением концентрированной кислоты. [6] Усовершенствования в технологии фильтрации приводят к тому, что «мокрый процесс с фосфорной кислотой» заменяет термический процесс, устраняя необходимость в производстве белого фосфора в качестве исходного материала. [7] Дегидратация фосфорной кислоты до пятиокиси фосфора невозможна, поскольку при нагревании метафосфорная кислота будет кипеть, не теряя всей своей воды.
Приложения [ править ]
Пятиокись фосфора является сильнодействующим дегидратирующим агентом, на что указывает экзотермический характер его гидролиза:
- P 4 O 10 + 6 H 2 O → 4 H 3 PO 4 (–177 кДж )
Однако его полезность для сушки несколько ограничена его тенденцией к образованию защитного вязкого покрытия, которое препятствует дальнейшему обезвоживанию неизрасходованным материалом. Гранулированный P 4 O 10 используется в эксикаторах .
Обладая сильной осушающей способностью, P 4 O 10 используется в органическом синтезе для обезвоживания. Наиболее важное применение - преобразование первичных амидов в нитрилы : [8]
- P 4 O 10 + RC (O) NH 2 → P 4 O 9 (OH) 2 + RCN
Указанный побочный продукт P 4 O 9 (OH) 2 является идеальной формулой для неопределенных продуктов, возникающих в результате гидратации P 4 O 10 .
В качестве альтернативы, при сочетании с карбоновой кислотой результатом является соответствующий ангидрид : [9]
- P 4 O 10 + RCO 2 H → P 4 O 9 (OH) 2 + [RC (O)] 2 O
«Реагент Онодера», раствор P 4 O 10 в ДМСО , используется для окисления спиртов . [10] Эта реакция напоминает окисление Сверна .
Осушающая способность P 4 O 10 достаточно сильна, чтобы преобразовать многие минеральные кислоты в их ангидриды. Примеры: HNO 3 превращается в N 2 O 5 ; H 2 SO 4 превращается в SO 3 ; HClO 4 превращается в Cl 2 O 7 ; CF 3 SO 3 H превращается в (CF 3 ) 2 S 2 O 5 .
Связанные оксиды фосфора [ править ]
Между коммерчески важными P 4 O 6 и P 4 O 10 известны оксиды фосфора с промежуточной структурой. [11]
Опасности [ править ]
Сам по себе пятиокись фосфора не горюч. Как и триоксид серы , он бурно реагирует с водой и содержащими воду веществами, такими как дерево или хлопок, выделяет много тепла и может даже вызвать пожар из-за сильно экзотермического характера таких реакций. Он вызывает коррозию металла и вызывает сильное раздражение - он может вызвать серьезные ожоги глаз, кожи, слизистой оболочки и дыхательных путей даже при таких низких концентрациях, как 1 мг / м 3 . [12]
См. Также [ править ]
- Реагент Итона
Ссылки [ править ]
- ^ a b Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ Круикшэнк, DWJ (1964). «Усовершенствования структур, содержащих связи между Si, P, S или Cl и O или N: V. P 4 O 10 ». Acta Crystallogr . 17 (6): 677–9. DOI : 10.1107 / S0365110X64001669 .
- ^ DEC Corbridge "Фосфор: Краткое описание его химии, биохимии и технологии" 5-е издание Elsevier: Амстердам. ISBN 0-444-89307-5 .
- ^ а б . Кэтрин Э. Хаукрофт; Алан Г. Шарп (2008). «Глава 15: Группа 15 элементов». Неорганическая химия, 3-е издание . Пирсон. п. 473. ISBN 978-0-13-175553-6.
- ^ D. Stachel, I. Svoboda и H. Fuess (июнь 1995 г.). «Пятиокись фосфора при 233 К». Acta Crystallogr. C . 51 (6): 1049–1050. DOI : 10.1107 / S0108270194012126 .
- ^ Трелфолл, Ричард Э., (1951). История 100-летия производства фосфора: 1851 - 1951 гг . Олдбери: Олбрайт и Уилсон Лтд.
- ^ Поджер, Хью (2002). Олбрайт и Уилсон: Последние 50 лет . Studley: Brewin Books. ISBN 1-85858-223-7
- ^ Мейер, М.С. «Оксид фосфора (V)» в Энциклопедии реагентов для органического синтеза (Эд: Л. Пакетт) 2004, J. Wiley & Sons, Нью-Йорк. DOI : 10.1002 / 047084289X .
- ^ Джозеф С. Саламоне, изд. (1996). Энциклопедия полимерных материалов: С, Том 2 . CRC Press. п. 1417. ISBN 0-8493-2470-X.
- ^ Тидвелл, TT «Диметилсульфоксид – пятиокись фосфора» в Энциклопедии реагентов для органического синтеза (Эд: Л. Пакетт) 2004, J. Wiley & Sons, Нью-Йорк. DOI : 10.1002 / 047084289X .
- ^ Luer, B .; Янсен, М. «Уточнение кристаллической структуры нонаоксида тетрафосфора, P 4 O 9 » Zeitschrift fur Kristallographie 1991, том 197, страницы 247-8.
- ^ Пятиокись фосфора MSDS