 | |
| Имена | |
|---|---|
| Название ИЮПАК Платина (IV) фторид | |
| Другие имена Тетрафторид платины Фторид платины | |
| Идентификаторы | |
3D модель ( JSmol ) | |
PubChem CID | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| F 4 Pt | |
| Молярная масса | 271.078 [1] |
| Внешность | красно-оранжевое твердое вещество [1] |
| Плотность | 7,08 г / см 3 (рассчитано) [2] |
| Температура плавления | 600 ° С (1112 ° F, 873 К) [1] |
| + 455,0 · 10 −6 см 3 / моль | |
| Структура | |
| Ромбическая , oF40 | |
| Fdd2, № 43 [2] | |
a = 0,9284 нм, b = 0,959 нм, c = 0,5712 нм | |
| Родственные соединения | |
Другие анионы | Бромид платины (IV) Хлорид платины (IV) |
Родственные соединения | Фторид платины (V) Фторид платины (VI) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
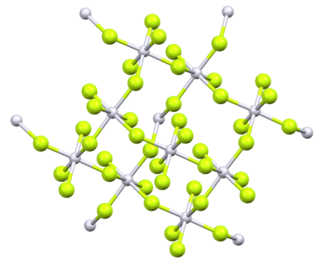
Тетрафторид платины - неорганическое соединение с химической формулой PtF.
4. В твердом состоянии соединение имеет платину (IV) в октаэдрической координационной геометрии . [2]
Подготовка [ править ]
О соединении впервые сообщил Анри Муассан при фторировании металлической платины в присутствии фтороводорода . [3] Современный синтез включает термическое разложение гексафторида платины . [4]
Свойства [ править ]
Пары тетрафторида платины при 298,15 К состоят из отдельных молекул. Энтальпия сублимации 210 кДжмоль -1 . [5] Первоначальный анализ порошкообразного PtF 4 предполагал тетраэдрическую геометрию молекулы , но более поздний анализ несколькими методами идентифицировал его как октаэдрический, с четырьмя из шести фторов на каждой платине, соединяющими мостик с соседними платиновыми центрами. [6]
Реакции [ править ]
Раствор тетрафторида платины в воде окрашен в красновато-коричневый цвет, но он быстро разлагается, выделяя тепло и образуя осадок гидрата диоксида платины оранжевого цвета и фторплатиновую кислоту. [7] При нагревании до температуры докрасна тетрафторид платины разлагается на металлическую платину и газообразный фтор. При нагревании в контакте со стеклом вместе с металлом образуется газообразный тетрафторид кремния . [7]
Тетрафторид платины может образовывать аддукты с тетрафторидом селена и трифторидом брома . [7] Летучие кристаллические аддукты также образуются в комбинации с BF 3 , PF 3 , BCl 3 и PCl 3 . [7]
Родственные соединения [ править ]
В fluoroplatinates представляют собой соли , содержащие PTF 6 2- ион. Фтороплатиновая кислота H 2 PtF 6 образует желтые кристаллы, которые поглощают воду из воздуха. Аммоний, натрий, магний, кальций, стронций и редкоземельные элементы, включая соли фторпалатината лантана, растворимы в воде. [7] Соли калия, рубидия, цезия и бария не растворимы в воде. [7]
Ссылки [ править ]
- ^ a b c Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press . п. 4.81. ISBN 1439855110.
- ^ a b c Mueller, BG; Серафин, М. (1992). «Монокристаллические исследования PtF 4 и PtF 5 ». Европейский журнал неорганической химии твердого тела . 29 : 625–633. DOI : 10.1002 / chin.199245006 .[ требуется полная цитата ]
- ^ Муассан, Х. «Тетрафторид платины». Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences . 109 : 807–9.
- ^ Сливник, JE; Земва, Б .; Дружина, Б. (1980). «Новые синтезы фторидов платины (IV) и платины (VI)». Журнал химии фтора . 15 (4): 351. DOI : 10.1016 / S0022-1139 (00) 81471-2 .
- ^ Бондаренко, АА; Коробов М.В.; Миткин, В.Н.; Сидоров, Л.Н. (март 1988 г.). «Энтальпия сублимации тетрафторида платины». Журнал химической термодинамики . 20 (3): 299–303. DOI : 10.1016 / 0021-9614 (88) 90125-5 .
- ^ "Твердотельные структуры двойных фторидов переходных металлов". Успехи неорганической химии и радиохимии . 27 . Академическая пресса. 1983. Раздел V: Тетрафториды, страницы 97–103. ISBN 9780080578767.
- ^ a b c d e f Дерек Гарри Ломанн (октябрь 1961 г.). Фториды платины и родственных соединений (Дис.). Университет Британской Колумбии.