| Химозин | |||||||||
|---|---|---|---|---|---|---|---|---|---|
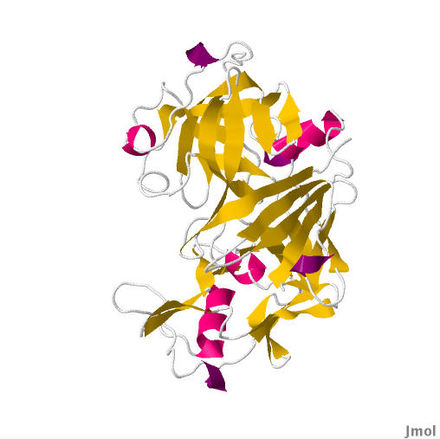 Кристаллическая структура бычьего химозинового комплекса с ингибитором CP-113972. [1] | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 3.4.23.4 | ||||||||
| Количество CAS | 9001-98-3 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
Химозин / к aɪ м ə с ɪ п / или ренин / г ɛ п ɪ п / является протеазы найдены в сычужный . Это аспарагиновая эндопептидаза, принадлежащая к семейству MEROPS A1. Новорожденные жвачные животные вырабатывают его в слизистой оболочке сычуга для свертывания молока, которое они проглатывают, что позволяет дольше оставаться в кишечнике и лучше всасываться. Он широко используется при производстве сыра . Химозин крупного рогатого скота теперь производится рекомбинантнов E. coli , Aspergillus niger var awamori и K. lactis в качестве альтернативного ресурса.
Возникновение [ править ]
Химозин производится жвачных животных в слизистой оболочке сычуга . Химозин вырабатывается главными клетками желудка молодых жвачных и некоторых других новорожденных животных [2] для свертывания молока, которое они глотают, что позволяет дольше оставаться в кишечнике и лучше всасываться. Его производят некоторые другие нежвачные животные, в том числе свиньи, кошки и тюлени. [3]
В одном исследовании сообщалось об обнаружении химозиноподобного фермента у некоторых младенцев [4], но другим не удалось воспроизвести это открытие. [5] У людей есть псевдоген химозина, который не генерирует белок, обнаруженный на хромосоме 1 . [3] [6] У людей есть другие белки для переваривания молока, такие как пепсин и липаза . [7] : 262
Ферментативная реакция [ править ]
Химозин используется для обильного выпадения осадков и образования творога в сыроделии . Нативный субстрат химозина представляет собой К-казеин, который специфически расщепляется по пептидной связи между аминокислотными остатками 105 и 106, фенилаланином и метионином . [8] Полученный продукт - фосфоказеинат кальция . [ необходима цитата ] Когда специфическая связь между гидрофобной (пара-казеин) и гидрофильной (кислый гликопептид ) группамиказеин разрушается, гидрофобные группы объединяются и образуют трехмерную сеть, которая улавливает водную фазу молока.
Зарядовые взаимодействия между гистидинами на каппа-казеине и глутаматами и аспартатами химозина инициируют связывание фермента с субстратом. [8] Когда химозин не связывает субстрат, бета-шпилька, иногда называемая «лоскутом», может связывать водород с активным сайтом, таким образом покрывая его и не позволяя в дальнейшем связываться с субстратом. [1]
Примеры [ править ]
Ниже перечислены ген Cym жвачных животных и соответствующий псевдоген человека:
|
| ||||||||||||||||||||||||||||||||||||||||||||
Рекомбинантный химозин [ править ]
Из-за несовершенства и нехватки микробных и животных сычужных ферментов производители искали замену. С развитием генной инженерии стало возможным извлекать гены, продуцирующие сычужный фермент, из желудка животных и вставлять их в определенные бактерии , грибы или дрожжи, чтобы они производили химозин во время ферментации. [10] [11] Генетически модифицированный микроорганизм погибает после ферментации, и химозин выделяется из ферментационного бульона, поэтому химозин, произведенный ферментацией (FPC), используемый производителями сыра, не содержит каких-либо ГМ-компонентов или ингредиентов. [12]FPC содержит химозин, идентичный химозину животного происхождения, но производится более эффективным способом. Продукты FPC присутствуют на рынке с 1990 года и считаются идеальным ферментом свертывания молока. [13]
FPC был первым искусственно созданным ферментом, зарегистрированным и разрешенным Управлением по контролю за продуктами и лекарствами США . В 1999 г. около 60% твердого сыра в США производилось из FPC [14], и на него приходилось до 80% доли мирового рынка сычужного фермента. [15]
К 2008 году примерно от 80% до 90% сыров, производимых в промышленных масштабах в США и Великобритании, производились с использованием FPC. [12] Наиболее широко используемый химозин, производимый ферментацией, производится с использованием грибка Aspergillus niger или Kluyveromyces lactis .
FPC содержит только химозин B, достигая высокой степени чистоты по сравнению с животным сычужным ферментом. FPC может принести производителю сыра несколько преимуществ по сравнению с животным или микробным сычужным ферментом, например, более высокий выход продукции, лучшая текстура творога и снижение горечи. [13]
Ссылки [ править ]
- ^ a b PDB : 1CZI ; Groves MR, Dhanaraj V, Badasso M, Nugent P, Pitts JE, Hoover DJ, Blundell TL (октябрь 1998 г.). «А 2.3. Разрешающая структура химозина в комплексе с ингибитором восстановленных связей показывает, что бета-шпилька активного центра перестраивается по сравнению с природной кристаллической структурой» (PDF) . Protein Eng . 11 (10): 833–40. DOI : 10,1093 / белок / 11.10.833 . PMID 9862200 .
- ↑ Kitamura N, Tanimoto A, Hondo E, Andrén A, Cottrell DF, Sasaki M, Yamada J (август 2001). «Иммуногистохимическое исследование онтогенеза прохимозин- и пепсиноген-продуцирующих клеток в сычуге овец». Anatomia, Histologia, Embryologia: Журнал ветеринарной медицины серии C . 30 (4): 231–5. DOI : 10.1046 / j.1439-0264.2001.00326.x . PMID 11534329 .
- ^ a b Персонал, Интернет-база данных по менделевскому наследованию в человеке (OMIM). Последнее обновление: 21 февраля 1997 г. Псевдоген химозина; CYMP prochymosin, включенный в OMIM
- ^ Хеншель, MJ; Ньюпорт, MJ; Пармар, В. (1987). «Желудочные протеазы у младенца человека». Биология новорожденного . 52 (5): 268–272. DOI : 10.1159 / 000242719 . ISSN 0006-3126 . PMID 3118972 .
- ^ Сечи, Пал Бела; Харбо, Марианна (2013). «Глава 5: Химозин» . В Rawlings, Neil D .; Салвесен, Гай (ред.). Справочник по протеолитическим ферментам . 1 . С. 37–42. DOI : 10.1016 / B978-0-12-382219-2.00005-3 .
- ^ Фокс, П. Ф. Книги Google. Сыр: химия, физика и микробиология: Том 1: Общие аспекты.
- ^ Ян Р. Сандерсон, доктор медицины и У. Аллан Уокер, Развитие желудочно-кишечного тракта pmph usa 1999. ISBN 155009081X
- ^ a b Gilliland GL, Oliva MT, Dill J (1991). «Функциональные последствия трехмерной структуры бычьего химозина». Adv. Exp. Med. Биол . Успехи экспериментальной медицины и биологии. 306 : 23–37. DOI : 10.1007 / 978-1-4684-6012-4_3 . ISBN 978-1-4684-6014-8. PMID 1812710 .
- ^ PDB : 4CMS ; Ньюман М., Сафро М., Фразао С., Хан Г., Зданов А., Щекотка И.Дж., Бланделл Т.Л., Андреева Н. (октябрь 1991 г.). «Рентгеновский анализ аспарагиновых протеиназ. IV. Структура и уточнение при разрешении 2,2 А бычьего химозина». J. Mol. Биол . 221 (4): 1295–309. DOI : 10.1016 / 0022-2836 (91) 90934-X . PMID 1942052 .
- ^ Emtage JS, Angal S, Doel MT, Харрис TJ, Дженкинс B, G Лилли, Lowe PA (июнь 1983). «Синтез прохимозина теленка (прореннина) в Escherichia coli» . Proc. Natl. Акад. Sci. США . 80 (12): 3671–5. Bibcode : 1983PNAS ... 80.3671E . DOI : 10.1073 / pnas.80.12.3671 . PMC 394112 . PMID 6304731 .
- ↑ Harris TJ, Lowe PA, Lyons A, Thomas PG, Eaton MA, Millican TA, Patel TP, Bose CC, Carey NH, Doel MT (апрель 1982). «Молекулярное клонирование и нуклеотидная последовательность кДНК, кодирующая препрохимозин теленка» . Nucleic Acids Res . 10 (7): 2177–87. DOI : 10.1093 / NAR / 10.7.2177 . PMC 320601 . PMID 6283469 .
- ^ а б «Химосин» . ГМО Компас. Архивировано из оригинала на 2015-03-26 . Проверено 3 марта 2011 .
- ^ а б Закон BA (2010). Технология сыроделия . Великобритания: Wiley-Blackwell. С. 100–101. ISBN 978-1-4051-8298-0.
- ^ «Пищевая биотехнология в Соединенных Штатах: наука, регулирование и проблемы» . Государственный департамент США . Проверено 14 августа 2006 .
- ↑ Johnson ME, Люси JA (апрель 2006 г.). «Основные технологические достижения и тенденции в области сыра» . J. Dairy Sci . 89 (4): 1174–8. DOI : 10.3168 / jds.S0022-0302 (06) 72186-5 . PMID 16537950 .
Дальнейшее чтение [ править ]
- Фольтманн Б. (1966). «Обзор прореннина и реннина». CR Trav Lab Carlsberg . 35 (8): 143–231. PMID 5330666 .
- Visser S, Slangen CJ, van Rooijen PJ (июнь 1987 г.). «Пептидные субстраты для химозина (реннина). Сайты взаимодействия в последовательностях, связанных с каппа-казеином, расположены вне области (103-108) -гексапептида, которая входит в щель активного сайта фермента» . Biochem. Дж . 244 (3): 553–8. DOI : 10.1042 / bj2440553 . PMC 1148031 . PMID 3128264 .
Внешние ссылки [ править ]
- Merops онлайновой базы данных для пептидазы и их ингибиторов: A01.006