| Имена | |||
|---|---|---|---|
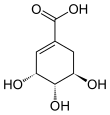
| Название ИЮПАК (3 R , 4 S , 5 R ) -3,4,5-тригидроксициклогекс-1-ен-1-карбоновая кислота | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100,004,850 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 7 Н 10 О 5 | |||
| Молярная масса | 174,15 г / моль | ||
| Температура плавления | От 185 до 187 ° C (от 365 до 369 ° F; от 458 до 460 K) | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Шикимовая кислота , более известная как ее анионная форма шикимат , представляет собой циклогексен , циклитол и циклогексанкарбоновую кислоту . Это важный биохимический метаболит растений и микроорганизмов. Его название происходит от японского цветка шикими (シ キ ミ, японский звездчатый анис , Illicium anisatum ), от которого он был впервые выделен в 1885 году Йоханом Фредриком Эйкманом . [1] Выяснение его структуры было сделано почти 50 лет спустя. [2]
Свойства [ править ]
Он входит в список канцерогенов Группы 3 Международного агентства по изучению рака . Группа 3 означает, что агент не поддается классификации по канцерогенности для человека. Тем не менее, рекомендуется жарить листья древовидного папоротника, специальное блюдо, называемое фиддлхед (свернутые листья молодого древовидного папоротника отряда Cyatheales , собранные для использования в качестве овоща). Эти листья съедобны, но сначала их нужно обжарить, чтобы удалить шикимовую кислоту. [3]
Шикимовая кислота также является гликозидной частью некоторых гидролизуемых танинов . Кислота хорошо растворяется в воде и нерастворима в неполярных растворителях, поэтому шикимовая кислота активна только против грамположительных бактерий из-за непроницаемости грамотрицательных бактерий через внешнюю клеточную мембрану . [4]
Биосинтез [ править ]
Фосфоенолпируват и эритрозо-4-фосфат реагируют с образованием 3-дезокси- D- арабиногептулозонат-7-фосфата (DAHP) в реакции, катализируемой ферментом DAHP-синтазой . Затем DAHP превращается в 3-дегидрохинат (DHQ) в реакции, катализируемой DHQ-синтазой . Хотя для этой реакции в качестве кофактора требуется никотинамидадениндинуклеотид (НАД), ферментативный механизм регенерирует его, что приводит к отсутствию чистого использования НАД.
- Биосинтез 3-дегидрохината из фосфоенолпирувата и эритрозо-4-фосфата
ДГК дегидратируется до 3-дегидрошикимовой кислоты ферментом 3-дегидрохинатдегидратазой , которая восстанавливается до шикимовой кислоты ферментом шикиматдегидрогеназой , который использует никотинамидадениндинуклеотидфосфат (НАДФН) в качестве кофактора.
- Биосинтез шикимовой кислоты из 3-дегидрохината
Путь Шикимата [ править ]
Биосинтез ароматических аминокислот [ править ]
Путь шикимата - это семиэтапный метаболический путь, используемый бактериями , грибами , водорослями , паразитами и растениями для биосинтеза ароматических аминокислот ( фенилаланина , тирозина и триптофана ). Этот путь не встречается у животных; следовательно, фенилаланин и триптофан представляют собой незаменимые аминокислоты, которые должны быть получены из рациона животного (животные могут синтезировать тирозин из фенилаланина и, следовательно, не являются незаменимой аминокислотой, за исключением людей, неспособных гидроксилировать фенилаланин до тирозина ).
Семь ферментов, участвующих в пути шикимата, - это DAHP-синтаза , 3-дегидрохинатсинтаза , 3-дегидрохинатдегидратаза , шикиматдегидрогеназа , шикимат-киназа , EPSP-синтаза и хоризмат-синтаза . Путь начинается с двух субстратов , фосфоенолпирувата и эритрозо-4-фосфата, и заканчивается хоризматом , субстратом для трех ароматических аминокислот. Пятый задействованный фермент - это шикимат киназа , фермент, который катализирует АТФ- зависимуюфосфорилирование по шикимат с образованием шикимат 3-фосфата ( как показано на рисунке , приведенном ниже). [5] Затем шикимат-3-фосфат соединяется с фосфоенолпируватом с образованием 5-енолпирувилшикимат-3-фосфата через фермент 5-енолпирувилшикимат-3-фосфат (EPSP) синтазу .
Затем 5-енолпирувилшикимат-3-фосфат превращается в хоризмат с помощью хоризмат-синтазы .
Затем префеновая кислота синтезируется перегруппировкой по Клайзену хоризмата с помощью хоризматмутазы . [6] [7]
Префенат подвергается окислительному декарбоксилированию с сохранением гидроксильной группы с образованием п- гидроксифенилпирувата, который трансаминируется с использованием глутамата в качестве источника азота с образованием тирозина и α-кетоглутарата .
Отправная точка в биосинтезе некоторых фенольных соединений [ править ]
Фенилаланин и тирозин являются предшественниками, используемыми в биосинтезе фенилпропаноидов . Затем фенилпропаноиды используются для производства флавоноидов , кумаринов , танинов и лигнина . Первый задействованный фермент - это фенилаланинаммиаклиаза (PAL), которая превращает L - фенилаланин в транс - коричную кислоту и аммиак .
Биосинтез галловой кислоты [ править ]
Галловая кислота образуется из 3-дегидрошикимата под действием фермента шикимат-дегидрогеназа с образованием 3,5-дидегидрошикимата . Это последнее соединение спонтанно перестраивается в галловую кислоту. [8]
Другие соединения [ править ]
Шикимовая кислота является предшественником:
- индол , производные индола и триптофан и производные триптофана ароматических аминокислот, такие как психоделическое соединение диметилтриптамин
- многие алкалоиды и другие ароматические метаболиты
Микоспорин-подобные аминокислоты [ править ]
Микоспориноподобные аминокислоты представляют собой небольшие вторичные метаболиты, вырабатываемые организмами, которые живут в среде с большим количеством солнечного света, обычно в морской среде.
Использует [ редактировать ]
В фармацевтической промышленности шикимовая кислота из китайского звездчатого аниса ( Illicium verum ) используется в качестве основного материала для производства осельтамивира ( Тамифлю ). Хотя шикимовая кислота присутствует в большинстве автотрофных организмов, она является промежуточным продуктом биосинтеза и обычно встречается в очень низких концентрациях. Низкий выход шикимовой кислоты из китайского аниса звездчатого является причиной нехватки озельтамивира в 2005 году. Шикимовую кислоту также можно извлечь из семян плодов сладкой жевательной резинки ( Liquidambar styraciflua ) [2]который в изобилии встречается в Северной Америке, его урожайность составляет около 1,5%. Например, для четырнадцати упаковок Тамифлю необходимо 4 кг семян сладкой жевательной резинки. Для сравнения, звездчатый анис дает от 3% до 7% шикимовой кислоты. Биосинтетические пути в E. coli недавно были усовершенствованы, чтобы позволить организму накапливать достаточно материала для коммерческого использования. [9] [10] [11] Исследование 2010 года, опубликованное Университетом штата Мэн, показало, что шикимовую кислоту можно легко получить из игл нескольких видов сосны . [12]
Защитные группы чаще используются в небольших лабораторных работах и на начальных этапах разработки, чем в процессах промышленного производства, поскольку их использование добавляет дополнительные этапы и затраты на материалы. Однако наличие дешевого хирального строительного блока может преодолеть эти дополнительные затраты, например, шикимовую кислоту для осельтамивира .
Аминошикимовая кислота также является альтернативой шикимовой кислоте в качестве исходного материала для синтеза осельтамивира.
Мишень для наркотиков [ править ]
Шикимат может быть использован для синтеза (6 S ) -6-fluoroshikimic кислоты , [13] антибиотик , который ингибирует ароматический путь биосинтеза. [14]
Глифосат , активный ингредиент гербицида Раундап , убивает растения, нарушая путь шикимата у растений. Более конкретно, глифосат ингибирует фермент 5-енолпирувилшикимат-3-фосфатсинтазу (EPSPS). Генетически модифицированные культуры "Roundup Ready" преодолевают этот запрет. [ необходима цитата ]
См. Также [ править ]
- Путь аминосикимат , новый вариант пути шикимат
Ссылки [ править ]
- ^ Эйкман, JF (1881). "Ботанические отношения Illicium Religiosum Sieb., Illicium anisatum Lour" . Американский фармацевтический журнал . 53 (8).
- ^ a b Enrich, LB; Scheuermann, ML; Mohadjer, A .; Матиас, КР; Eller, CF; Ньюман, MS; Fujinaka, M .; Пун, Т. (2008). « Liquidambar styraciflua : возобновляемый источник шикимовой кислоты». Буквы тетраэдра . 49 (16): 2503–2505. DOI : 10.1016 / j.tetlet.2008.02.140 .
- ^ Эванс, ИА; Осман, Массачусетс (26 июля 1974 г.). «Канцерогенность папоротника и шикимовой кислоты». Природа . 250 (5464): 348–9. Bibcode : 1974Natur.250..348E . DOI : 10.1038 / 250348a0 . PMID 4211848 . S2CID 4175635 .
- Перейти ↑ Hai-Jung, Chung (2009). «Оценка биологической активности экстрактов звездчатого аниса» (PDF) . ocean.kisti.re.kr . Проверено 18 июня 2019 .
- ^ Herrmann, KM; Уивер, LM (1999). «Путь Шикимэ». Ежегодный обзор физиологии растений и молекулярной биологии растений . 50 : 473–503. DOI : 10.1146 / annurev.arplant.50.1.473 . PMID 15012217 .
- ^ Goerisch, H. (1978). «О механизме хоризматмутазной реакции». Биохимия . 17 (18): 3700–3705. DOI : 10.1021 / bi00611a004 . PMID 100134 .
- ^ Kast, P .; Tewari, YB; Wiest, O .; Hilvert, D .; Houk, KN ; Голдберг, Роберт Н. (1997). «Термодинамика превращения хоризма в префенат: экспериментальные результаты и теоретические прогнозы». Журнал физической химии B . 101 (50): 10976–10982. DOI : 10.1021 / jp972501l .
- ^ "Путь галловой кислоты" . metacyc.org .
- Перейти ↑ Bradley, D. (декабрь 2005 г.). «Звездная роль бактерий в борьбе с пандемией гриппа?». Обзоры природы Открытие лекарств . 4 (12): 945–946. DOI : 10.1038 / nrd1917 . PMID 16370070 . S2CID 30035056 .
- ^ Krämer, M .; Bongaerts, J .; Bovenberg, R .; Кремер, С .; Müller, U .; Орф, С .; Wubbolts, M .; Рэйвен, Л. (2003). «Метаболическая инженерия для микробиологического производства шикимовой кислоты». Метаболическая инженерия . 5 (4): 277–283. DOI : 10.1016 / j.ymben.2003.09.001 . PMID 14642355 .
- ^ Johansson, L .; Линдског, А .; Silfversparre, G .; Cimander, C .; Nielsen, KF; Лиден, Г. (2005). «Производство шикимовой кислоты модифицированным штаммом E. coli (W3110.shik1) в условиях ограничения фосфатов и углерода». Биотехнология и биоинженерия . 92 (5): 541–552. DOI : 10.1002 / bit.20546 . PMID 16240440 . S2CID 19659961 .
- ^ "Хвоя сосны штата Мэн дает ценный материал Тамифлю" . Boston.com . 7 ноября 2010 г.
- ^ (PDF) https://web.archive.org/web/20160304001748/http://jiang.tju.edu.cn/pdfs/6flufull.pdf . Архивировано 4 марта 2016 года из оригинального (PDF) . Отсутствует или пусто
|title=( справка ) - ^ «(6 S ) -6-фторошикимовая кислота, антибактериальный агент, действующий на ароматический биосинтетический путь» (PDF) .
Книги [ править ]
- Хаслам, Э. (1974). Путь Шикимате (1-е изд.).
- Хаслам, Э. (1993). Шикимовая кислота .
Внешние ссылки [ править ]
- «Биосинтез шикимата и хоризматов» . Департамент химии Лондонского университета королевы Марии.