 | |
 | |
| Имена | |
|---|---|
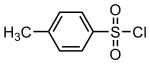
| Предпочтительное название IUPAC 4-метилбензол-1-сульфонилхлорид | |
| Другие названия Тозилхлорид, п- толуолсульфонилхлорид, п -TsCl, TsCl | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.002.441 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 7 H 7 ClO 2 S | |
| Молярная масса | 190,65 г / моль |
| Появление | Белое твердое вещество |
| Температура плавления | От 65 до 69 ° C (от 149 до 156 ° F, от 338 до 342 K) |
| Точка кипения | 134 ° С (273 ° F, 407 К) при 10 мм рт. |
| Гидролиз | |
| Опасности [1] | |
| Основные опасности | Реагирует с водой с образованием различных кислот. |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 128 ° С (262 ° F, 401 К) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
4-Толуолсульфонилхлорид ( п- толуолсульфонилхлорид , толуол- п- сульфонилхлорид ) представляет собой органическое соединение с формулой CH 3 C 6 H 4 SO 2 Cl. Это белое твердое вещество с неприятным запахом - реагент, широко используемый в органическом синтезе . [2] Сокращенно TsCl или TosCl , это производное толуола и содержит функциональную группу сульфонилхлорида (-SO 2 Cl) .
Использует [ редактировать ]
Характерным образом, TsCl превращает спирты (сокращенно ROH) в соответствующие сложные эфиры толуолсульфоновой кислоты или тозилпроизводные («тозилаты»):
- CH 3 C 6 H 4 SO 2 Cl + ROH → CH 3 C 6 H 4 SO 2 OR + HCl
Тозилаты можно расщеплять алюмогидридом лития:
- 4 CH 3 C 6 H 4 SO 2 OR + LiAlH 4 → LiAl (O 3 SC 6 H 4 CH 3 ) 4 + 4 RH
Таким образом, тозилирование с последующим восстановлением позволяет удалить гидроксильную группу.
Аналогичным образом, TsCl используется для получения сульфонамидов из аминов: [3]
- CH 3 C 6 H 4 SO 2 Cl + R 2 NH → CH 3 C 6 H 4 SO 2 NR 2 + HCl
Получающиеся сульфонамиды не являются основными, а, если они получены из первичных аминов, даже являются кислотными.
TsCl реагирует с гидразином с образованием п-толуолсульфонилгидразида .
Получение тозиловых эфиров и амидов проводят в присутствии основания, поглощающего хлористый водород. Выбор основания часто имеет решающее значение для эффективности тозилирования. Типичные основания включают пиридин и триэтиламин . Также используются необычные базы; например, каталитические количества хлорида триметиламмония в присутствии триэтиламина очень эффективны благодаря триметиламина . [2]
Другие реакции [ править ]
Поскольку TsCl является широко доступным реагентом, его реакционная способность была тщательно изучена. Он используется при дегидратации для получения нитрилов , изоцианидов и диимидов . [2] В необычной реакции, сосредоточенной на серном центре, цинк восстанавливает TsCl до сульфината, CH 3 C 6 H 4 SO 2 Na. [4]
Производство [ править ]
Этот реагент недорого доступен для лабораторного использования. Это побочный продукт производства орто- толуолсульфонилхлорида (предшественник для синтеза обычной пищевой добавки и сахарина катализатора ) путем хлорсульфирования толуола : [5]
- CH 3 C 6 H 5 + SO 2 Cl 2 → CH 3 C 6 H 4 SO 2 Cl + HCl
Ссылки [ править ]
- ^ «П-ТОЛУОЛЕСУЛЬФОНИЛХЛОРИД (ТОСИЛХЛОРИД)» .
- ^ a b c Whitaker, DT; Whitaker, KS; Джонсон, CR; Хаас, Дж. (2006). «П-толуолсульфонилхлорид» .п- Толуолсульфонилхлорид . Энциклопедия реагентов для органического синтеза . Нью-Йорк: Джон Вили. DOI : 10.1002 / 047084289X.rt136.pub2 . ISBN 978-0471936237. Архивировано из оригинала на 2016-03-05 . Проверено 28 мая 2013 .
- ^ Ichikawa, J .; Nadano, R .; Мори, Т .; Вада, Ю. (2006). "5- эндо - тригонометрические Циклизация 1,1-дифтор-1-алкенов: Синтез 3-бутил-2-фтор-1-Tosylindole" . Органический синтез . 83 : 111.; Коллективный том , 11 , с. 834
- ^ Уитмор, ФК; Гамильтон, FH (1922). «Толуолсульфинат натрия» . Органический синтез . 2 : 89.; Сборник , 1 , стр. 492
- ^ Lindner, O .; Родефельд, Л. "Бензолсульфоновые кислоты и их производные". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a03_507 .
