 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гексакарбонил вольфрам | |
| Другие имена Карбонил вольфрама гексакарбонилвольфрам | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ECHA InfoCard | 100.034.423 |
| Номер ЕС |
|
PubChem CID | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 6 O 6 Вт | |
| Молярная масса | 351,901 г / моль |
| Внешность | Бесцветное твердое вещество |
| Плотность | 2,65 г / см 3 |
| Температура плавления | 170 ° С (338 ° F, 443 К) (разлагается) |
| нерастворимый | |
| Растворимость | экономно в THF |
| Опасности | |
| Основные опасности | Воспламеняющийся, источник CO |
| Родственные соединения | |
Другие катионы | Гексакарбонил хрома Гексакарбонил молибдена |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
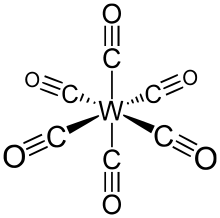
Гексакарбонил вольфрама (также называемый карбонилом вольфрама ) представляет собой химическое соединение с формулой W (CO) 6 . Этот комплекс дал начало первому примеру дигидрогенного комплекса. [1]
Это бесцветное соединение, как и его аналоги из хрома и молибдена , примечательно как летучее, стабильное на воздухе производное вольфрама в его нулевой степени окисления.
Подготовка, свойства и структура [ править ]
W (CO) 6 получают путем сокращения из ВКТ 6 под давлением моноксида углерода . Состав относительно устойчив на воздухе. Умеренно растворим в неполярных органических растворителях. Карбонил вольфрама широко используется в технике осаждения под действием электронного луча - он легко испаряется и разлагается под действием электронного луча, обеспечивая удобный источник атомов вольфрама. [2]
W (CO) 6 Принимает октаэдрическую геометрию , состоящие из шести стержнеобразных СО лиганды излучающего от центрального атома W с дипольным моментом 0 D .
Реакционная способность [ править ]
Все реакции W (CO) 6 начинаются с вытеснения части лигандов CO в W (CO) 6 . W (CO) 6 ведет себя так же, как Mo (CO) 6, но имеет тенденцию образовывать соединения, которые кинетически более устойчивы.
Обработка гексакарбонила вольфрама циклопентадиенидом натрия с последующим окислением образовавшегося NaW (CO) 3 (C 5 H 5 ) дает димер трикарбонила циклопентадиенил вольфрама . [3]
Одним из производных является дигидрогенный комплекс W (CO) 3 [P (C 6 H 11 ) 3 ] 2 (H 2 ). [1]
Три из этих лигандов CO могут быть замещены ацетонитрилом. [4] W (CO) 6 использовался для обессеривания сероорганических соединений и в качестве предшественника катализаторов метатезиса алкенов .
Безопасность и обращение [ править ]
Как и все карбонилы металлов, W (CO) 6 является опасным источником летучего металла, а также CO.
Ссылки [ править ]
- ^ a b Кубас, GJ, Metal Dihydrogen and σ-Bond Complexes, Kluwer Academic / Plenum Publishers: Нью-Йорк, 2001.
- ^ Randolph, S .; Fowlkes, J .; Стойка, П. (2006). «Сфокусированное наномасштабное осаждение и травление под действием электронного пучка». Критические обзоры твердого тела и материаловедения . 31 (3): 55. DOI : 10,1080 / 10408430600930438 .
- ^ Мэннинг, АР; Хакет, Пол; Бердвистелл, Ральф (1990). «Гексакарбонилбис (η 5 -циклопентадиенил) дихром, молибден и вольфрам и их аналоги, M 2 (η 5 -C 5 H 4 R) 2 (CO) 6 (M = Cr, Mo и W; R = H, Me или PhCH 2 ) ". Неорганические синтезы . 28 : 148–149. DOI : 10.1002 / 9780470132593.ch39 .
- ^ Кубас, GJ; ван дер Слейс, LS (1990). «Трикарбонилтрис (нитрил) комплексы Cr, Mo и W». Неорганические синтезы . 28 : 29–33. DOI : 10.1002 / 9780470132593.ch6 .