 | |||
| Имена | |||
|---|---|---|---|
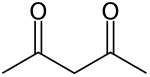
| Предпочтительное название IUPAC Пентан-2,4-дион | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 741937 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004.214 | ||
| Номер ЕС |
| ||
| 2537 | |||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2310 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 5 Н 8 О 2 | |||
| Молярная масса | 100,117 г · моль -1 | ||
| Плотность | 0,975 г / мл [1] | ||
| Температура плавления | -23 ° С (-9 ° F, 250 К) | ||
| Точка кипения | 140 ° С (284 ° F, 413 К) | ||
| 16 г / 100 мл | |||
| -54,88 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H226 , H302 , H311 , H320 , H331 , H335 , H341 , H370 , H402 , H412 | ||
Меры предосторожности GHS | Р201 , Р202 , Р210 , Р233 , Р240 , Р241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P273 , P280 , P281 , P301 + 312 , P302 + 352 , P303 + 361 + 353 , Р304 + 340 , P305 + 351 + 338 , P307 + 311 , P308 + 313 , P311 , P312 | ||
| NFPA 704 (огненный алмаз) |  2 2 0 | ||
| точка возгорания | 34 ° С (93 ° F, 307 К) | ||
самовоспламенения температуру | 340 ° С (644 ° F, 613 К) | ||
| Пределы взрываемости | 2,4–11,6% | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Ацетилацетон - это органическое соединение с формулой CH 3 COCH 2 COCH 3 . Это бесцветная жидкость, относящаяся к 1,3- дикетону . Он находится в равновесии с таутомером CH 3 C (O) CH = C (OH) CH 3 . Эти таутомеры взаимопревращаются настолько быстро в большинстве условий, что в большинстве случаев их рассматривают как единое соединение. [2] Это бесцветная жидкость, которая является предшественником ацетилацетонатного аниона (обычно сокращенно acac - ), бидентатного лиганда . Это также строительный блок для синтезагетероциклические соединения .
Свойства [ править ]
Таутомерия [ править ]
В кето и енольные таутомеры ацетилацетон сосуществует в растворе. Енольная форма имеет симметрию C 2v , что означает, что атом водорода делится поровну между двумя атомами кислорода. [3] В газовой фазе, то константа равновесия , К кет → енольному , 11,7, в пользу енольной формы. Две таутомерные формы можно различить с помощью ЯМР-спектроскопии , ИК-спектроскопии и других методов. [4] [5]
| Растворитель | К кет → енольному |
|---|---|
| Газовая фаза | 11,7 |
| Циклогексан | 42 |
| Толуол | 10 |
| THF | 7.2 |
| ДМСО | 2 |
| Вода | 0,23 |
Константа равновесия имеет тенденцию быть высокой в неполярных растворителях; кето-форма становится более предпочтительной в полярных растворителях, связывающих водородные связи, таких как вода. [6] Енольная форма представляет собой винилогичный аналог карбоновой кислоты .
Кислотно-основные свойства [ править ]
| растворитель | Т / ° C | p K a [7] |
|---|---|---|
| 40% этанол / вода | 30 | 9,8 |
| 70% диоксан / вода | 28 год | 12,5 |
| 80% ДМСО / вода | 25 | 10,16 |
| ДМСО | 25 | 13,41 |
Ацетилацетон - слабая кислота :
- С 5 Н 8 О 2 ⇌ С
5ЧАС
7О-
2+ H +
ИЮПАК рекомендовал значения p K a для этого равновесия в водном растворе при 25 ° C: 8,99 ± 0,04 ( I = 0), 8,83 ± 0,02 ( I = 0,1 M NaClO 4 ) и 9,00 ± 0,03 ( I = 1,0 M NaClO 4 ; I = Ионная сила ). [8] Доступны значения для смешанных растворителей. Очень сильные основания, такие как литийорганические соединения, дважды депротонируют ацетилацетон. Полученные дилитио-частицы затем можно алкилировать по C-1.
Подготовка [ править ]
Ацетилацетон получают в промышленности путем термической перегруппировки изопропенилацетата . [9]
- CH 2 (CH 3 ) COC (O) Me → MeC (O) CH 2 C (O) Me
Лабораторные пути к ацетилацетону начинаются также с ацетона . Ацетон и уксусный ангидрид при добавлении катализатора трифторида бора (BF 3 ): [10]
- (CH 3 CO) 2 O + CH 3 C (O) CH 3 → CH 3 C (O) CH 2 C (O) CH 3
Второй синтез включает катализируемую основанием конденсацию ацетона и этилацетата с последующим подкислением: [10]
- NaOEt + EtO 2 CCH 3 + CH 3 C (O) CH 3 → NaCH 3 C (O) CHC (O) CH 3 + 2 EtOH
- NaCH 3 C (O) CHC (O) CH 3 + HCl → CH 3 C (O) CH 2 C (O) CH 3 + NaCl
Из-за простоты этих синтезов известно много аналогов ацетилацетонатов. Некоторые примеры включают C 6 H 5 C (O) CH 2 C (O) C 6 H 5 (dbaH) и (CH 3 ) 3 CC (O) CH 2 C (O) CC (CH 3 ) 3 . Гексафторацетилацетонат также широко используется для образования летучих комплексов металлов.
Реакции [ править ]
Конденсация [ править ]
Ацетилацетон является универсальным бифункциональным предшественником гетероциклов, поскольку обе кетогруппы подвергаются конденсации . Гидразин реагирует с образованием пиразолов . Мочевина дает пиримидины . Конденсация с двумя арил- и алкиламинами с образованием NacNac , в котором атомы кислорода в ацетилацетоне заменены на NR (R = арил, алкил).
Координационная химия [ править ]
Ацетилацетонат- анион acac - образует комплексы со многими ионами переходных металлов . Общий метод синтеза заключается в обработке соли металла ацетилацетоном в присутствии основания : [11]
- МБ z + z Hacac ⇌ M (acac) z + z BH
Оба атома кислорода связываются с металлом с образованием шестичленного хелатного кольца. В некоторых случаях хелатный эффект настолько силен, что для образования комплекса не требуется добавление основания.
Биоразложение [ править ]
Фермент ацетилацетондиоксигеназа расщепляет углерод-углеродную связь ацетилацетона, образуя ацетат и 2-оксопропаналь . Фермент зависит от железа (II), но было доказано, что он также связывается с цинком. Распад ацетилацетона был охарактеризован у бактерии Acinetobacter johnsonii . [12]
- С 5 Н 8 О 2 + О 2 → С 2 Н 4 О 2 + С 3 Н 4 О 2
Ссылки [ править ]
- ^ "05581: Ацетилацетон" . Сигма-Олдрич .
- ↑ Томас М. Харрис (2001). «2,4-Пентандион». 2,4 ‐ пентандион . Энциклопедия реагентов для органического синтеза e-EROS . DOI : 10.1002 / 047084289X.rp030 . ISBN 0471936235.
- ^ Caminati, W .; Грабов, Ж.-У. (2006). «Структура C 2v энольного ацетилацетона». Варенье. Chem. Soc. 128 (3): 854–857. DOI : 10.1021 / ja055333g . PMID 16417375 .
- ^ Manbeck, Kimberly A .; Вооз, Николай С .; Bair, Nathaniel C .; Сандерс, Allix MS; Марш, Андерсон Л. (2011). «Влияние заместителей на кето-енольные равновесия с использованием ЯМР-спектроскопии». J. Chem. Educ. 88 (10): 1444–1445. Bibcode : 2011JChEd..88.1444M . DOI : 10.1021 / ed1010932 .
- ^ Йошида, З .; Ogoshi, H .; Токумицу, Т. (1970). «Внутримолекулярная водородная связь в енольной форме 3-замещенного-2,4-пентандиона». Тетраэдр . 26 (24): 5691–5697. DOI : 10.1016 / 0040-4020 (70) 80005-9 .
- Перейти ↑ Reichardt, Christian (2003). Растворители и эффекты растворителей в органической химии (3-е изд.). Wiley-VCH. ISBN 3-527-30618-8.
- ^ База данных IUPAC SC Полная база данных опубликованных данных о константах равновесия комплексов металлов и лигандов.
- ^ Stary, J .; Liljenzin, JO (1982). «Критическая оценка констант равновесия с участием ацетилацетона и его хелатов металлов» (PDF) . Чистая и прикладная химия . 54 (12): 2557–2592. DOI : 10,1351 / pac198254122557 .
- ^ Сигель, Хардо; Эггерсдорфер, Манфред (2002). «Кетоны». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a15_077 . ISBN 9783527306732.
- ^ a b C. E. Denoon, младший "Ацетилацетон" . Органический синтез .; Сборник , 3 , с. 16
- ^ О'Брайен, Брайан. «Раздаточный материал Co (tfa) 3 & Co (acac) 3 » (PDF) . Колледж Густава Адольфа.
- ^ Straganz, GD; Glieder, A .; Brecker, L .; Ленты, DW; Штайнер, В. (2003). «Фермент, расщепляющий ацетилацетон Dke1: новый фермент, расщепляющий С – С-связь из Acinetobacter johnsonii » . Биохим. Дж . 369 (3): 573–581. DOI : 10.1042 / BJ20021047 . PMC 1223103 . PMID 12379146 .
Внешние ссылки [ править ]
- Международная карта химической безопасности 0533



