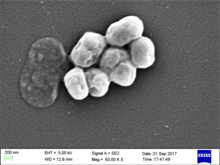
| Acinetobacter baumannii | |
|---|---|
 | |
| Acinetobacter baumannii | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Протеобактерии |
| Учебный класс: | Гаммапротеобактерии |
| Заказ: | Pseudomonadales |
| Семья: | Moraxellaceae |
| Род: | Acinetobacter |
| Разновидность: | А. бауманний |
| Биномиальное имя | |
| Acinetobacter baumannii Буве и Гримон 1986 [1] | |
Acinetobacter baumannii - это обычно короткие, почти круглые палочковидные ( коккобациллы ) грамотрицательные бактерии . Он назван в честь бактериолога Поля Баумана. [2] Это может быть оппортунистический патоген у людей, поражающий людей с ослабленной иммунной системой, и приобретает все большее значение как внутрибольничная ( нозокомиальная ) инфекция. В то время как другие виды рода Acinetobacter часто встречаются вобразцах почвы (что приводит к распространенному заблуждению о том, что A. baumannii тоже является почвенным организмом), он почти исключительно изолирован от больничных сред. [3]Хотя время от времени он обнаруживается в пробах почвы и воды [4], его естественная среда обитания до сих пор неизвестна.
Бактерии этого рода не имеют жгутиков , подобных плетям структур, которые многие бактерии используют для передвижения, но демонстрируют подергивание или роение подвижности. Это может быть связано с активностью пилей IV типа, столбовидных структур, которые могут выдвигаться и втягиваться. Подвижность A. baumannii также может быть связана с экскрецией экзополисахарида , создавая пленку из высокомолекулярных сахарных цепей позади бактерии, чтобы двигаться вперед. [5] Клинические микробиологи обычно дифференцируют представителей рода Acinetobacter от других Moraxellaceae , выполняя оксидазный тест , например Acinetobacter.виды являются единственными представителями Moraxellaceae, у которых отсутствует цитохром с оксидаза . [6]
A. baumannii является частью комплекса ACB ( геномные виды A. baumannii , A. calcoaceticus и Acinetobacter 13TU). Трудно определить конкретные виды членов комплекса ACB, и они включают наиболее клинически значимых представителей этого рода. [7] [8] A. baumannii также был идентифицирован как патоген ESKAPE ( Enterococcus faecium , Staphylococcus aureus , Klebsiella pneumoniae , Acinetobacter baumannii , Pseudomonas aeruginosa и Enterobacter разновидности), группа патогенов с высокой частотойустойчивость к антибиотикам , вызывающая большинство внутрибольничных инфекций. [9]
В просторечии A. baumannii называют « Иракибактером » из-за его внезапного появления в военных лечебных учреждениях во время войны в Ираке . [10] Это продолжало быть проблемой для ветеранов и солдат, служивших в Ираке и Афганистане. A. baumannii с множественной лекарственной устойчивостью распространился в гражданские больницы отчасти из-за транспортировки инфицированных солдат через несколько медицинских учреждений. [5]
OmpA [ править ]
Адгезия может быть решающим фактором вирулентности бактерий. Способность прикрепляться к клеткам-хозяевам позволяет бактериям взаимодействовать с ними различными способами, будь то система секреции типа III или просто удерживаясь от преобладающего движения жидкостей. Было показано, что белок А внешней мембраны (OmpA) участвует в прикреплении A. baumannii к эпителиальным клеткам. Это позволяет бактериям проникать в клетки через механизм застежки-молнии. [11] Было также показано, что белок локализуется в митохондриях эпителиальных клеток и вызывает некроз, стимулируя выработку активных форм кислорода . [12]
Устойчивость к антибиотикам [ править ]
Острова сопротивления AbaR [ править ]
Островки патогенности , относительно общие генетические структуры у бактериальных патогенов, состоят из двух или более соседних генов, которые увеличивают вирулентность патогена . Они могут содержать гены, кодирующие токсины , свертывающие кровь или, как в этом случае, позволяющие бактериям сопротивляться антибиотикам. Островки устойчивости к AbaR-типу типичны для устойчивых к лекарствам A. baumannii , и в данном штамме могут присутствовать различные варианты. Каждый состоит из основы транспозона размером около 16,3 КБ, что облегчает горизонтальный перенос генов.. Транспозоны позволяют вырезать части генетического материала из одного места в геноме и интегрировать в другое. Это делает горизонтальный перенос генов этого и подобных островов патогенности более вероятным, потому что, когда генетический материал захватывается новой бактерией, транспозоны позволяют островку патогенности интегрироваться в геном нового микроорганизма. В этом случае это даст новому микроорганизму возможность сопротивляться определенным антибиотикам. AbaR содержат несколько генов устойчивости к антибиотикам, и все они фланкированы последовательностями вставки . Эти гены обеспечивают устойчивость к аминогликозидам , аминоциклитам , тетрациклину и хлорамфениколу . [13] [14]
Отводящие насосы [ править ]
Насосы оттока - это белковые машины, которые используют энергию для перекачки антибиотиков и других небольших молекул, которые попадают в бактериальную цитоплазму и периплазматическое пространство из клетки. Постоянно выкачивая антибиотики из клетки, бактерии могут увеличивать концентрацию данного антибиотика, необходимую для их уничтожения, или подавлять их рост, когда цель антибиотика находится внутри бактерии. Известно, что A. baumannii имеет два основных оттока, которые снижают его чувствительность к антимикробным препаратам. Было показано, что первый, AdeB, отвечает за устойчивость к аминогликозидам. [15]Второй, AdeDE, отвечает за отток широкого спектра субстратов, включая тетрациклин, хлорамфеникол и различные карбапенемы. [16]
Малая РНК [ править ]
Бактериальные малые РНК - это некодирующие РНК, которые регулируют различные клеточные процессы. Три мРНК, AbsR11, AbsR25 и AbsR28, были экспериментально подтверждены на штамме MTCC 1425 (ATCC15308), который является штаммом (с множественной лекарственной устойчивостью ), демонстрирующим устойчивость к 12 антибиотикам. МРНК AbsR25 может играть роль в регуляции оттока и устойчивости к лекарствам. [17]
Бета-лактамаза [ править ]
Было показано, что A. baumannii продуцирует по крайней мере одну бета-лактамазу , которая является ферментом, ответственным за расщепление четырехатомного лактамного кольца, типичного для бета-лактамных антибиотиков . Бета-лактамные антибиотики структурно родственны пенициллину , который подавляет синтез клеточной стенки бактерий . Расщепление лактамного кольца делает эти антибиотики безвредными для бактерий. Было обнаружено, что A. baumannii экспрессирует бета-лактамазы, известные как производные от Acinetobacter цефалоспориназы (ADC), которые являются бета-лактамазами класса C. [18] Кроме того, бета-лактамаза OXA-51, бета-лактамаза класса D, была обнаружена у A. baumannii., как было обнаружено, фланкированы последовательностями вставки, что позволяет предположить, что он был получен путем горизонтального переноса генов . [19]
Формирование биопленки [ править ]
A. baumannii был известен своей очевидной способностью выживать на искусственных поверхностях в течение длительного периода времени, что позволяет ему сохраняться в условиях больницы. Считается, что это связано с его способностью образовывать биопленки . [20] У многих бактерий, образующих биопленку, этот процесс опосредуется жгутиками. Однако у A. baumannii этот процесс, по-видимому, опосредуется пили. Кроме того, было показано , что нарушение предполагаемого шаперона пилей и генов- активаторов csuC и csuE ингибирует образование биопленок. [21]Было показано, что образование биопленок изменяет метаболизм микроорганизмов внутри биопленки, следовательно, снижает их чувствительность к антибиотикам. Это может быть связано с тем, что глубже биопленки доступно меньше питательных веществ. Более медленный метаболизм может помешать бактериям поглощать антибиотик или выполнять жизненно важные функции достаточно быстро, чтобы определенные антибиотики подействовали. Они также создают физический барьер против более крупных молекул и могут предотвратить высыхание бактерий. [4] [22]
Признаки и симптомы инфекции [ править ]
A. baumannii - условно-патогенный микроорганизм, вызывающий ряд различных заболеваний, каждое из которых имеет свои симптомы. Некоторые возможные типы инфекций, вызываемых A. baumannii, включают:
- Пневмония
- Инфекции кровотока
- Менингит
- Инфекции раны и области хирургического вмешательства, включая некротический фасциит
- Инфекция мочеиспускательного канала
Симптомы инфекций, вызванных A. baumannii , часто неотличимы от других оппортунистических инфекций, вызываемых другими условно-патогенными бактериями, включая Klebsiella pneumoniae и Streptococcus pneumoniae .
Симптомы инфекций A. baumannii, в свою очередь, варьируются от лихорадки и озноба, сыпи, спутанности сознания и / или изменения психического состояния, боли или жжения при мочеиспускании, сильных позывов к мочеиспусканию, чувствительности к яркому свету, тошноты (с рвотой или без нее) боли в мышцах и груди, проблемы с дыханием и кашель (с желтой, зеленой или кровянистой слизью или без нее). [23] В некоторых случаях A. baumannii может не проявлять инфекции или симптомов, например, при колонизации открытой раны или места трахеостомы.
Лечение [ править ]
Поскольку большинство инфекций в настоящее время устойчивы к нескольким лекарствам, определение чувствительности конкретного штамма необходимо для успешного лечения. Традиционно, инфекции обрабатывали имипенем или меропенем , но устойчивый рост в карбапенема резистентные A. baumannii было отмечено. [24] Следовательно, методы лечения часто основываются на полимиксинах , особенно колистине . [25] Колистин считается лекарством последней инстанции, потому что он часто вызывает повреждение почек, помимо других побочных эффектов. [26]Методы профилактики в больницах сосредоточены на более частом мытье рук и более тщательных процедурах стерилизации. [27] А. baumannii инфекция была недавно лечить с помощью фага терапии . [28] Фаги - это вирусы, атакующие бактерии [29], а также было продемонстрировано, что они повторно повышают чувствительность A. baumannii к антибиотикам, которым он обычно сопротивляется. [30]
Ученые из Массачусетского технологического института, Гарвардского института Броада и CSAIL Массачусетского технологического института с помощью глубокого обучения обнаружили соединение под названием галицин, которое может эффективно убить A. baumannii . Соединение представляет собой перепрофилированный препарат. [31] [32]
Число пострадавших ветеранов в Ираке и Афганистане [ править ]
Солдаты в Ираке и Афганистане подвергаются риску травм из-за стрельбы и самодельных взрывных устройств . Ранее считалось, что заражение происходит из-за заражения A. baumannii во время травмы. Последующие исследования показали, что хотя A. baumannii может нечасто выделяться из естественной среды, инфекция, скорее всего, передается внутрибольничным путем, вероятно, из-за способности A. baumanniiоставаться на искусственных поверхностях в течение длительного времени, а также в нескольких помещениях, в которых раненые солдаты оказываются в процессе эвакуации раненых. Раненых солдат сначала доставляют в объекты уровня I, где их стабилизируют. В зависимости от тяжести травмы солдаты могут быть переведены в учреждение уровня II, которое состоит из передовой хирургической бригады, для дополнительной стабилизации. В зависимости от материально-технического обеспечения местности, раненые солдаты могут переходить между этими объектами несколько раз, прежде чем их наконец доставят в крупный госпиталь в зоне боевых действий (уровень III). Как правило, через 1–3 дня, когда состояние пациентов стабилизируется, их переводят по воздуху в региональное учреждение (уровень IV) для дополнительного лечения. Для солдат, проходящих службу в Ираке или Афганистане, это обычноРегиональный медицинский центр Ландштуль в Германии. Наконец, раненые солдаты переводятся в больницы своей страны для реабилитации и дополнительного лечения. [33] Это повторяющееся воздействие различных медицинских сред, кажется, является причиной того, что инфекции, вызванные A. baumannii , становятся все более распространенными. A. baumannii с множественной лекарственной устойчивостью является основным фактором, затрудняющим лечение и реабилитацию раненых солдат, и привел к дополнительным смертельным исходам. [7] [34] [35]
Заболеваемость в больницах [ править ]
Инфекция A. baumanii, которую называют условно-патогенной инфекцией, широко распространена в больницах. A. baumanii представляет очень небольшой риск для здоровых людей; [36] однако факторы, повышающие риск заражения, включают:
- Ослабленная иммунная система
- Хроническая болезнь легких
- Сахарный диабет
- Увеличено пребывание в больнице
- Заболевание, требующее использования аппарата искусственной вентиляции легких
- Лечение открытой раны в больнице
- Лечение, требующее инвазивных устройств, таких как мочевые катетеры
A. baumanii может передаваться через прямой контакт с поверхностями, предметами и кожей зараженных людей. [23]
Завоз A. baumannii и последующее присутствие в больницах хорошо задокументированы. [37] A. baumannii обычно вводится в больницу колонизированным пациентом. Благодаря своей способности выживать на искусственных поверхностях и сопротивляться высыханию, он может оставаться и, возможно, инфицировать новых пациентов в течение некоторого времени. Предполагается, что рост baumannii будет предпочтительным в больничных условиях из-за постоянного использования антибиотиков пациентами в больнице. [38] Acinetobacter может передаваться от человека к человеку или при контакте с загрязненными поверхностями. [39] Acinetobacter может проникнуть через открытые раны, катетеры и дыхательные трубки. [40]В исследовании, проведенном в европейских отделениях интенсивной терапии в 2009 году, было обнаружено , что A. baumannii является причиной 19,1% случаев вентилятор-ассоциированной пневмонии. [41]
| Страна | Ссылка |
|---|---|
| Австралия | [42] [43] |
| Бразилия | [44] [45] [46] [47] |
| Китай | [48] [49] [50] [51] |
| Германия | [52] [53] [54] |
| Индия | [55] [56] [57] |
| Южная Корея | [58] [59] [60] [61] |
| объединенное Королевство | [62] [63] |
| Соединенные Штаты | [64] [65] [66] [67] |
Ссылки [ править ]
- ^ Parte, AC «Acinetobacter» . LPSN .
- ^ Лин, Мин-Фэн; Лан, Чунг-Ю (2014). «Устойчивость к противомикробным препаратам в Acinetobacter baumannii: от скамейки к постели» . Всемирный журнал клинических случаев . 2 (12): 787–814. DOI : 10,12998 / wjcc.v2.i12.787 . PMC 4266826 . PMID 25516853 .
- ^ Antunes, Луиза CS; Виска, Паоло; Таунер, Кевин Дж. (Август 2014 г.). « Acinetobacter baumannii : эволюция глобального патогена» . Возбудители и болезни . 71 (3): 292–301. DOI : 10.1111 / 2049-632X.12125 . PMID 24376225 .
- ^ а б Йом, Джинки; Шин, Джи-Хён; Ян, Джи-Ён; Ким, Чонмин; Хван, Гым-Сук; Банди, Джейкоб Гай (6 марта 2013 г.). «Профилирование метаболитов планктонных и биопленочных клеток на основе ЯМР 1H в Acinetobacter baumannii 1656-2» . PLOS ONE . 8 (3): e57730. Bibcode : 2013PLoSO ... 857730Y . DOI : 10.1371 / journal.pone.0057730 . PMC 3590295 . PMID 23483923 .
- ^ а б Маккуири, Кристин Н .; Киркуп, Бенджамин С .; Си Юаньчжэн; Барлоу, Мириам; Actis, Luis A .; Ремесло, Дэвид В .; Журавски, Даниэль В. (30 июня 2012 г.). «Внеклеточный стресс и липополисахариды модулируют подвижность, связанную с поверхностью Acinetobacter baumannii » . Журнал микробиологии . 50 (3): 434–443. DOI : 10.1007 / s12275-012-1555-1 . PMID 22752907 . S2CID 18294862 .
- ^ Гаррити, Г., изд. (2000). «Пункты A и B: Proteobacteria». Руководство Берджи по систематической бактериологии . 2 (2-е изд.). Нью-Йорк: Спрингер. п. 454. ISBN 978-0-387-95040-2.
- ^ а б О'Ши, МК (май 2012 г.). «Acinetobacter в современной войне». Международный журнал противомикробных агентов . 39 (5): 363–75. DOI : 10.1016 / j.ijantimicag.2012.01.018 . PMID 22459899 .
- ^ Gerner-Smidt, P (октябрь 1992). «Риботипирование комплекса Acinetobacter calcoaceticus - Acinetobacter baumannii » . Журнал клинической микробиологии . 30 (10): 2680–5. DOI : 10.1128 / JCM.30.10.2680-2685.1992 . PMC 270498 . PMID 1383266 .
- ↑ Rice, LB (15 апреля 2008 г.). «Федеральное финансирование исследования устойчивости к противомикробным препаратам внутрибольничных патогенов: нет ESKAPE» . Журнал инфекционных болезней . 197 (8): 1079–81. DOI : 10.1086 / 533452 . PMID 18419525 .
- ↑ Драммонд, Кэти (24 мая 2010 г.). «Пентагон против супербактерий, убивающих войска: сопротивление бесполезно» . Wired.com . Condé Nast . Проверено 8 апреля 2013 года .
- ^ Чой, Чул Хи; Ли, Джун Сик; Ли, Ю Чоль; Пак, Тэ Ин; Ли, Дже Чул (2008). « Acinetobacter baumannii проникает в эпителиальные клетки, а белок А внешней мембраны опосредует взаимодействия с эпителиальными клетками» . BMC Microbiology . 8 (1): 216. DOI : 10,1186 / 1471-2180-8-216 . PMC 2615016 . PMID 19068136 .
- ↑ Ли, Джун Сик; Чой, Чул Хи; Ким, Чон Ук; Ли, Дже Чул (23 июня 2010 г.). « Белок А внешней мембраны Acinetobacter baumannii вызывает гибель дендритных клеток за счет нацеливания на митохондрии». Журнал микробиологии . 48 (3): 387–392. DOI : 10.1007 / s12275-010-0155-1 . PMID 20571958 . S2CID 33040805 .
- ^ Шепутене, Вайда; Повилонис, Юстас; Сужеделене, Эдита (апрель 2012 г.). «Новые варианты островов устойчивости к AbaR с общим позвоночником в изолятах Acinetobacter baumannii европейского клона II» . Противомикробные препараты и химиотерапия . 56 (4): 1969–1973. DOI : 10,1128 / AAC.05678-11 . PMC 3318354 . PMID 22290980 .
- ^ Сообщение, V .; Белый, PA; Холл, РМ (7 апреля 2010 г.). «Эволюция островков устойчивости к геному AbaR-типа у Acinetobacter baumannii с множественной устойчивостью к антибиотикам » . Журнал антимикробной химиотерапии . 65 (6): 1162–1170. DOI : 10,1093 / JAC / dkq095 . PMID 20375036 .
- ^ Магнит, S; Курвалин, П; Ламберт, Т. (декабрь 2001 г.). « Оттокный насос резистентно- клубенькового типа деления клеток, участвующий в устойчивости к аминогликозидам в штамме Acinetobacter baumannii BM4454» . Противомикробные препараты и химиотерапия . 45 (12): 3375–80. DOI : 10,1128 / aac.45.12.3375-3380.2001 . PMC 90840 . PMID 11709311 .
- ^ Чау, SL; Чу, Ю.В.; Houang, ET (октябрь 2004 г.). «Новая система устойчивости-клубеньков-оттока клеток-делений AdeDE в группе 3 геномной ДНК Acinetobacter» . Противомикробные препараты и химиотерапия . 48 (10): 4054–5. DOI : 10,1128 / aac.48.10.4054-4055.2004 . PMC 521926 . PMID 15388479 .
- ^ Шарма, Раджникант; Арья, Санкальп; Патил, Суприя Дипак; Шарма, Атин; Джайн, Прадип Кумар; Навани, Навин Кумар; Патания, Ранджана (01.01.2014). «Идентификация новых регуляторных малых РНК в Acinetobacter baumannii » . PLOS ONE . 9 (4): e93833. Bibcode : 2014PLoSO ... 993833S . DOI : 10.1371 / journal.pone.0093833 . ISSN 1932-6203 . PMC 3976366 . PMID 24705412 .
- ^ Перишон, Бруно; Гуссар, Сильви; Валевски, Виолайн; Кризова, Ленка; Серкейра, Густаво; Мерфи, Шерил; Фельдгарден, Майкл; Вортман, Дженнифер; Клермон, Доминик; Немец, Александр; Курвалин, Патрис (февраль 2014 г.). «Идентификация 50 β-лактамаз класса D и 65 цефалоспориназ, производных Acinetobacter, в Acinetobacter spp» . Противомикробные препараты и химиотерапия . 58 (2): 936–949. DOI : 10,1128 / AAC.01261-13 . PMC 3910822 . PMID 24277043 .
- ^ Хиггинс, PG; Pérez-Llarena, FJ; Зандер, Э; Фернандес, А; Боу, G; Зайферт, H (25 февраля 2013 г.). «OXA-235, новая бета-лактамаза класса D, участвующая в устойчивости к карбапенемам у Acinetobacter baumannii » . Противомикробные препараты и химиотерапия . 57 (5): 2121–6. DOI : 10,1128 / AAC.02413-12 . PMC 3632948 . PMID 23439638 .
- ^ Espinal, P; Марти, S; Вила, Дж. (Январь 2012 г.). «Влияние образования биопленки на выживаемость Acinetobacter baumannii на сухих поверхностях». Журнал больничной инфекции . 80 (1): 56–60. DOI : 10.1016 / j.jhin.2011.08.013 . PMID 21975219 .
- ^ Tomaras, AP; Дорси, CW; Эдельманн, RE; Actis, LA (декабрь 2003 г.). «Прикрепление и формирование биопленки на абиотических поверхностях с помощью Acinetobacter baumannii : участие новой системы сборки шаперон-ашер пилей». Микробиология . 149 (Pt 12): 3473–84. DOI : 10.1099 / mic.0.26541-0 . PMID 14663080 .
- ^ Уортингтон, RJ; Ричардс, Дж. Дж .; Меландер, К. (7 октября 2012 г.). «Низкомолекулярный контроль бактериальных биопленок» . Органическая и биомолекулярная химия . 10 (37): 7457–74. DOI : 10.1039 / c2ob25835h . PMC 3431441 . PMID 22733439 .
- ^ a b "Что такое Acinetobacter Baumannii?" . Ежедневное здоровье . Проверено 18 апреля 2017 года .
- ^ Вс, СН; Ван, JT; Сюн, Калифорния ; Chien, LJ; и другие. (2012). «Увеличение числа устойчивых к карбапенемам инфекций Acinetobacter baumannii в больницах неотложной помощи на Тайване: ассоциация с использованием противомикробных препаратов в больницах» . PLOS One . 7 (5): e37788. Bibcode : 2012PLoSO ... 737788S . DOI : 10.1371 / journal.pone.0037788 . PMC 3357347 . PMID 22629456 .
- ^ Abbo, A; Навон-Венеция, S; Хаммер-Мунц, О; Кричали, Т; и другие. (Январь 2005 г.). « Acinetobacter baumannii с множественной лекарственной устойчивостью » . Возникающие инфекционные заболевания . 11 (1): 22–9. DOI : 10.3201 / eid1101.040001 . PMC 3294361 . PMID 15705318 .
- ^ Spapen, H; Джейкобс, Р. Ван Горп, В; Troubleyn, J; и другие. (25 мая 2011 г.). «Почечные и неврологические побочные эффекты колистина у пациентов в критическом состоянии» . Летопись интенсивной терапии . 1 (1): 14. DOI : 10,1186 / 2110-5820-1-14 . PMC 3224475 . PMID 21906345 .
- ^ «Acinetobacter в медицинских учреждениях» . CDC . Проверено 8 апреля 2013 года .
- ^ «Он умирал. Антибиотики не работали. Затем врачи попробовали забытое лечение» . Мать Джонс . Проверено 17 мая 2018 .
- ^ Альтамирано, Фернандо Л. Гордилло; Барр, Джереми Дж. (20 марта 2019 г.). «Фаговая терапия в эру постантибиотиков» . Обзоры клинической микробиологии . 32 (2). DOI : 10.1128 / CMR.00066-18 . PMC 6431132 . PMID 30651225 .
- ^ Гордилло Альтамирано, Фернандо; Форсайт, Джон Х .; Патва, Рузин; Костулиас, Ксения; Трим, Майкл; Субеди, Динеш; Арчер, Стюарт К .; Моррис, Фэй С.; Оливейра, Коди; Килти, Луиза; Корнеев, Денис; О'Брайан, Мойра К .; Литгоу, Тревор Дж .; Пелег, Антон Ю .; Барр, Джереми Дж. (Февраль 2021 г.). «Устойчивые к бактериофагам Acinetobacter baumannii повторно чувствительны к противомикробным препаратам». Природная микробиология . 6 (2): 157–161. DOI : 10.1038 / s41564-020-00830-7 . PMID 33432151 .
- ↑ Рэй, Тирнан (13 марта 2020 г.). «Глубокое обучение Массачусетского технологического института нашло антибиотик для микроба, который ничто другое не могло убить» . ZDNet .
- ^ Стоукс, Джонатан М .; Ян, Кевин; Суонсон, Кайл; Цзинь, Венгонг; Кубильос-Руис, Андрес; Donghia, Nina M .; MacNair, Craig R .; Френч, Шон; Carfrae, Lindsey A .; Блум-Акерман, Зохар; Тран, Виктория М .; Чиаппино-Пепе, Ануш; Бадран, Ахмед Х .; Эндрюс, Ян У .; Чори, Эмма Дж .; Церковь, Джордж М .; Браун, Эрик Д .; Jaakkola, Tommi S .; Барзилай, Регина; Коллинз, Джеймс Дж. (20 февраля 2020 г.). «Подход с глубоким обучением к открытию антибиотиков» . Cell . 180 (4): 688–702.e13. DOI : 10.1016 / j.cell.2020.01.021 . PMID 32084340 .
- ^ "Армейская медицинская логистика" (PDF) . FM 4-02.1 . Соединенные Штаты. Архивировано из оригинального (PDF) 23 марта 2013 года . Проверено 8 апреля 2013 года .
- ^ Meghoo, Colin A .; Деннис, Джеймс В .; Туман, Кэролайн; Фанг, Раймонд (май 2012 г.). «Диагностика и ведение эвакуированных раненых с повреждениями сосудов шейки матки в результате взрывов боеприпасов» . Журнал сосудистой хирургии . 55 (5): 1329–1337. DOI : 10.1016 / j.jvs.2011.11.125 . PMID 22325667 .
- ^ Мюррей, Клинтон К. (март 2008 г.). «Эпидемиология инфекций, связанных с боевыми травмами в Ираке и Афганистане». Журнал травмы: травмы, инфекции и неотложная помощь . 64 (Приложение): S232 – S238. DOI : 10.1097 / TA.0b013e318163c3f5 . PMID 18316967 .
- ^ « Acinetobacter в медицинских учреждениях» . Центры по контролю и профилактике заболеваний . Министерство здравоохранения и социальных служб США . Проверено 18 апреля 2017 года .
- ^ Джонс, Анна; Морган, Дилис; Уолш, Аманда; Тертон, Джейн; Ливермор, Дэвид; Питт, Тайрон; Грин, Энди; Гилл, Мартин; Мортибой, Дебора (июнь 2006 г.). «Импорт инфекций Acinetobacter spp. С множественной лекарственной устойчивостью, пострадавшие из Ирака». Ланцетные инфекционные болезни . 6 (6): 317–318. DOI : 10.1016 / S1473-3099 (06) 70471-6 . PMID 16728314 .
- ^ Dijkshoorn, Lenie; Немец, Александр; Зейферт, Харальд (декабрь 2007 г.). «Возрастающая угроза в больницах: Acinetobacter baumannii с множественной лекарственной устойчивостью». Обзоры природы микробиологии . 5 (12): 939–951. DOI : 10.1038 / nrmicro1789 . PMID 18007677 . S2CID 3446152 .
- ^ «Acinetobacter в медицинских учреждениях - HAI - CDC» . www.cdc.gov . Проверено 2 апреля 2018 .
- ^ Acinetobacter baumannii с множественной лекарственной устойчивостью (MDRAB) ». ВОЗ Регион Западной части Тихого океана, WPRO | Регион Западной части Тихого океана ВОЗ, 1 ноября 2010 г., www.wpro.who.int/mediacentre/factsheets/fs_20101102/en/.
- ^ Koulenti, Деспоина; Лиссабон, Тьяго; Брун-Бюиссон, Кристиан; Крюгер, Вольфганг; Macor, Антонио; Соле-Виолан, Хорди; Диас, Эмили; Топели, Арзу; ДеВаэле, Ян; Карнейро, Антонио; Мартин-Лёчес, Игнасио; Армаганидис, Апостолос; Релло, Хорди; Исследовательская группа EU-VAP / CAP (август 2009 г.). «Спектр практики диагностики внутрибольничной пневмонии у пациентов, которым требуется искусственная вентиляция легких в европейских отделениях интенсивной терапии». Реанимационная медицина . 37 (8): 2360–2369. DOI : 10.1097 / CCM.0b013e3181a037ac . PMID 19531951 . S2CID 205537662 .
- ^ Ng, J .; Госбелл, И.Б .; Келли, JA; Бойл, MJ; Фергюсон, Дж. К. (6 сентября 2006 г.). «Лечение мультирезистентных инфекций центральной нервной системы Acinetobacter baumannii с помощью внутрижелудочкового или интратекального колистина: серия случаев и обзор литературы» . Журнал антимикробной химиотерапии . 58 (5): 1078–1081. DOI : 10,1093 / JAC / dkl347 . PMID 16916866 .
- ^ Фарруджа, Даниэль Н .; Эльбурн, Лиам Д.Х. Hassan, Karl A .; Eijkelkamp, Bart A .; Тету, Саша Г .; Браун, Мелисса Х .; Shah, Bhumika S .; Пелег, Антон Ю .; Mabbutt, Bridget C .; Полсен, Ян Т .; де Креси-Лагар, Валери (19 марта 2013 г.). «Полный геном и феном приобретенных сообществом Acinetobacter baumannii» . PLOS ONE . 8 (3): e58628. Bibcode : 2013PLoSO ... 858628F . DOI : 10.1371 / journal.pone.0058628 . PMC 3602452 . PMID 23527001 .
- ^ Werneck, JS; Picao, RC; Carvalhaes, CG; Cardoso, JP; Гейлс, AC (3 декабря 2010 г.). «Acinetobacter baumannii, продуцирующий OXA-72, в Бразилии: отчет о болезни» . Журнал антимикробной химиотерапии . 66 (2): 452–454. DOI : 10,1093 / JAC / dkq462 . PMID 21131320 .
- ^ Мартинс, N .; Мартинс, ИС; Фрейтас, Западная Вирджиния; Matos, JA; Magalhães, ACG; Жирао, VBC; Диас, RCS; Соуза, ТК; Пеллегрино, ФЛПК; Коста, LD; Boasquevisque, CHR; Nouér, SA; Райли, LW; Санторо-Лопес, G .; Морейра, Б.М. (июнь 2012 г.). «Тяжелая инфекция реципиента легкого, вызванная донором устойчивой к карбапенемам Acinetobacter baumannii» . Инфекционное заболевание трансплантата . 14 (3): 316–320. DOI : 10.1111 / j.1399-3062.2011.00701.x . PMC 3307813 . PMID 22168176 .
- ^ Суперти, Сильвана Варгас; Мартинс, Даниэла де Соуза; Caierão, Juliana; Соареш, Фабиана да Силва; Прохнов, Таиса; Заваски, Александр Прен (апрель 2009 г.). «Признаки эволюции устойчивости к карбапенему через гетерорезистентность как промежуточную стадию у Acinetobacter baumannii после введения карбапенема» . Revista do Instituto de Medicina Tropical de São Paulo . 51 (2): 111–113. DOI : 10.1590 / s0036-46652009000200010 . PMID 19390741 .
- ^ Gionco, B .; Pelayo, JS; Venancio, EJ; Cayo, R .; Gales, AC; Каррара-Маррони, ИП (26 июня 2012 г.). «Обнаружение OXA-231, нового варианта blaOXA-143, в Acinetobacter baumannii из Бразилии: отчет о болезни» . Журнал антимикробной химиотерапии . 67 (10): 2531–2532. DOI : 10,1093 / JAC / dks223 . PMID 22736746 .
- ^ Чжао, WS; Лю, GY; Mi, ZH; Чжан Ф. (март 2011 г.). «Сосуществование blaOXA-23 с armA и новой мутацией gyrA в изоляте Acinetobacter baumannii, устойчивом к пандлекарствам, из крови пациента с гематологическим заболеванием в Китае». Журнал госпитальной инфекции . 77 (3): 278–279. DOI : 10.1016 / j.jhin.2010.11.006 . PMID 21281989 .
- ^ Сяо, Южная Каролина; Zhu, SH; Xia, ZF; Ma, B; Ченг, Д.С. (ноябрь 2009 г.). «Успешное лечение критического больного ожоговой с упрямой гипергликемии и септического шока от штаммов сковорода лекарственной устойчивостью». Монитор медицинской науки . 15 (11): CS163-5. PMID 19865060 .
- ^ Ву, Юй-Чин; Се, Те-Чун; Сунь, Шунг-Шунг; Ван, Чжи-Сю; Йен, Го-Ян; Линь, Ю-И; Као, Чиа-Хунг (ноябрь 2009 г.). «Неожиданное образование облаков на сцинтиграфии с галлием-67: обнаружение подкожного абсцесса под кожей с нормальным внешним видом у пациента в коматозном состоянии в условиях интенсивной терапии». Американский журнал медицинских наук . 338 (5): 388. DOI : 10,1097 / MAJ.0b013e3181a6dd36 . PMID 19770790 .
- ^ Дуань, Сяоцзюнь; Ян, Лю; Ся, Пэйюань (26 августа 2009 г.). «Септический артрит колена, вызванный устойчивым к антибиотикам Acinetobacter baumannii у пациента подагрой: отчет о редком случае». Архив ортопедической и травматологической хирургии . 130 (3): 381–384. DOI : 10.1007 / s00402-009-0958-х . PMID 19707778 . S2CID 37311301 .
- ^ Вагнер, JA; Nenoff, P; Хэндрик, Вт; Реннер, Р; Саймон, Дж; Трейдлер, Р. (февраль 2011 г.). «Некротический фасциит, вызванный Acinetobacter baumannii : отчет о болезни». Der Hautarzt; Zeitschrift für Dermatologie, Venerologie, und Verwandte Gebiete (на немецком языке). 62 (2): 128–30. DOI : 10.1007 / s00105-010-1962-3 . PMID 20835812 .
- ^ Айвазова, В; Кайнер, Ф; Friese, K; Милонас, I (январь 2010 г.). « Инфекция Acinetobacter baumannii во время беременности и послеродового периода». Архив гинекологии и акушерства . 281 (1): 171–4. DOI : 10.1007 / s00404-009-1107-Z . PMID 19462176 . S2CID 23112180 .
- ^ Шульте, B; Гёрке, C; Weyrich, P; Грёбнер, С; Bahrs, C; Wolz, C; Autenrieth, IB; Боргманн, S (декабрь 2005 г.). «Клональное распространение устойчивых к меропенему штаммов Acinetobacter baumannii в больницах Средиземноморского региона и передача в Юго-Западную Германию». Журнал больничной инфекции . 61 (4): 356–7. DOI : 10.1016 / j.jhin.2005.05.009 . PMID 16213625 .
- ^ Piparsania, S; Раджпут, N; Бхатамбаре, Дж. (Сентябрь – октябрь 2012 г.). «Внутрижелудочковый полимиксин B для лечения неонатального менинго-вентрикулита, вызванного мультирезистентным Acinetobacter baumannii - отчет о случае и обзор литературы». Турецкий журнал педиатрии . 54 (5): 548–54. PMID 23427525 .
- ^ Джон, TM; Джейкоб, CN; Ittycheria, CC; Джордж, AM; Jacob, AG; Субраманиям, S; Puthiyaveettil, J; Джаяпракаш, Р. (март 2012 г.). «Синдром активации макрофагов после сепсиса Acinetobacter baumannii » . Международный журнал инфекционных болезней . 16 (3): e223–4. DOI : 10.1016 / j.ijid.2011.12.002 . PMID 22285540 .
- ^ Шарма, А; Шариф, М; Тукрал, СС; Шах, А (октябрь 2005 г.). «Хроническая внебольничная пневмония, вызванная Acinetobacter, которая медленно реагировала на рифампицин в противотуберкулезном режиме». Журнал инфекции . 51 (3): e149–52. DOI : 10.1016 / j.jinf.2004.12.003 . PMID 16230195 .
- ^ Jeong, HL; Йом, JS; Park, JS; Seo, JH; Парк, ЕС; Lim, JY; Park, CH; Ву, ХО; Юн, HS (июль – август 2011 г.). « Выделение Acinetobacter baumannii в спинномозговой жидкости у новорожденного с лихорадкой». Турецкий журнал педиатрии . 53 (4): 445–7. PMID 21980849 .
- ^ Хонг, КБ; О, HS; Песня, JS; Lim, JH; Канг, Дания; Сын, IS; Парк, JD; Kim, EC; Ли, HJ; Цой, EH (июль 2012 г.). «Расследование и борьба со вспышкой имипенем-резистентной инфекции Acinetobacter baumannii в педиатрическом отделении интенсивной терапии». Журнал детских инфекционных болезней . 31 (7): 685–90. DOI : 10,1097 / inf.0b013e318256f3e6 . PMID 22466324 . S2CID 1078450 .
- ^ Ли, YK; Ким, JK; Ой, SE; Ли, Дж; Но, JW (декабрь 2009 г.). «Успешная терапия блокировкой антибиотиков у пациентов с рефрактерным перитонитом». Клиническая нефрология . 72 (6): 488–91. DOI : 10.5414 / cnp72488 . PMID 19954727 .
- ^ Ли, SY; Ли, JW; Чон, округ Колумбия; Chung, SY; Чанг, Д.С.; Канг, Дж. Х. (август 2008 г.). «Менингит с множественной лекарственной устойчивостью, вызванный Acinetobacter, у 3-летнего мальчика, получавшего внутривенное введение колистина». Международная педиатрия . 50 (4): 584–5. DOI : 10.1111 / j.1442-200x.2008.02677.x . PMID 18937759 . S2CID 42715424 .
- ^ Адамс, D; Да, L; Риммер, JA; Уильямс, Р. Мартин, H; Овингтон, К. (февраль 2011 г.). «Расследование и лечение вспышки A. Baumannii в отделении интенсивной терапии». Британский журнал медсестер . 20 (3): 140, 142, 144–7. DOI : 10.12968 / bjon.2011.20.3.140 . PMID 21378633 .
- ^ Pencavel, TD; Сингх-Рейнджер, G; Криннион, Дж. Н. (май 2006 г.). «Консервативное лечение ранней инфекции трансплантата аорты, вызванной Acinetobacter baumanii». Анналы сосудистой хирургии . 20 (3): 415–7. DOI : 10.1007 / s10016-006-9030-2 . PMID 16602028 . S2CID 38699601 .
- ^ Густен, WM; Хансен, EA; Cunha, BA (январь – февраль 2002 г.). « Псевдоменингит, вызванный Acinetobacter baumannii ». Сердце и легкие . 31 (1): 76–8. DOI : 10.1067 / mhl.2002.120258 . PMID 11805753 .
- ^ Фитцпатрик, Массачусетс; Esterly, JS; Постельник, MJ; Саттон, SH (июль – август 2012 г.). «Успешное лечение перитонита перитонеального диализа Acinetobacter baumannii с широкой лекарственной устойчивостью с внутрибрюшинным полимиксином B и ампициллин-сульбактамом». Летопись фармакотерапии . 46 (7–8): e17. DOI : 10,1345 / aph.1r086 . PMID 22811349 . S2CID 20744216 .
- ^ Патель, JA; Пачеко, С. М.; Постельник, М; Саттон, С. (15 августа 2011 г.). «Длительная тройная терапия стойкого вентрикулита, вызванного Acinetobacter baumannii с множественной лекарственной устойчивостью ». Американский журнал фармации системы здравоохранения . 68 (16): 1527–31. DOI : 10,2146 / ajhp100234 . PMID 21817084 .
- ^ Салливан, DR; Щиты, Дж; Нетцер, Г. (июнь 2010 г.). «Смертельный случай некротического фасциита Acinetobacter baumannii с множественной лекарственной устойчивостью ». Американский хирург . 76 (6): 651–3. DOI : 10.1177 / 000313481007600636 . PMID 20583528 . S2CID 41059355 .