| Справиться реакция | |
|---|---|
| Названный в честь | Артур Коуп |
| Тип реакции | Реакция элиминации |
| Идентификаторы | |
| Портал органической химии | справиться-устранение |
| Идентификатор онтологии RSC | RXNO: 0000539 |
Коп реакции или Копы ликвидация , разработанная Arthur C. Коп , является реакция элиминирования из N-оксида с образованием алкена и гидроксиламина . [1]
Механизм и приложения [ править ]
Механизм реакции включает внутримолекулярной 5-членное циклическое переходное состояние , [1] приводит к син элиминации продукта, Е я Pathway . Эта органическая реакция тесно связана с ликвидацией Hofmann , [2] но базой является частью уходящей группы . Оксид амина получают окислением соответствующего амина окислителем, таким как m CPBA . Фактическое устранение просто требует тепла.
Иллюстрацией реакции Копа является синтез метиленциклогексана : [2]
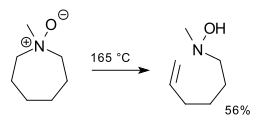
Пиперидины устойчивы к внутримолекулярной реакции Коупа [3] [4] [5], но с пирролидином и кольцами размером 7 и более продукт реакции представляет собой ненасыщенный гидроксиламин. Этот результат согласуется с 5-членным циклическим переходным состоянием .
Обратная реакция [ править ]
Сообщалось об обратном или ретро-копе-элиминировании, при котором N, N-дизамещенный гидроксиламин реагирует с алкеном с образованием третичного N-оксида. [6] [7] Реакция представляет собой форму гидроаминирования и может быть расширена до использования незамещенного гидроксиламина, в этом случае образуются оксимы . [8]
Связанные процессы [ править ]
Сульфоксиды могут подвергаться практически идентичной реакции с образованием сульфеновых кислот, что важно в антиоксидантной химии чеснока и других растений рода Allium . Селеноксиды также подвергаются удалению селеноксида . Остальные реакции E i протекают аналогично.
Ссылки [ править ]
- ^ Питер К. Эстлес, Саймон В. Мортлок, Эрик Дж. Томас (1991). «Удаление Cope, удаление сульфоксида и связанные с ним термические реакции». Комплексный органический синтез . 6 . С. 1011–1039. DOI : 10.1016 / B978-0-08-052349-1.00178-5 . ISBN 9780080523491.CS1 maint: uses authors parameter (link)
- ^ Коп, Артур С .; Циганек, Энгельберт (1963). «Метиленциклогексан и гидрохлорид N, N-диметилгидроксиламина». Органический синтез . 4 : 612. DOI : 10,15227 / orgsyn.039.0040 .
- ^ Марш, Джерри; Смит, Майкл Б. (2007). Продвинутая органическая химия марта: реакции, механизмы и структура (6-е изд.). Wiley-Interscience. п. 1525 . ISBN 978-0-471-72091-1.
- ^ Окиси аминов. VIII. Циклические олефины среднего размера из оксидов аминов и четвертичных гидроксидов аммония Артур К. Коуп, Энгельберт Циганек, Чарльз Ф. Хауэлл, Эдвард Э. Швейцер J. Am. Chem. Soc. , 1960 , 82 (17), стр 4663-4669 DOI : 10.1021 / ja01502a053
- ^ Окиси аминов. VII. Термическое разложение N-оксидов N-метилазациклоалканов Артур К. Коуп, Норман А. ЛеБель; Варенье. Chem. Soc. ; 1960 ; 82 (17); 4656-4662. DOI : 10.1021 / ja01502a052
- ^ Циганек, Энгельберт; Прочтите, Джон М .; Калабрезе, Джозеф К. (сентябрь 1995 г.). «Обратные реакции элиминации Коупа. 1. Механизм и область применения». Журнал органической химии . 60 (18): 5795–5802. DOI : 10.1021 / jo00123a013 .
- ^ Cigánek Энгельберт (сентябрь 1995). «Реакции обратного элиминирования Коупа. 2. Применение к синтезу». Журнал органической химии . 60 (18): 5803–5807. DOI : 10.1021 / jo00123a014 .
- ^ Beauchemin, Андре М .; Моран, Джозеф; Лебрен, Мари-Ева; Сеген, Екатерина; Димитриевич, Елена; Чжан, Лили; Горельский, Сергей И. (8 февраля 2008 г.). «Межмолекулярное гидроаминирование копе-типа алкенов и алкинов». Angewandte Chemie . 120 (8): 1432–1435. DOI : 10.1002 / ange.200703495 .