| Имена | |||
|---|---|---|---|
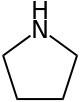
| Предпочтительное название IUPAC Пирролидин | |||
| Другие имена Azolidine азациклопентан тетрагидропиррол проламины Azolane | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 102395 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004.227 | ||
| Номер ЕС |
| ||
| 1704 | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1922 г. | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 4 H 9 N | |||
| Молярная масса | 71,123 г · моль -1 | ||
| Внешность | Бесцветная прозрачная жидкость | ||
| Плотность | 0,866 г / см 3 | ||
| Температура плавления | -63 ° С (-81 ° F, 210 К) | ||
| Точка кипения | 87 ° С (189 ° F, 360 К) | ||
| Смешиваемый | |||
| Кислотность (p K a ) | 11,27 (p K a конъюгированной кислоты в воде), [1] 19,56 (p K a конъюгированной кислоты в ацетонитриле) [2] | ||
| -54,8 · 10 −6 см 3 / моль | |||
Показатель преломления ( n D ) | 1.4402 при 28 ° C | ||
| Опасности | |||
| Основные опасности | легковоспламеняющийся, вредный, едкий, возможный мутаген | ||
| Паспорт безопасности | Паспорт безопасности | ||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H225 , H302 , H314 , H318 , H332 | ||
Меры предосторожности GHS | Р210 , Р233 , Р240 , Р241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P280 , P301 + 312 , P301 + 330 + 331 , P303 + 361 + 353 , Р304 + 312 , Р304 + 340 , P305 + 351 + 338 , P310 , P312 , P321 , P330 , P363 , P370 + 378 , P403 + 235 | ||
| NFPA 704 (огненный алмаз) |  3 3 1 | ||
| точка возгорания | 3 ° С (37 ° F, 276 К) | ||
самовоспламенения температуру | 345 ° С (653 ° F, 618 К) | ||
| Родственные соединения | |||
Родственные азотные гетероциклические соединения | Пиррол (ароматический с двумя двойными связями) Пирролин (одна двойная связь) Пирролизидин (два пятиугольных кольца) | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Пирролидин , также известный как тетрагидропиррол , представляет собой органическое соединение с молекулярной формулой (CH 2 ) 4 NH. Это циклический вторичный амин , также классифицируемый как насыщенный гетероцикл . Это бесцветная жидкость, смешиваемая с водой и большинством органических растворителей. Он имеет характерный запах, который был описан как «аммиачный, рыбный, похожий на запах моллюсков». [3] Помимо самого пирролидина, известно много замещенных пирролидинов.
Производство и синтез [ править ]
Промышленное производство [ править ]
Промышленным способом пирролидин получают реакцией 1,4-бутандиола и аммиака при температуре 165–200 ° C и давлении 17–21 МПа в присутствии катализатора на основе оксидов кобальта и никеля , нанесенного на оксид алюминия . [4]
Реакцию проводят в жидкой фазе в реакторе непрерывного действия с трубчатым или пучковым пучком труб, который работает по методу циркулирующего газа. Катализатор выполнен в виде неподвижного слоя, и конверсия осуществляется в режиме нисходящего потока. Продукт получают после многоступенчатой очистки и разделения экстрактивной и азеотропной перегонкой . [4]
Лабораторный синтез [ править ]
В лаборатории пирролидин обычно синтезировали путем обработки 4-хлорбутан-1-амина сильным основанием:
Происшествие [ править ]
Многие модификации пирролидина встречаются в естественной и синтетической химии. Кольцевая структура пирролидина присутствует во многих природных алкалоидах, таких как никотин и гигрин . Он содержится во многих лекарствах, таких как проциклидин и бепридил . Он также составляет основу соединений рацетама ( например, пирацетама , анирацетама ). Эти аминокислоты пролина и гидроксипролина , в некотором смысле структурного, производные пирролидина.
- Никотин содержит кольцо N- метилпирролидина, связанное с кольцом пиридина.
Реакции [ править ]
Пирролидин - это основа. Его основность типична для других диалкиламинов. [5] По сравнению со многими вторичными аминами, пирролидин отличается своей компактностью, что является следствием его циклической структуры.
Пирролидин используется в качестве строительного блока при синтезе более сложных органических соединений. Он используется для активации кетонов и альдегидов в направлении нуклеофильного присоединения путем образования енаминов (например, используется при алкилировании енаминов Stork ): [6]
Ссылки [ править ]
- Перейти ↑ Hall, HK (1957). «Соотношение основных сильных сторон аминов». Журнал Американского химического общества . 79 (20): 5441–5444. DOI : 10.1021 / ja01577a030 .
- ^ Kaljurand, I .; Kütt, A .; Sooväli, L .; Родима, Т .; Мяэметс, В .; Leito, I .; Коппель, ИА (2005). «Расширение самосогласованной спектрофотометрической шкалы основности в ацетонитриле до полного диапазона 28 единиц pKa: объединение различных шкал основности». Журнал органической химии . 70 (3): 1019–1028. DOI : 10.1021 / jo048252w . PMID 15675863 .
- ^ Пирролидин , The Good Company Ароматы
- ^ a b Боу Чедид, Роланд; Мельдер, Иоганн-Петер; Досталек, Роман; Пастре, Йорг; Тан, Айк Мем. «Способ получения пирролидина» . Патенты Google . BASF SE . Дата обращения 5 июля 2019 .
- Перейти ↑ HK Hall, Jr. (1957). «Соотношение основных сильных сторон аминов». Варенье. Chem. Soc . 79 (20): 5441. DOI : 10.1021 / ja01577a030 .
- ^ RB Woodward , IJ Пэчтер и ML Scheinbaum (1974). «2,2- (Триметилендитио) циклогексанон» . Органический синтез . 54 : 39.CS1 maint: несколько имен: список авторов ( ссылка ); Сборник , 6 , с. 1014
Внешние ссылки [ править ]
- СМИ, связанные с пирролидином, на Викискладе?