| Имена | |||
|---|---|---|---|
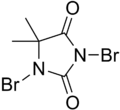
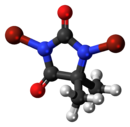
| Название ИЮПАК 1,3-дибром-5,5-диметилгидантоин | |||
| Другие названия DBDMH, дибромантин, дибромодиметилгидантоин | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.938 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 5 H 6 Br 2 N 2 O 2 | |||
| Молярная масса | 285,923 г · моль -1 | ||
| Появление | Белое твердое вещество | ||
| Плотность | 1,36 г / см 3 | ||
| Температура плавления | От 197 до 203 ° C (от 387 до 397 ° F, от 470 до 476 K) | ||
| 0,1 г / 100 мл (20 ° С) | |||
| Опасности | |||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасность | ||
| H301 , H302 , H314 , H317 , H319 , H400 , H410 | |||
| Р260 , Р261 , Р264 , Р270 , P272 , P273 , P280 , P301 + 310 , P301 + 312 , P301 + 330 + 331 , P302 + 352 , P303 + 361 + 353 , Р304 + 340 , P305 + 351 + 338 , Р310 , P321 , P330 , P333 + 313 , P337 + 313 , P363 , P391 , P405 , P501 | |||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
DBDMH (также известный как 1,3-дибр-5,5-диметилгидантоин ) представляет собой органическое соединение , образованное из гетероцикл называемого диметил гидантоином . Это белое кристаллическое соединение с легким запахом брома широко используется в качестве дезинфицирующего средства для очистки питьевой воды , рекреационной очистки воды, в качестве отбеливающего агента на целлюлозно-бумажных комбинатах и для обработки промышленных / коммерческих систем водяного охлаждения. [1] Его действие не связано с использованием хлорноватистой кислоты .
Механизм действия [ править ]
1,3-Дибром-5,5-Диметилгидантоин является источником брома, который эквивалентен бромистоводородной кислоте (HOBr).
- Br 2 X + 2 H 2 O → 2 HOBr + H 2 X
(Где H 2 X - 5,5-диметилгидантоин)
При p K a , равном 8,6, бромистоводородная кислота частично диссоциирует в воде:
- HOBr ⇌ H + + BrO -
Бромистоводородная кислота служит источником Br + , образующего бромид-ионы в процессе дезинфекции:
- HOBr + живые патогены → Br - + мертвые патогены
Образующиеся в результате бромид-ионы могут затем подвергаться окислению до бромистоводородной кислоты в присутствии окислителя достаточной силы, например озона , хлорноватистой кислоты , моноперсульфата калия . Этот процесс повторного окисления обычно называют «активацией» бромид-иона:
- Br - + HOCl → HOBr + Cl -
Ссылки [ править ]
- ^ Дэвид Иоффе, Арье Кампф «Бром, органические соединения» в Энциклопедии химической технологии Кирк-Отмера , 2002, John Wiley & Sons. DOI : 10.1002 / 0471238961.0218151325150606.a01
Внешние ссылки [ править ]
- Паспорт безопасности