| Электрокортикография | |
|---|---|
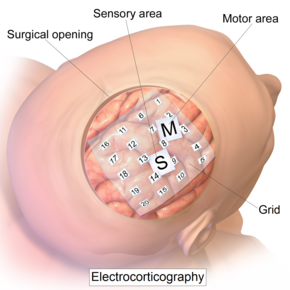 Внутричерепная электродная сетка для электрокортикографии. | |
| Синонимы | Внутричерепная электроэнцефалография |
| Цель | записывать электрическую активность коры головного мозга. (инвазивный) |
Электрокортикография ( ЭКоГ ) или внутричерепная электроэнцефалография ( иЭЭГ ) - это тип электрофизиологического мониторинга, при котором используются электроды, помещаемые непосредственно на обнаженную поверхность мозга, для регистрации электрической активности коры головного мозга . Напротив, обычные электроды электроэнцефалографии (ЭЭГ) контролируют эту активность снаружи черепа. ЭКоГ можно проводить либо в операционной во время операции (интраоперационная ЭКоГ), либо вне операции (внеоперационная ЭКоГ). Потому что краниотомия (хирургический разрез в черепе) требуется для имплантации электродной сетки, ЭКоГ - инвазивная процедура.
История [ править ]
ЭКоГ была впервые предложена в начале 1950-х годов Уайлдером Пенфилдом и Гербертом Джаспером , нейрохирургами из Монреальского неврологического института . [1] Эти двое разработали ЭКоГ как часть своей революционной процедуры в Монреале , хирургического протокола, используемого для лечения пациентов с тяжелой эпилепсией . Корковые потенциалы, зарегистрированные с помощью ЭКоГ, использовались для выявления эпилептогенных зон - областей коры, вызывающих эпилептические припадки.. Затем эти зоны удалялись хирургическим путем из коры во время резекции, разрушая таким образом ткань мозга, в которой возникли эпилептические припадки. Пенфилд и Джаспер также использовали электрическую стимуляцию во время записи ЭКоГ у пациентов, перенесших операцию по эпилепсии под местной анестезией . [2] Эта процедура использовалась для изучения функциональной анатомии головного мозга, картирования речевых областей и определения соматосенсорной и соматомоторной областей коры, которые необходимо исключить из хирургического удаления. Врач по имени Роберт Гэлбрейт Хит также был одним из первых исследователей мозга в Медицинской школе Тулейнского университета. [3] [4]
Электрофизиологические основы [ править ]
Сигналы ЭКоГ состоят из синхронизированных постсинаптических потенциалов (потенциалов локального поля ), записываемых непосредственно с открытой поверхности коры. Потенциалы возникают в основном в кортикальных пирамидных клетках и, следовательно, должны проходить через несколько слоев коры головного мозга, спинномозговую жидкость (CSF), мягкую мозговую оболочку и паутинную оболочку, прежде чем достичь субдуральных записывающих электродов, расположенных непосредственно под твердой мозговой оболочкой (наружной черепной мембраной). . Однако, чтобы достичь электродов скальпа при обычной электроэнцефалограмме (ЭЭГ), электрические сигналы также должны проходить через череп., где потенциалы быстро затухают из-за низкой проводимости кости . По этой причине пространственное разрешение ЭКоГ намного выше, чем у ЭЭГ, что является важным преимуществом визуализации для дооперационного планирования. [5] ЭКоГ обеспечивает временное разрешение примерно 5 мс и пространственное разрешение 1 см. [6]
Используя глубинные электроды, потенциал локального поля дает меру нейронной популяции в сфере радиусом 0,5–3 мм вокруг кончика электрода. [7] При достаточно высокой частоте дискретизации (более 10 кГц) глубинные электроды также могут измерять потенциалы действия . [8] В этом случае пространственное разрешение ограничивается отдельными нейронами, а поле зрения отдельного электрода составляет приблизительно 0,05–0,35 мм. [7]
Процедура [ править ]
Запись ЭКоГ производится с электродов, помещенных на обнаженный кортекс. Чтобы получить доступ к коре головного мозга, хирург должен сначала выполнить краниотомию, удалив часть черепа, чтобы обнажить поверхность мозга. Эта процедура может выполняться либо под общей анестезией, либо под местной анестезией, если для функционального кортикального картирования требуется взаимодействие с пациентом. Затем электроды хирургическим путем имплантируются на поверхность коры головного мозга с учетом результатов предоперационной ЭЭГ и магнитно-резонансной томографии (МРТ). Электроды могут быть размещены вне твердой мозговой оболочки (эпидуральная анестезия) или под твердой мозговой оболочкой (субдурально). Массивы электродов ЭКоГ обычно состоят из шестнадцати стерильных одноразовых электродов из нержавеющей стали, углеродного наконечника, платины, платино-иридиевого сплава.или золотые шариковые электроды, каждый из которых установлен на шарнирном соединении для облегчения позиционирования. Эти электроды прикреплены к вышележащей раме в виде «короны» или «гало». [9] Субдуральные полосковые и сеточные электроды также широко используются в различных размерах, от 4 до 256 [10]электродные контакты. Сетки прозрачные, гибкие и пронумерованы на каждом контакте электрода. Стандартное расстояние между электродами сетки - 1 см; отдельные электроды обычно имеют диаметр 5 мм. Электроды легко прилегают к кортикальной поверхности и имеют достаточно гибкую конструкцию, чтобы гарантировать, что нормальные движения мозга не вызывают травм. Ключевым преимуществом решетчатых и полосовых электродов является то, что они могут быть введены под твердую мозговую оболочку в области коры, не обнаженные при краниотомии. Ленточные электроды и решетки коронок могут использоваться в любой желаемой комбинации. Глубинные электроды также могут использоваться для регистрации активности более глубоких структур, таких как гиппокамп .
DCES [ править ]
Прямая кортикальная электрическая стимуляция (DCES), также известная как картирование корковой стимуляции , часто выполняется одновременно с записью ЭКоГ для функционального картирования коры и идентификации критических корковых структур. [9] При использовании конфигурации коронки переносной биполярный стимулятор с палочкой можно использовать в любом месте электродной решетки. Однако при использовании субдуральной полоски необходимо применять стимуляцию между парами соседних электродов из-за непроводящего материала, соединяющего электроды на сетке. Электрические стимулирующие токи, прикладываемые к коре головного мозга, относительно низкие: от 2 до 4 мА для соматосенсорной стимуляции и около 15 мА для когнитивной стимуляции. [9]Частота стимуляции обычно составляет 60 Гц в Северной Америке и 50 Гц в Европе, и любая плотность заряда более 150 мкКл / см2 вызывает повреждение тканей. [11] [12]
Функции, наиболее часто отображаемые с помощью DCES, - это первичная моторная, первичная сенсорная и языковая. Пациент должен быть внимательным и интерактивным для процедур картирования, хотя участие пациента зависит от каждой процедуры картирования. Языковое отображение может включать наименование, чтение вслух, повторение и понимание устной речи; соматосенсорное картирование требует, чтобы пациент описал ощущения, испытываемые на лице и конечностях, когда хирург стимулирует различные области коры. [9]
Клинические приложения [ править ]
С момента своего развития в 1950-х годах ЭКоГ использовалась для локализации эпилептогенных зон во время дооперационного планирования, картирования корковых функций и прогнозирования успеха эпилептической хирургической резекции. ЭКоГ предлагает несколько преимуществ перед альтернативными методами диагностики:
- Гибкое размещение регистрирующего и стимулирующего электродов [2]
- Может выполняться на любом этапе до, во время и после операции.
- Позволяет осуществлять прямую электрическую стимуляцию головного мозга, определяя критические области коры, которых следует избегать во время операции
- Более высокая точность и чувствительность, чем при записи ЭЭГ скальпа - пространственное разрешение выше, а отношение сигнал / шум лучше из-за более близкого расстояния к нейронной активности
Ограничения ЭКоГ включают:
- Ограниченное время выборки - судороги ( иктальные события) могут не регистрироваться в течение периода записи ЭКоГ.
- Ограниченное поле зрения - размещение электродов ограничено площадью обнаженной коры и временем операции, возможны ошибки при взятии проб
- Запись подвержена влиянию анестетиков, наркотических анальгетиков и самой операции [2]
Неизлечимая эпилепсия [ править ]
Эпилепсия в настоящее время занимает третье место среди наиболее часто диагностируемых неврологических расстройств, от которых страдают около 2,5 миллионов человек только в Соединенных Штатах. [13] Эпилептические припадки являются хроническими и не связаны с какими-либо немедленно излечимыми причинами, такими как токсины или инфекционные заболевания, и могут широко варьироваться в зависимости от этиологии, клинических симптомов и места происхождения в головном мозге. Для пациентов с трудноизлечимой эпилепсией - эпилепсией, не поддающейся лечению противосудорожными препаратами, - хирургическое лечение может быть жизнеспособным вариантом лечения.
- Экстраоперационная ЭКоГ
Прежде чем пациент может быть идентифицирован как кандидат на операцию по резекции, необходимо выполнить МРТ, чтобы продемонстрировать наличие структурного поражения в коре головного мозга, подтвержденное данными ЭЭГ об эпилептогенной ткани. [2] После того, как поражение было идентифицировано, ЭКоГ может быть проведена для определения местоположения и степени поражения и окружающей раздражающей области. ЭЭГ кожи головы, хотя и является ценным диагностическим инструментом, не имеет точности, необходимой для локализации эпилептогенной области. ЭКоГ считается золотым стандартом для оценки нейрональной активности у пациентов с эпилепсией и широко используется для предоперационного планирования для руководства хирургической резекцией поражения и эпилептогенной зоны. [14] [15]Успех операции зависит от точной локализации и удаления эпилептогенной зоны. Данные ЭКоГ оцениваются в отношении активности иктального пика - «диффузной активности быстрых волн», зарегистрированной во время припадка, - и интерктальной активности.эпилептиформная активность (IEA), короткие всплески нейрональной активности, зарегистрированные между эпилептическими событиями. ЭКоГ также выполняется после операции резекции, чтобы обнаружить оставшуюся эпилептиформную активность и определить успех операции. Остаточные выбросы на ЭКоГ, не измененные резекцией, указывают на плохой контроль над приступом и неполную нейтрализацию эпилептогенной корковой зоны. Для полного устранения судорожной активности может потребоваться дополнительная операция. Экстраоперационная ЭКоГ также используется для локализации функционально важных областей (также известных как красноречивый кортекс), которые необходимо сохранить во время операции по эпилепсии. [16] Сообщается, что двигательные, сенсорные и когнитивные задачи во время экстраоперационной ЭКоГ увеличивают амплитуду высокочастотной активности с частотой 70–110 Гц в областях, вовлеченных в выполнение данных задач.[16] [17] [18] Высокочастотная активность, связанная с задачей, может анимировать «когда» и «где» кора головного мозга активируется и подавляется в четырехмерном режиме с временным разрешением 10 миллисекунд или ниже и пространственным разрешением 10 мм или меньше. [17] [18]
- Интраоперационная ЭКоГ
Целью резекционной операции является удаление эпилептогенной ткани без недопустимых неврологических последствий. Помимо выявления и локализации размеров эпилептогенных зон, ЭКоГ, используемая в сочетании с DCES, также является ценным инструментом для функционального кортикального картирования . Жизненно важно точно локализовать критические структуры головного мозга, определив, какие области хирург должен сохранить во время резекции (« красноречивая кора головного мозга»)."), чтобы сохранить сенсорную обработку, координацию движений и речь. Функциональное картирование требует, чтобы пациент мог взаимодействовать с хирургом, и, таким образом, выполняется под местной, а не общей анестезией. Используется электрическая стимуляция с использованием корковых и острых глубинных электродов. для исследования отдельных областей коры головного мозга с целью выявления центров речи, соматосенсорной интеграции и соматомоторной обработки. Во время операции резекции также может проводиться интраоперационная ЭКоГ, чтобы контролировать эпилептическую активность ткани и гарантировать резекцию всей эпилептогенной зоны .
Хотя использование экстраоперационной и интраоперационной ЭКоГ при резекционной хирургии было общепринятой клинической практикой в течение нескольких десятилетий, недавние исследования показали, что полезность этого метода может варьироваться в зависимости от типа эпилепсии у пациента. Курувилла и Флинк сообщили, что, хотя интраоперационная ЭКоГ играет решающую роль в индивидуальной височной лобэктомии, при множественных субпиальных разрезах (MST) и в устранении пороков развития коры головного мозга (MCD), она оказалась непрактичной при стандартной резекции медиальной височной доли. эпилепсия (TLE) с МРТ-свидетельством мезиального височного склероза (MTS). [2] Исследование, проведенное Веннбергом, Кесни и Расмуссеном, продемонстрировало дооперационное значение ЭКоГ в случаях лобной эпилепсии (ФЛЭ).[19]
Приложения для исследований [ править ]
ЭКоГ недавно стала многообещающим методом записи для использования в интерфейсах мозг-компьютер (BCI). [20] BCI - это прямые нейронные интерфейсы, которые обеспечивают управление протезами, электронными устройствами или устройствами связи посредством прямого использования сигналов мозга человека. Сигналы в головном мозге могут регистрироваться либо инвазивно, с помощью записывающих устройств, имплантированных непосредственно в кору головного мозга, либо неинвазивно с использованием электродов ЭЭГ на черепе. ЭКоГ служит для обеспечения частично инвазивного компромисса между двумя модальностями - хотя ЭКоГ не проникает через гематоэнцефалический барьер, как инвазивные записывающие устройства, она имеет более высокое пространственное разрешение и более высокое отношение сигнал / шум, чем ЭЭГ. [20]ECoG недавно привлек внимание к декодированию воображаемой речи или музыки, что может привести к «буквальным» BCI [21], в которых пользователи просто представляют слова, предложения или музыку, которые BCI может напрямую интерпретировать. [22] [23]
Помимо клинических приложений для локализации функциональных областей для поддержки нейрохирургии, функциональное картирование мозга в режиме реального времени с помощью ЭКоГ привлекло внимание для поддержки исследований фундаментальных вопросов нейробиологии. Например, в исследовании 2017 года изучались регионы в областях обработки лица и цвета и было обнаружено, что эти субрегионы вносят весьма специфический вклад в различные аспекты зрения. [24] Другое исследование показало, что высокочастотная активность в диапазоне 70–200 Гц отражает процессы, связанные как с временным, так и с постоянным процессом принятия решений. [25] В другой работе, основанной на ЭКоГ, был представлен новый подход к интерпретации активности мозга, предполагающий, что мощность и фаза совместно влияют на мгновенный потенциал напряжения, который напрямую регулирует возбудимость коры. [26]Подобно работе по декодированию воображаемой речи и музыки, эти направления исследований, включающие функциональное картирование мозга в реальном времени, также имеют значение для клинической практики, включая как нейрохирургию, так и системы BCI. Система, которая использовалась в большинстве этих публикаций по функциональному картированию в реальном времени, «CortiQ» . используется как для исследований, так и для клинических приложений.
Последние достижения [ править ]
Электрокортикограмма до сих пор считается « золотым стандартом » для определения эпилептогенных зон; однако эта процедура рискованна и очень инвазивна. В недавних исследованиях изучалась разработка неинвазивной техники визуализации коры головного мозга для дооперационного планирования, которая может предоставить аналогичную информацию и разрешение инвазивной ЭКоГ.
В одном новом подходе Lei Ding et al. [27]стремятся объединить информацию, предоставленную структурной МРТ и ЭЭГ кожи головы, чтобы обеспечить неинвазивную альтернативу ЭКоГ. В этом исследовании изучается подход к локализации источника подпространства с высоким разрешением, FINE (первопринципные векторы), для получения изображения местоположения и оценки протяженности источников тока от ЭЭГ скальпа. К результирующей томографии значений подпространственной корреляции была применена методика пороговой обработки, чтобы идентифицировать эпилептогенные источники. Этот метод был протестирован на трех педиатрических пациентах с трудноизлечимой эпилепсией и дал обнадеживающие клинические результаты. Каждого пациента обследовали с помощью структурной МРТ, длительного видео-ЭЭГ-мониторинга с помощью электродов для кожи головы, а затем с помощью субдуральных электродов. Затем данные ЭКоГ регистрировались с имплантированных субдуральных электродных сеток, размещенных непосредственно на поверхности коры.Для каждого испытуемого были также получены изображения МРТ и компьютерной томографии.
Эпилептогенные зоны, идентифицированные по предоперационным данным ЭЭГ, были подтверждены наблюдениями по послеоперационным данным ЭКоГ у всех трех пациентов. Эти предварительные результаты предполагают, что можно направить хирургическое планирование и определить местонахождение эпилептогенных зон неинвазивно, используя описанные методы визуализации и интеграции. Результаты ЭЭГ были дополнительно подтверждены хирургическими исходами всех трех пациентов. После хирургической резекции у двух пациентов приступы исчезли, а у третьего значительно уменьшилось количество приступов. Благодаря своему клиническому успеху, FINE предлагает многообещающую альтернативу предоперационной ЭКоГ, предоставляя информацию как о локализации, так и о степени эпилептогенных источников с помощью неинвазивной процедуры визуализации.
См. Также [ править ]
- Интерфейс мозг – компьютер
- Электроэнцефалограмма
- Эпилепсия
- Магнитно-резонансная томография
- Герберт Джаспер
- Уайлдер Пенфилд
Ссылки [ править ]
- ^ Palmini, A (2006). «Концепция эпилептогенной зоны: современный взгляд на взгляды Пенфилда и Джаспера на роль межприступных спайков» . Эпилептические расстройства . 8 (Дополнение 2): S10–5. PMID 17012068 .
- ^ а б в г д Курувилла, А; Флинк, Р. (2003). «Интраоперационная электрокортикография в хирургии эпилепсии: полезно или нет?» . Захват . 12 (8): 577–84. DOI : 10.1016 / S1059-1311 (03) 00095-5 . PMID 14630497 . S2CID 15643130 .
- ^ Баумейстер AA (2000). «Программа электрической стимуляции мозга Тулейна - исторический пример медицинской этики». J Hist Neurosci . 9 (3): 262–78. DOI : 10,1076 / jhin.9.3.262.1787 . PMID 11232368 . S2CID 38336466 .
- ^ Марван Хариз; Патрик Бломстедт; Людвик Зринцо (2016). «Глубокая стимуляция мозга между 1947 и 1987 годами: невыразимая история» . Нейрохирург Фокус . 29 (2). e1 - через Medscape.CS1 maint: использует параметр авторов ( ссылка )
- ^ Hashiguchi, K; Мориока, Т; Yoshida, F; Мияги, Й; и другие. (2007). «Корреляция между электроэнцефалографической и электрокортикографической активностями, записанными на коже головы в иктальный период» . Захват . 16 (3): 238–247. DOI : 10.1016 / j.seizure.2006.12.010 . PMID 17236792 . S2CID 1728557 .
- ^ Асано, E; Юхас, К; Шах, А; Музик, О; и другие. (2005). «Происхождение и распространение эпилептических спазмов, выявленных при электрокортикографии» . Эпилепсия . 46 (7): 1086–1097. DOI : 10.1111 / j.1528-1167.2005.05205.x . PMC 1360692 . PMID 16026561 .
- ^ a b Логотетис, Н.К. (2003). «Основа функционального сигнала магнитно-резонансной томографии BOLD» . Журнал неврологии . 23 (10): 3963–71. DOI : 10.1523 / JNEUROSCI.23-10-03963.2003 . PMC 6741096 . PMID 12764080 .
- ^ Ульберт, я; Halgren, E; Heit, G; Кармос, Г. (2001). «Система записи нескольких микроэлектродов для интракортикальных приложений человека». Журнал методов неврологии . 106 (1): 69–79. DOI : 10.1016 / S0165-0270 (01) 00330-2 . PMID 11248342 . S2CID 12203755 .
- ^ a b c d Schuh, L; Друри, я (1996). «Интраоперационная электрокортикография и прямая корковая электростимуляция». Семинары по анестезии . 16 : 46–55. DOI : 10.1016 / s0277-0326 (97) 80007-4 .
- ^ Месгарани, N; Чанг, EF (2012). «Избирательное корковое представление присутствующего говорящего при восприятии речи несколькими говорящими» . Природа . 485 (7397): 233–6. Bibcode : 2012Natur.485..233M . DOI : 10.1038 / nature11020 . PMC 3870007 . PMID 22522927 .
- ^ Бойер А, Duffau Н, Винсент М, Ramdani S, Mandonnet Е, D Гиро, Bonnetblanc F (2018). «Электрофизиологическая активность, вызванная прямой электрической стимуляцией человеческого мозга: интерес компонента P0» (PDF) . Conf Proc IEEE Eng Med Biol Soc . 2018 : 2210–2213. DOI : 10,1109 / EMBC.2018.8512733 . ISBN 978-1-5386-3646-6. PMID 30440844 . S2CID 53097668 .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ "Электрическая стимуляция мозга: основные принципы и новые альтернативы" Авторы Энтони Л. Ритаччо, Питер Бруннер и Гервин Шалк. Издательский журнал клинической нейрофизиологии, том 35, номер 2. Дата март 2018 г. «частота» на странице 6 из 12, «повреждение» на странице 3 из 12
- ^ Kohrman, M (2007). «Что такое эпилепсия? Клинические перспективы в диагностике и лечении». Журнал клинической нейрофизиологии . 24 (2): 87–95. DOI : 10.1097 / WNP.0b013e3180415b51 . PMID 17414964 . S2CID 35146214 .
- ^ Сугано, H; Симидзу, H; Сунага, S (2007). «Эффективность интраоперационной электрокортикографии для оценки судорожных исходов у трудноизлечимых пациентов с эпилепсией с поражениями височной доли» . Захват . 16 (2): 120–127. DOI : 10.1016 / j.seizure.2006.10.010 . PMID 17158074 .
- ^ Миллер, KJ; denNijs, M; Шеной, П; Миллер, JW; и другие. (2007). «Функциональное картирование мозга в реальном времени с помощью электрокортикографии». NeuroImage . 37 (2): 504–507. DOI : 10.1016 / j.neuroimage.2007.05.029 . PMID 17604183 . S2CID 3362496 .
- ^ a b Крон, NE; Miglioretti, DL; Гордон, Б; Меньший, Р.П. (1998). «Функциональное картирование сенсомоторной коры головного мозга человека с электрокортикографическим спектральным анализом. II. Событийная синхронизация в гамма-диапазоне» . Мозг . 121 (12): 2301–15. DOI : 10,1093 / мозг / 121.12.2301 . PMID 9874481 .
- ^ a b Nakai, Y; Jeong, JW; Браун, ЕС; Rothermel, R; Кодзима, К; Камбара, Т; Шах, А; Mittal, S; Суд, S; Асано, Э (2017). «Трех- и четырехмерное картирование речи и языка у больных эпилепсией» . Мозг . 140 (5): 1351–1370. DOI : 10,1093 / мозг / awx051 . PMC 5405238 . PMID 28334963 .
- ^ a b Nakai, Ya; Нагашима, А; Хаякава, А; Осуки, Т; Jeong, JW; Сугиура, А; Браун, ЕС; Асано, Э (2018). «Четырехмерная карта ранней зрительной системы человека» . Clin Neurophysiol . 129 (1): 188–197. DOI : 10.1016 / j.clinph.2017.10.019 . PMC 5743586 . PMID 29190524 .
- ^ Веннберг, R; Quesney, F; Оливье, А; Расмуссен, Т. (1998). «Электрокортикография и исход при лобной эпилепсии». Электроэнцефалография и клиническая нейрофизиология . 106 (4): 357–68. DOI : 10.1016 / S0013-4694 (97) 00148-X . PMID 9741764 .
- ^ а б Шеной, П; Миллер, KJ; Ojemann, JG; Рао, РПН (2007). «Обобщенные характеристики электрокортикографических ИМК» (PDF) . IEEE Transactions по биомедицинской инженерии . 55 (1): 273–80. CiteSeerX 10.1.1.208.7298 . DOI : 10.1109 / TBME.2007.903528 . PMID 18232371 . S2CID 3034381 . Архивировано (PDF) из оригинала 14 декабря 2014 г. - через http://homes.cs.washington.edu/~rao/ .
- Перейти ↑ Allison, Brendan Z. (2009). «Глава 2: На пути к повсеместным BCI». Интерфейсы мозг-компьютер . Springer. С. 357–387. ISBN 978-3-642-02091-9.
- ^ Свифт, Джеймс; Кун, Уильям; Гугер, Кристоф; Бруннер, Питер; Букет, М; Линч, Т; Фроули, Т; Ритаччо, Энтони; Шалк, Гервин (2018). «Пассивное функциональное картирование рецептивных речевых зон с помощью электрокортикографических сигналов» . Клиническая нейрофизиология . 6 (12): 2517–2524. DOI : 10.1016 / j.clinph.2018.09.007 . PMC 6414063 . PMID 30342252 . CS1 maint: использует параметр авторов ( ссылка )
- ^ Мартин, Стефани; Итуррате, Иньяки; Миллан, Хосе дель Р .; Рыцарь, Роберт; Пэсли, Брайан Н. (2018). «Расшифровка внутренней речи с помощью электрокортикографии: прогресс и проблемы на пути к речевому протезу» . Границы неврологии . 12 : 422. DOI : 10,3389 / fnins.2018.00422 . PMC 6021529 . PMID 29977189 . CS1 maint: использует параметр авторов ( ссылка )
- ^ Шальк, Гервин; Капеллер, Кристоф; Гугер, Кристоф; Огава, H; Хиросима, Южный; Лафер-Соуза, Р. Сайгин, Зеньип М .; Камада, Кёсукэ; Канвишер, Нэнси (2017). «Facephenes и радуга: причинные доказательства функциональной и анатомической специфичности обработки лица и цвета в человеческом мозге» . Proc Natl Acad Sci USA . 114 (46): 12285–12290. DOI : 10.1073 / pnas.1713447114 . PMC 5699078 . PMID 29087337 . CS1 maint: использует параметр авторов ( ссылка )
- ^ Саез, я; Lin, J; Столк, А; Изменять; Парвизи, Дж; Шальк, Гервин; Knight, Роберт Т .; Сюй, М. (2018). «Кодирование множественных вычислений, связанных с вознаграждением в переходных и устойчивых высокочастотных процессах в человеческом OFC» . Текущая биология . 28 (18): 2889–2899.e3. DOI : 10.1016 / j.cub.2018.07.045 . PMC 6590063 . PMID 30220499 . CS1 maint: использует параметр авторов ( ссылка )
- ^ Шальк, Гервин; Marple, J .; Knight, Роберт Т .; Кун, Уильям Г. (2017). «Мгновенное напряжение как альтернатива силовой и фазовой интерпретации колебательной активности мозга» . NeuroImage . 157 : 545–554. DOI : 10.1016 / j.neuroimage.2017.06.014 . PMC 5600843 . PMID 28624646 . CS1 maint: использует параметр авторов ( ссылка )
- ^ Дин, L; Wilke, C; Сюй, В; Сюй, Х; и другие. (2007). «Визуализация источника ЭЭГ: сопоставление местоположений и размеров источников с электрокортикографией и хирургическими резекциями у пациентов с эпилепсией» . Журнал клинической нейрофизиологии . 24 (2): 130–136. DOI : 10.1097 / WNP.0b013e318038fd52 . PMC 2758789 . PMID 17414968 .