 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Эмцит, Эстрацит |
| Другие имена | ЭМИ; Leo 299; NSC-89199; Ro 21-8837 / 001; Эстрадиол, нормустин фосфат; Эстрадиол 3-нормустин 17β-фосфат; Эстрадиол 3- (бис (2-хлорэтил) карбамат) 17β- (дигидрофосфат) |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a608046 |
| Данные лицензии |
|
Категория беременности |
|
| Пути администрирования | Устно |
| Класс препарата | Химиотерапевтическое средство ; Эстроген ; Эстрогеновый эфир |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Биодоступность | 44–75% (как эстрамустин и эстромустин) [1] |
| Связывание с белками | • Эстрадиол: 98% [2] • Эстрон: 96% [2] |
| Метаболизм | Печень , кишечник [3] [1] [6] |
| Метаболиты | • Эстрамустин [3] [1] • Эстромустин [3] [1] • Эстрадиол [3] [1] • Эстрон [3] [1] • Фосфорная кислота [3] [1] • Нормустин [4] |
| Ликвидация Период полураспада | • ЭМИ: 1,27 часа [5] • Эстромустин: 10–14 часов [1] • Эстрон: 15–17 часов [1] |
| Экскреция | Желчь , кал (2,9–4,8%) [1] [6] |
| Идентификаторы | |
Название ИЮПАК
| |
| Количество CAS |
|
| PubChem CID |
|
| IUPHAR / BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| КЕГГ |
|
| ЧЭБИ |
|
| ЧЭМБЛ |
|
| CompTox Dashboard ( EPA ) |
|
| ECHA InfoCard | 100.023.193 |
| Химические и физические данные | |
| Формула | C 23 H 32 Cl 2 N O 6 P |
| Молярная масса | 520,38 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
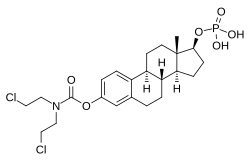
Эстрамустин фосфат ( EMP ), также известный как эстрадиол-нормустин-фосфат и продаваемый под торговыми марками Emcyt и Estracyt , представляет собой двойной эстроген и химиотерапевтический препарат, который используется при лечении рака простаты у мужчин. [7] [4] [8] [9] [10] [3] [1] [11] [5] [12] » Его принимают несколько раз в день перорально или путем инъекции в вену . [7] [8] [3] [1] [5] [12]
Побочные эффекты EMP включают тошноту , рвоту , гинекомастию , феминизацию , демаскулинизацию , сексуальную дисфункцию , тромбы и сердечно-сосудистые осложнения. [3] [9] [13] EMP является двойным цитостатическим и, следовательно, химиотерапевтическим средством и гормональным противораковым средством типа эстрогена . [1] [3] [14] [5] Это является пролекарством из эстрамустина иэстромустин с точки зрения его цитостатических эффектов и пролекарство эстрадиола в отношении его эстрогенных эффектов. [1] [3] EMP оказывает сильное эстрогенное действие при типичных клинических дозировках и, следовательно, имеет выраженный антигонадотропный и функциональный антиандрогенный эффект. [4] [1] [3] [14]
ЭМИ был введен для медицинского использования в начале 1970-х годов. [3] Он доступен в США , Канаде , Великобритании , других европейских странах и в других странах мира. [15] [16]
Медицинское использование [ править ]
ЭЙ указываются, в Соединенных Штатах , для паллиативного лечения от метастатического и / или прогрессивного рака простаты, [6] , тогда как в Соединенном Королевстве указываются для лечения или зависаний рецидивирующий рака простаты. [17] [5] [1] [10] Лекарство обычно предназначено для использования в случаях гормонорезистентного рака простаты, хотя оно также используется в качестве монотерапии первой линии. [3] Считается, что эффективность ЭМП при раке простаты эквивалентна традиционной терапии высокими дозами эстрогенов . [18]
Из-за относительно серьезных побочных эффектов и токсичности EMP редко использовался при лечении рака простаты. [4] Это особенно актуально сегодня в западных странах . [4] В результате, а также из-за редких побочных эффектов модуляторов гонадотропин-рилизинг-гормона (модуляторов гонадолиберина), таких как лейпрорелин , от ЭМП практически отказались. [3] Однако обнадеживающие результаты клинических исследований привели к возобновлению интереса к EMP для лечения рака простаты. [3]
EMP использовался в дозах от 140 до 1400 мг / день перорально. [19] Было обнаружено, что низкие дозы, такие как 280 мг / день, имеют сравнимую эффективность с более высокими дозами, но с улучшенной переносимостью и пониженной токсичностью. [4] Доза 140 мг / день была описана как очень низкая дозировка. [20] ЭМП использовался в дозах от 240 до 450 мг / день внутривенно. [1]
EMP и другие эстрогены, такие как фосфат полиэстрадиола и этинилэстрадиол , намного дешевле, чем новые методы лечения, такие как модуляторы GnRH, ацетат абиратерона и энзалутамид . [4] [21] [22] Кроме того, эстрогены могут иметь значительные преимущества по сравнению с другими средствами терапии по депривации андрогенов , например, в отношении потери костной массы и переломов , приливов , когнитивных способностей и метаболического статуса . [4] [22]
EMP использовался для предотвращения обострения тестостерона в начале терапии агонистом GnRH у мужчин с раком простаты. [23]
| Маршрут / форма | Эстроген | Дозировка | |
|---|---|---|---|
| Устный | Эстрадиол | 1-2 мг 3 раза в день | |
| Конъюгированные эстрогены | 1,25–2,5 мг 3 раза в день | ||
| Этинилэстрадиол | 0,15–3 мг / день | ||
| Сульфонат этинилэстрадиола | 1-2 мг 1 раз в неделю | ||
| Диэтилстильбестрол | 1–3 мг / день | ||
| Диенестрол | 5 мг / день | ||
| Гексэстрол | 5 мг / день | ||
| Фосфестрол | 100–480 мг 1–3 раза в день | ||
| Хлортрианизен | 12–48 мг / день | ||
| Квадросилан | 900 мг / день | ||
| Эстрамустин фосфат | 140–1400 мг / день | ||
| Трансдермальный пластырь | Эстрадиол | 2–6x 100 мкг / день Мошонка: 1x 100 мкг / день | |
| IM или SC инъекция | Бензоат эстрадиола | 1,66 мг 3 раза в неделю | |
| Дипропионат эстрадиола | 5 мг 1 раз в неделю | ||
| Эстрадиола валерат | 10-40 мг 1 раз в 1-2 недели | ||
| Эстрадиола ундецилат | 100 мг 1 раз в 4 недели | ||
| Полиэстрадиолфосфат | Самостоятельно: 160–320 мг 1 раз в 4 недели При пероральном приеме ЭЭ : 40–80 мг 1 раз в 4 недели | ||
| Estrone | 2–4 мг 2–3 раза в неделю | ||
| Внутривенная инъекция | Фосфестрол | 300–1200 мг 1–7 раз в неделю | |
| Эстрамустин фосфат | 240–450 мг / день | ||
| Примечание. Дозировки не обязательно эквивалентны. Источники: см. Шаблон. | |||
Доступные формы [ править ]
EMP доступен или был доступен в форме как капсул (140 мг, 280 мг) для перорального введения, так и водных растворов (300 мг) для внутривенных инъекций . [19] [24] [25] [7]
Противопоказания [ править ]
EMP является противопоказанием при использовании у детей, больных сверхчувствительность к эстрогенам или азота горчица , те , с язвенной болезнью ( язвы в желудочно - кишечном тракте ), те , с сильно скомпрометированных функции печени , те со слабой сердечной мышцы (также известный как миокардиальной недостаточности ) , и те , при тромбоэмболических нарушениях или осложнениях, связанных с задержкой жидкости . [17]
Побочные эффекты [ править ]
В побочных эффектах от ОГО в целом были описаны как относительно жесткими. [3] Наиболее частыми побочными эффектами ЭМП являются побочные эффекты со стороны желудочно-кишечного тракта, такие как тошнота , рвота и диарея , при этом тошнота и рвота наблюдаются у 40% мужчин. [9] [1] Они обычно бывают легкой или средней степени тяжести, а тошноту и рвоту можно контролировать с помощью профилактических противорвотных препаратов. [9] Тем не менее, в тяжелых случаях побочных эффектов со стороны желудочно-кишечного тракта при приеме ЭМП может потребоваться снижение дозы или прекращение терапии. [1]Хотя тошнота и рвота, как сообщается, являются наиболее частыми побочными эффектами ЭМП, гинекомастия (развитие мужской груди), как было обнаружено, встречается у 83% мужчин, получавших ЭМИ, а частота эректильной дисфункции , возможно, аналогична таковой. или чуть меньше риска гинекомастии. [3] Как правило, считается , что феминизация , гиноидное распределение жира , демаскулинизация и импотенция происходят практически или почти у 100% мужчин, получающих терапию высокими дозами эстрогенов . [13] [26] Также сообщалось о снижении сексуальной активности у мужчин, получавших ЭМИ. [1]Эти побочные эффекты связаны с высоким уровнем эстрогена и низким уровнем тестостерона . [1] [3] Профилактическое облучение из груди может быть использовано , чтобы уменьшить частоту и тяжесть гинекомастия с эстрогенами. [13]
К серьезным побочным эффектам ЭМП относятся тромбоэмболические и сердечно-сосудистые осложнения, включая тромбоэмболию легочной артерии , тромбоз глубоких вен , инсульт , тромбофлебит , ишемическую болезнь сердца (ишемическая болезнь сердца; например, инфаркт миокарда ), тромбофлебит и застойная сердечная недостаточность с задержкой жидкости . [9] [1] ЭМИ вызывает сердечно-сосудистую токсичность, как и диэтилстильбестрол., но в меньшей степени по сравнению с низкими дозами (например, 280 мг / день перорального ЭМП против 1 мг / день перорального диэтилстильбестрола). [3] [27] Заболевание рака простаты также увеличивает риск тромбоэмболии, а комбинация с доцетакселом также может усилить риск тромбоэмболии. [9] Мета-анализ о клинических испытаниях было установлено , что общий риск тромбоэмболии с ЭМ составляет от 4 до 7%, по сравнению с 0,4% для химиотерапии схемы без ОГО. [9] Тромбоэмболия является основной связанной с токсичностью причиной прекращения приема ЭМП. [28] Антикоагулянтная терапия такими лекарствами, какаспирин , варфарин , нефракционированный и низкомолекулярный гепарин и антагонисты витамина К могут быть полезны для снижения риска тромбоэмболии с помощью EMP и других эстрогенов, таких как диэтилстильбэстрол и этинилэстрадиол . [9] [29] [4]
Неблагоприятные функциональные пробы печени обычно наблюдаются при приеме ЭМИ, но тяжелая дисфункция печени при приеме лекарства встречается редко. [1] Побочные эффекты со стороны центральной нервной системы редко наблюдаются при ЭМП, хотя сообщалось об увеличении желудочков и пигментации нейронов у обезьян, получавших очень высокие дозы ЭМП (20–140 мг / кг / день) в течение 3–6 месяцев. [1] EMP, по-видимому, не оказывает цитостатического действия на нормальную ткань мозга . [1] У женщин, получавших EMP в клинических исследованиях, наблюдалось несколько случаев незначительных гинекологических кровотечений . [1] ЭМП описывается как относительно хорошо переносимая цитостатическими противоопухолевыми препаратами и азотно-ипритными агентами, редко или совсем не связана со значительной гематологической токсичностью, такой как миелосупрессия (подавление костного мозга), желудочно-кишечная токсичность или другая более выраженная токсичность, связанная с такими агентами. [5] [1] [30] В отличие от большинства других цитостатических агентов, которые часто вызывают миелосупрессии, лейкопении (снижение белых кровяных телец подсчет) и нейтропении (снижение нейтрофилов подсчет), ЭМИ на самом деле производит лейкоцитоз (увеличение количества лейкоцитов) как побочный эффект.[31] [32]
В небольшом исследовании низких доз с использованием 280 мг / день перорального ЭМП в течение 150 дней переносимость была значительно улучшена, при этом раздражение желудочно-кишечного тракта наблюдалось только у 15% мужчин, и не было случаев тяжелой сердечно-сосудистой токсичности или тромбоза глубоких вен. [3] [4] Кроме того, никаких других побочных эффектов, кроме незначительного преходящего повышения уровня печеночных ферментов, не наблюдалось. [3] Эти данные свидетельствуют о том, что более низкие дозы перорального ЭМП могут быть более безопасным вариантом, чем более высокие дозы для лечения рака простаты. [4]
| Системный орган | Очень часто (≥10%) | Обычный (1–10%) | Частота неизвестна c |
|---|---|---|---|
| Нарушения со стороны крови и лимфатической системы | Анемия ; Лейкопения | Тромбоцитопения | |
| Со стороны иммунной системы | Гиперчувствительность | ||
| Нарушения обмена веществ и питания | Задержка жидкости | ||
| Психиатрические расстройства | Состояние спутанности сознания ; Депрессия | ||
| Расстройства нервной системы | Вялость ; Головная боль | ||
| Сердечные расстройства | Хроническая сердечная недостаточность | Инфаркт миокарда | Ишемия миокарда |
| Сосудистые расстройства | Эмболия | Гипертония | |
| Желудочно-кишечные расстройства | Тошнота b ; Рвота b ; Диарея b | ||
| Гепатобилиарные расстройства | Нарушение функции печени | ||
| Заболевания кожи и подкожной клетчатки | Ангионевротический отек c ; Аллергический дерматит | ||
| Опорно - двигательный аппарат и соединительная ткань | Мышечная слабость | ||
| Репродуктивная система и заболевания груди | Гинекомастия | Эректильная дисфункция | |
| Общие расстройства и состояния в месте введения | Тромбоз места инъекции ( раствор для внутривенного введения ) | ||
| Сноски: a = Невозможно оценить по имеющимся данным. b = Особенно в течение первых 2 недель терапии. с = Ангиодистрофия ( Квинке отек , гортани отек ) может произойти. Часто встречается в сочетании с ингибиторами АПФ . При возникновении ангионевротического отека следует немедленно прекратить прием ЭМИ. Источники: см. Шаблон. | |||
| Побочный эффект | Эстрамустин фосфат (перорально 11,5–15,9 мг / кг / день) (n = 93) (%) | Диэтилстильбестрол (перорально 3,0 мг / день) (n = 93) (%) |
|---|---|---|
| Сердечно-сосудистые и респираторные | ||
| Остановка сердца | 0 | 2 |
| Цереброваскулярное нарушение (инсульт) | 2 | 0 |
| Инфаркт миокарда (сердечный приступ) | 3 | 1 |
| Тромбофлебит | 3 | 7 |
| Легочная эмболия | 2 | 5 |
| Хроническая сердечная недостаточность | 3 | 2 |
| Отек ( припухлость ) | 19 | 17 |
| Одышка (одышка) | 11 | 3 |
| Судороги ног | 8 | 11 |
| Выделения из верхних дыхательных путей | 1 | 1 |
| Охриплость | 1 | 0 |
| Желудочно-кишечный тракт | ||
| Тошнота | 15 | 8 |
| Диарея | 12 | 11 |
| Незначительное расстройство желудочно-кишечного тракта | 11 | 6 |
| Анорексия (потеря аппетита) | 4 | 3 |
| Метеоризм | 2 | 0 |
| Рвота | 1 | 1 |
| Желудочно-кишечное кровотечение | 1 | 0 |
| Горло горло | 1 | 0 |
| Жажда | 1 | 0 |
| Покровный | ||
| Сыпь | 1 | 4 |
| Зуд (зуд) | 2 | 2 |
| Сухая кожа | 2 | 0 |
| Пигментные изменения | 0 | 3 |
| Легкие синяки | 3 | 0 |
| Промывка | 1 | 0 |
| Ночные поты | 0 | 1 |
| Шелушение кожи кончиков пальцев | 1 | 0 |
| Истончение волос | 1 | 1 |
| Изменения груди | ||
| Болезненность молочных желез | 66 | 64 |
| Увеличение груди ( гинекомастия или развитие мужской груди ) | ||
| Незначительный | 60 | 54 |
| Умеренный | 10 | 16 |
| Отмечен | 0 | 5 |
| Разное | ||
| Вялость в одиночку | 4 | 3 |
| Депрессия | 0 | 2 |
| Эмоциональная лабильность | 2 | 0 |
| Бессонница | 3 | 0 |
| Головная боль | 1 | 1 |
| Беспокойство | 1 | 0 |
| Грудная боль | 1 | 1 |
| Приливы | 0 | 1 |
| Глазная боль | 0 | 1 |
| Слезотечение (слезы из глаз) | 1 | 1 |
| Тиннитус | 0 | 1 |
| Лабораторные отклонения | ||
| Гематологический ( кровь ) | ||
| Лейкопения (низкий уровень лейкоцитов ) | 4 | 2 |
| Тромбопения (низкие тромбоциты ) | 1 | 2 |
| Печеночный (печень) | ||
| Только билирубин | 1 | 5 |
| Билирубин и ЛДГ | 0 | 1 |
| Билирубин и АСТ | 2 | 1 |
| Билирубин, ЛДГ и SGOT | 2 | 0 |
| LDH и / или SGOT | 31 год | 28 |
| Разное | ||
| Преходящая гиперкальциемия (высокое содержание кальция ) | 0 | 1 |
| Источники: [7] | ||
Передозировка [ править ]
Клинического опыта передозировки EMP нет. [7] Передозировка EMP может привести к выраженным проявлениям известных побочных эффектов лекарства. [7] Специфического антидота при передозировке ЭМП не существует. [17] В случае передозировки следует использовать промывание желудка для удаления содержимого желудка по мере необходимости, а лечение должно быть симптоматическим и поддерживающим. [7] [17] В случае опасно низкого уровня эритроцитов , лейкоцитов или тромбоцитов , при необходимости может быть сдана цельная кровь .[17] Следует контролировать функцию печени при передозировке ЭМИ. [17] После передозировки EMPследует продолжать контролировать гематологические и печеночные параметры в течение как минимум 6 недель. [7]
EMP использовался в высоких дозах, до 1260 мг / день перорально и от 240 до 450 мг / день внутривенно . [3] [1]
Взаимодействия [ править ]
ЭМИ было сообщено , чтобы увеличить эффективность и токсичность из трициклических антидепрессантов , как амитриптилин и имипрамин . [17] Когда продукты, содержащие кальций , алюминий и / или магний , такие как молочные продукты, такие как молоко , различные пищевые пищевые добавки и антациды , потребляются одновременно с EMP, нерастворимым хелатным комплексом / фосфатной солью между EMP и этими металлами.могут образовываться, и это может заметно ухудшить абсорбцию и, следовательно, пероральную биодоступность EMP. [3] [1] [17] У тех, кто одновременно принимает ингибиторы АПФ, может быть повышенный риск отека Квинке . [17]
Фармакология [ править ]
Фармакодинамика [ править ]
EMP, также известный как фосфат эстрадиола и нормустина, представляет собой комбинированный эфир эстрогена и азотистого эфира иприта . [1] [3] [14] Он состоит из эстрадиола , эстрогена , связанного с фосфатным эфиром, а также сложного эфира нормустина , азотистого иприта. [1] [3] [14] С точки зрения его фармакодинамических эффектов, ЭМИ является пролекарством из эстрамустина , estromustine и эстрадиола . [1] [3]В качестве пролекарства эстрадиола, ЭЙ является эстрогеном и , следовательно, агонист из рецепторов эстрогена . [1] [2] Сам по себе EMP имеет очень слабое сродство к рецепторам эстрогена. [1] Лекарство имеет молекулярную массу примерно на 91% выше, чем эстрадиол, из-за присутствия в нем C3 нормустина и сложных фосфатных эфиров C17β. [33] [15] Поскольку ЭМП является пролекарством эстрадиола, его можно рассматривать как естественную и биоидентичную форму эстрогена [14], хотя он обладает дополнительной цитостатической активностью через эстрамустин и эстрромустин. [1] [3]
EMP действует по двойному механизму действия : 1) прямая цитостатическая активность посредством ряда действий; и 2) как форма терапии высокими дозами эстрогена через антигонадотропные и функциональные антиандрогенные эффекты, опосредованные рецепторами эстрогена . [1] [3] [14] Антигонадотропные и функциональные антиандрогенные эффекты EMP состоят в сильном подавлении выработки гонадных андрогенов и, следовательно, уровней циркулирующих андрогенов, таких как тестостерон ; значительно повышенный уровень глобулина, связывающего половые гормоны, и, следовательно, снижение доли свободных андрогенов в кровотоке; и прямое антиандрогенное действие на клетки простаты. [30] [1] [3] [4] [34] [35] [36] Индекс свободных андрогенов при пероральном ЭМП оказался в среднем в 4,6 раза ниже, чем при орхиэктомии . [35] Таким образом, терапия ЭМП приводит к значительно более сильной депривации андрогенов, чем орхиэктомия. [36] Метаболиты ЭМИ, в том числе эстрамустином, estromustine, эстрадиола и эстрона , как было обнаружено, действуют как слабые антагонисты этого рецептора андрогена ( EC 50 = 0.5-3.1 мкМ), хотя клиническое значение этого неизвестно.[37] [34] [3] [1]
Во время терапии ЭМП наблюдаются чрезвычайно высокие уровни эстрадиола и эстрона. [3] [4] Эстрогенные метаболиты EMP ответственны за его наиболее частые побочные эффекты и его сердечно-сосудистую токсичность . [1] В некоторых публикациях ЭМИ описывается как имеющий относительно слабый эстрогенный эффект. [5] [30] Тем не менее, он показал, по существу, те же уровни и степень эстрогенных эффектов, таких как болезненность груди , гинекомастия , сердечно-сосудистая токсичность, изменения синтеза белка в печени и подавление тестостерона, как и высокие дозы диэтилстильбэстрола иэтинилэстрадиол в клинических исследованиях. [7] [4] [30] [36] [38] Представление о том, что ЭМИ обладает относительно слабой эстрогеновой активностью, могло быть основано на исследованиях на животных , которые показали, что ЭМИ оказывает у крыс в 100 раз меньшее утеротрофическое действие, чем эстрадиол, и может также не были приняты во внимание очень высокие дозы ЭМИ, используемые клинически у людей. [38] [39]
Механизм действия цитостатических эффектов EMP сложен и изучен лишь частично. [1] EMP, как полагают, в основном является митотическим ингибитором , ингибирующим механизмы, участвующие в фазе митоза клеточного цикла . [1] [4] В частности, он связывается с микротрубочками белков , ассоциированных и / или к тубулина и производит деполимеризации из микротрубочек (K d = 10-20 мкМ для эстрамустином), в результате чего арест клеточного деления в G 2 / M фаза (в частностиметафаза ). [1] [4] [40] Первоначально считалось, что EMP опосредует его цитостатические эффекты как пролекарство нормустина , азотистого иприта , и, следовательно, считалось, что он является алкилирующим противоопухолевым агентом . [3] [10] [5] [14] Тем не менее, последующие исследования показали, что EMP лишен алкилирующего действия и что влияние EMP на микротрубочки опосредуется интактным эстрамустином и эстромустином, при этом нормустин или эстрадиол имеют лишь незначительные или незначительные эффекты. [1] [3] [41] Таким образом , уникальные свойства Estramustine и estromustine структур, Содержащий карбамата - эфирная связь , по- видимому, отвечаем за цитостатические эффекты ОГО. [1] В дополнение к антимитотическому действию, EMP также вызывает другие цитостатические эффекты, включая индукцию апоптоза , вмешательство в синтез ДНК , взаимодействие ядерного матрикса , изменения клеточной мембраны , индукцию активных форм кислорода (свободных радикалов кислорода), и, возможно, дополнительные механизмы. [1] [4] Было обнаружено, что ЭМИ оказывает радиосенсибилизирующее действие при раке простаты и глиоме.клетки, улучшающие также чувствительность к лучевой терапии . [1]
В цитостатических метаболитах EMP накапливаются в тканях в селективном образом, например , в раке простаты клеток . [5] [1] [4] Это может быть связано с присутствием специфического эстрамустин-связывающего белка (EMBP) (K d = 10–35 нМ для эстрамустина), также известного как простатин или белок секрета простаты (PSP), который был обнаружен в клетках рака простаты, глиомы , меланомы и рака груди . [1] [4] [42]Считается, что из-за своей тканевой селективности EMP оказывает минимальное цитостатическое действие в здоровых тканях, и его тканевая селективность может быть ответственной за его терапевтическую цитостатическую эффективность против клеток рака простаты. [5] [4] [1]
Первоначально EMP был разработан как пролекарство с двумя сложными эфирами эстрогена и нормустина в качестве противоопухолевого средства, алкилирующего азотистый иприт, которое из-за сродства эстрогенового фрагмента к рецепторам эстрогена будет избирательно накапливаться в тканях-мишенях эстрогена и, следовательно, в опухоли, положительной по рецептору эстрогена клетки. [4] [14] [2] Следовательно, считалось, что EMP будет предпочтительно доставлять алкилирующую нормустиновую составляющую в эти ткани, что позволяет снизить цитостатические эффекты в здоровых тканях и, следовательно, улучшить эффективность и переносимость . [4] Однако последующие исследования показали, что расщепление очень ограниченное и медленное.сложного эфира нормустина, и этот ЭМП лишен алкилирующей активности. [4] [1] [3] [30] Кроме того, похоже, что эстрамустин и эстромустин могут преимущественно накапливаться в тканях-мишенях эстрогена не из-за сродства к рецепторам эстрогена, а из-за сродства к отдельным EMBP. [1] [3]
Чрезвычайно высокие, беременность -как уровни эстрадиола может быть ответственна за лейкоцитоз (увеличение лейкоцитов счетов), которое наблюдается у лиц , получавших ЭЙ. [31] [32] Этот побочный эффект отличается от большинства других цитотоксических агентов, которые вместо этого вызывают миелосупрессию ( подавление костного мозга ), лейкопению (снижение количества лейкоцитов) и нейтропению (снижение количества нейтрофилов ). [ необходима цитата ]
Антигонадотропные эффекты [ править ]
Было обнаружено, что ЭМП в дозе 280 мг / день подавляет уровни тестостерона у мужчин до кастратного диапазона (до 30 нг / дл) в течение 20 дней и до низкого уровня кастрации (до 10 нг / дл) в течение 30 дней. [3] Точно так же доза EMP в 70 мг / день подавляла уровни тестостерона до кастрированного диапазона в течение 4 недель. [3]
Фармакокинетика [ править ]
| Параметр | Внутривенно 300 мг | Перорально 420 мг |
|---|---|---|
| C макс | 506 ± 61 нг / мл | 362 ± 38 нг / мл |
| Т макс | 2,6 ± 0,4 часа | 2,2 ± 0,2 часа |
| т 1/2 | 10,3 ± 0,95 часов | 13,6 ± 3,09 часов |
| AUC 0–32 | 4,82 ± 0,62 | 2,88 ± 0,34 |
| Биодоступность | 100,0% | 43,7% ± 4,6% |
| Источники: [30] | ||
| Метаболит | Плазма | Соотношение |
|---|---|---|
| Эстрамустин | 20 000–23 000 пг / мл | 1: 9,6–9,8 |
| Эстромустин | 191 000–267 000 пг / мл | |
| Эстрадиол | 4900–9000 пг / мл | 1: 9,4–11,8 |
| Estrone | 71 000–85 000 пг / мл | |
| Источники: [30] | ||
После перорального приема внутрь , ЭЙ быстро и полностью дефосфорилировали с помощью фосфатаза в эстрамустин во время первого прохода в желудочно - кишечном тракте. [1] [4] [5] [43] Эстрамустин также частично , но существенно окисляется в estromustine от 17β-гидроксистероид дегидрогеназы во время первого прохода. [5] [1] [12] [44] Таким образом, EMP попадает в кровоток в виде эстрамустина и эстромустина и основного метаболита.ЭМП - это эстромустин. [1] [12] ограниченное количество приблизительно от 10 до 15% от эстрамустина и estromustine далее медленно метаболизируется с помощью гидролиза в normustine эфира в эстрадиол и эстрон соответственно. [1] [4] [30] Эта реакция , как полагают, катализируемой с помощью carbamidases , хотя гены , кодирующие ферменты , ответственные не были охарактеризованы. [1] [45] [46] Уровни циркулирующего нормустина, образованного из ЭМИ, незначительны.[41] [47] Выделение азота горчичного газа из normustineпомощью расщепления кислоты карбоновой группы не было продемонстрированои кажется, не происходит. [40] [30]
Пероральная биодоступность EMP низкая, что связано с глубоким метаболизмом первого прохождения; в частности, дефосфорилирование EMP. [1] Пероральная биодоступность ЭМП, в частности эстрамустина и эстромустина, составляет от 44 до 75%, что позволяет предположить, что всасывание может быть неполным. [1] В любом случае существует линейная зависимость между пероральной дозой EMP и циркулирующими уровнями эстрамустина и эстрромустина. [1] Потребление кальция , алюминия или магния с пероральным ЭМИ может заметно ухудшить его биодоступность из-за пониженного всасывания.из кишечника, и это может повлиять на его терапевтическую эффективность в низких дозах. [3] [17]
После однократного перорального приема 420 мг ЭМП у мужчин с раком предстательной железы максимальные уровни эстромустина составляли от 310 до 475 нг / мл (475 000 пг / мл) и возникали через 2–3 часа. [1] Было обнаружено, что уровни эстрадиола при пероральном приеме ЭМП 280 мг / день увеличиваются до очень высоких концентраций в течение одной недели терапии. [3] В одном исследовании уровни эстрадиола превышали 20 000 пг / мл через 10 дней, составляли около 30 000 пг / мл через 30 дней и достигали пика примерно 40 000 пг / мл через 50 дней. [3] Другое исследование выявило более низкие уровни эстрадиола от 4900 до 9000 пг / мл во время хронической терапии пероральным приемом ЭМП 560 мг / день. [30] Дополнительное исследование показало, что уровни эстрадиола составляют около 17000 пг / мл при пероральном приеме ЭМИ 140 мг / день и 38000 пг / мл при пероральном приеме 280 мг / мл.[ необходима цитата ] Сообщалось, что циркулирующие уровни эстрадиола и эстрона во время терапии ЭМП превышают нормальные уровни у мужчин более чем в 100 и 1000 раз соответственно. [4] [30] Уровни эстрамустина и эстрадиола в кровотоке заметно ниже, чем у эстромустина и эстрона, соответственно, с соотношением примерно 1:10 в обоих случаях. [1] [30] Тем не менее, уровни эстрадиола во время терапии ЭМП, похоже, аналогичны уровням, которые наблюдаются в середине и на поздних сроках беременности , и колеблются от 5000 до 40 000 пг / мл. [48] При пероральном введении в кровотоке не наблюдается неизменного ЭМИ. [1]
В фармакокинетиках ЭХ разные с внутривенной инъекцией . [1] После однократной внутривенной инъекции 300 мг EMP уровни EMP были выше, чем уровни его метаболитов в течение первых 8 часов. [1] Вероятно, это связано с обходом метаболизма первого прохождения. [1] Однако через 24 часа после введения дозы неизмененный ЭМИ больше не обнаруживался в кровотоке. [1] клиренс ЭМП из плазмы крови составляет 4,85 ± 0,684 л / ч. [1] В объемах распределенияЭМИ при внутривенном введении были небольшими; в модели с двумя отсеками объем распределения для центрального отсека составлял 0,043 л / кг, а для периферийного отсека составлял 0,11 л / кг. [1] связывание белков плазмы ЭМП высока. [1] Эстрамустин накапливается в опухолевой ткани, например в ткани рака простаты и глиомы , при этом уровни эстрамустина в этих тканях намного выше, чем в плазме (например, в 6,3 и 15,9 раза соответственно). [1] И наоборот, уровни эстромустина в опухоли по сравнению с плазмой аналогичны (1,0 и 0,5 раза соответственно). [1] Эстрамустин и эстромустин накапливаются вжировая ткань . [1]
Полувыведения из estromustine с оральной EMP составили 13,6 часов в среднем, с диапазоном от 8,8 до 22,7 часов. [1] Напротив, период полувыведения эстромустина при внутривенной инъекции составлял 10,3 часа с диапазоном от 7,36 до 12,3 часа. [1] Для сравнения, соответствующие периоды полувыведения эстрона составляли 16,5 и 14,7 часа при пероральном и внутривенном введении соответственно. [1] Эстрамустин и эстромустин в основном выводятся с желчью и, следовательно, с калом . [1] [30] Считается, что они не выводятся с мочой . [1]
Химия [ править ]
ЭМИ, также известный как эстрадиол 3-normustine 17b-фосфата или как эстрадиол 3- (бис (2-хлорэтил) карбамата) 17β- (дигидрофосфат), является синтетическим эстрана стероид и производное от эстрадиола . [33] [15] Это сложный эфир эстрогена ; В частности, ЭЙ является диэфиром эстрадиола с С3 normustine ( азотистый иприт - карбамат фрагмента ) эфиром и C17β фосфатного эфиром. [33] [15] ЭЙ обеспечиваются как натрий или меглумин соль . [33][15] [24] EMP похож на соединение с другими сложными эфирами эстрадиола, такими как эстрадиолсульфат и эстрадиолвалерат , но отличается присутствием азотистых составляющих сложного эфира иприта. [33] [15] Противоопухолевые препараты, относящиеся к ЭМП, хотя ни один из них не поступал в продажу, включают алестрамустин , атримустин , цитестрол ацетат , эстрадиоловый иприт , ICI-85966 и фенестрол . [33] [15]
Из-за своей гидрофильной части сложного фосфатного эфира EMP является легко растворимым в воде соединением. [49] [50] [51] В этом отличие от большинства других эфиров эстрадиола, которые представляют собой сложные эфиры жирных кислот и липофильные соединения, которые не особенно растворимы в воде . [2] В отличие от EMP, эстрамустин обладает высокой липофильностью, практически не растворим в воде и неионизируется . [19] Фосфатный эфир EMP был включен в молекулу, чтобы увеличить ее растворимость в воде и сделать возможным внутривенное введение . [7]
| Эстроген | Структура | Сложный эфир (ы) | Относительная мол. масса | Относительное содержание E2 b | logP c | ||||
|---|---|---|---|---|---|---|---|---|---|
| Должность (я) | Moiet (ы) | Тип | Длина а | ||||||
| Эстрадиол | - | - | - | - | 1,00 | 1,00 | 4.0 | ||
| Эстрадиола ацетат | C3 | Этановая кислота | Жирная кислота с прямой цепью | 2 | 1,15 | 0,87 | 4.2 | ||
| Бензоат эстрадиола | C3 | Бензолкарбоновая кислота | Ароматическая жирная кислота | - (~ 4–5) | 1,38 | 0,72 | 4,7 | ||
| Дипропионат эстрадиола | C3, C17β | Пропановая кислота (× 2) | Жирная кислота с прямой цепью | 3 (× 2) | 1,41 | 0,71 | 4.9 | ||
| Эстрадиола валерат | C17β | Пентановая кислота | Жирная кислота с прямой цепью | 5 | 1,31 | 0,76 | 5,6–6,3 | ||
| Бутират бензоата эстрадиола | C3, C17β | Бензойная кислота , масляная кислота | Смешанная жирная кислота | - (~ 6, 2) | 1,64 | 0,61 | 6.3 | ||
| Эстрадиола ципионат | C17β | Циклопентилпропановая кислота | Ароматическая жирная кислота | - (~ 6) | 1,46 | 0,69 | 6.9 | ||
| Эстрадиол энантат | C17β | Гептановая кислота | Жирная кислота с прямой цепью | 7 | 1,41 | 0,71 | 6,7–7,3 | ||
| Эстрадиола диенантат | C3, C17β | Гептановая кислота (× 2) | Жирная кислота с прямой цепью | 7 (× 2) | 1,82 | 0,55 | 8,1–10,4 | ||
| Эстрадиола ундецилат | C17β | Ундекановая кислота | Жирная кислота с прямой цепью | 11 | 1,62 | 0,62 | 9,2–9,8 | ||
| Стеарат эстрадиола | C17β | Октадекановая кислота | Жирная кислота с прямой цепью | 18 | 1,98 | 0,51 | 12,2–12,4 | ||
| Дистеарат эстрадиола | C3, C17β | Октадекановая кислота (× 2) | Жирная кислота с прямой цепью | 18 (× 2) | 2,96 | 0,34 | 20,2 | ||
| Эстрадиола сульфат | C3 | Серная кислота | Водорастворимый конъюгат | - | 1,29 | 0,77 | 0,3–3,8 | ||
| Эстрадиол глюкуронид | C17β | Глюкуроновая кислота | Водорастворимый конъюгат | - | 1,65 | 0,61 | 2,1–2,7 | ||
| Эстрамустин фосфат d | C3, C17β | Нормустин , фосфорная кислота | Водорастворимый конъюгат | - | 1,91 | 0,52 | 2,9–5,0 | ||
| Полиэстрадиолфосфат е | C3 – C17β | Фосфорная кислота | Водорастворимый конъюгат | - | 1,23 f | 0,81 f | 2,9 г | ||
| Сноски: а = длина сложного эфира в атомах углерода для жирных кислот с прямой цепью или приблизительная длина эфира в атомах углерода для ароматических жирных кислот . b = относительное содержание эстрадиола по массе (т. е. относительное воздействие эстрогенов ). c = Экспериментальный или прогнозируемый коэффициент распределения октанол / вода (т.е. липофильность / гидрофобность ). Получено из PubChem , ChemSpider и DrugBank . d = Также известен как эстрадиол нормустин фосфат. е = Полимер из эстрадиола фосфата (~ 13 повторяющихся структурных единиц ). f = относительная молекулярная масса или содержание эстрадиола на повторяющуюся единицу. g = logP повторяющейся единицы (например, фосфат эстрадиола). Источники: см. Отдельные статьи. | |||||||||
История [ править ]
EMP был впервые синтезирован в середине 1960-х годов и запатентован в 1967 году. [40] Первоначально он был разработан для лечения рака груди . [1] Идея EMP была вдохновлена поглощением и накоплением радиоактивно меченных эстрогенов в ткани рака груди. [1] Однако первоначальные клинические результаты ЭМП у женщин с раком груди были разочаровывающими. [1] Впоследствии было обнаружено, что радиоактивно меченый ЭМП поглощается и накапливается в предстательной железе крысы , и это открытие привело к тому, что лекарство было перепрофилировано для лечения рака простаты . [1] [3]ЭМИ был введен для использования в медицине при лечении этого состояния в начале 1970-х годов и был одобрен в Соединенных Штатах для этого показания в 1981 году. [1] [3] [52] Изначально ЭМИ был введен для использования путем внутривенных инъекций. [30] Впоследствии был введен пероральный препарат, а от внутривенного препарата почти отказались в пользу перорального варианта. [30]
Общество и культура [ править ]
Общие имена [ править ]
EMP предоставляется в виде натриевой соли для перорального введения , которая имеет общие названия эстрамустинфосфат натрия ( USAN ) и эстрамустинфосфат натрия ( BANM , JAN ), а также в виде соли меглумина для внутривенного введения , имеющей общее название эстрамустинфосфат меглумин . [24] [33] [15] [53] [16] INNM является эстрамустинфосфатом . [33] Название эстрамустина фосфат.представляет собой сокращение эстрадиола и нормустин фосфата . [33] [16] EMP также известен под кодовыми названиями Leo 299 , Ro 21-8837 и Ro 21-8837 / 001 . [33] [15] [16]
Торговые марки [ править ]
EMP чаще всего продается под торговыми марками Estracyt и Emcyt, но также продается под рядом других торговых марок, включая Amsupros, Biasetyl, Cellmustin, Estramustin HEXAL, Estramustina Filaxis, Estranovag, Multosin, Multosin Injekt, Proesta, Prostamustin, и Сулопрост. [15] [16] [24]
Доступность [ править ]
EMP продается в США , [54] Канаде и Мексике под торговой маркой Emcyt, тогда как лекарство продается под торговой маркой Estracyt в Великобритании и других странах Европы, а также в Аргентине , Чили и Гонконге. . [15] Он был прекращен в ряде стран, включая Австралию , Бразилию , Ирландию и Норвегию . [55]
Исследование [ править ]
EMP был изучен при лечении других видов рака, таких как глиома и рак груди . [1] Было обнаружено, что он незначительно улучшает качество жизни людей с глиомой в течение первых 3 месяцев терапии. [1]
Ссылки [ править ]
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw топор ay az ba bb bc bd be bf bg bh bi bj bk bl bm bm bn bo bp bq br bs bt bu bv bw bx Автор: bz ca cb cc cd ce cf cg Bergenheim AT, Henriksson R (февраль 1998 г.). «Фармакокинетика и фармакодинамика эстрамустинфосфата».Clin Pharmacokinet.34(2): 163–72.DOI:10.2165 / 00003088-199834020-00004.PMID 9515186.
- ^ а б в г е Kuhl H (2005). «Фармакология эстрогенов и прогестагенов: влияние различных путей введения» (PDF) . Климактерический . 8 Дополнение 1: 3–63. DOI : 10.1080 / 13697130500148875 . PMID 16112947 .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar Kitamura T (февраль 2001 г. ). «Необходимость переоценки эстрамустинфосфата натрия (EMP) как варианта лечения монотерапии первой линии при распространенном раке простаты».Int. J. Urol . 8 (2): 33–6. DOI : 10.1046 / j.1442-2042.2001.00254.x . PMID 11240822 .
- ^ Б с д е е г ч я J к л м п о р Q R сек т у V ш х у г Inoue, Такахиро (2018). «Роль эстрамустинфосфата и других эстрогенов в устойчивом к кастрации раке простаты». Гормональная терапия и устойчивость к кастрации рака простаты . С. 249–256. DOI : 10.1007 / 978-981-10-7013-6_26 . ISBN 978-981-10-7012-9.
- ^ a b c d e f g h i j k l m Perry CM, McTavish D (июль 1995 г.). «Эстрамустин фосфат натрия. Обзор его фармакодинамических и фармакокинетических свойств, а также терапевтическая эффективность при раке простаты». Наркотики старения . 7 (1): 49–74. DOI : 10.2165 / 00002512-199507010-00006 . PMID 7579781 .
- ^ a b c «Дозирование Emcyt (эстрамустина), показания, взаимодействия, побочные эффекты и многое другое» . Ссылка на Medscape . WebMD . Проверено 8 февраля 2014 года .
- ^ a b c d e f g h i j https://www.accessdata.fda.gov/drugsatfda_docs/label/2008/018045s023lbl.pdf
- ^ a b Цинь З, Ли Х, Чжан Дж, Тан Дж, Хан П, Сюй З, Ю И, Ян С, Ван С, Сюй Т, Сюй З, Цзоу Q (сентябрь 2016 г.). «Химиотерапия с эстрамустином или без него для лечения кастрационно-резистентного рака простаты: систематический обзор и метаанализ» . Медицина (Балтимор) . 95 (39): e4801. DOI : 10.1097 / MD.0000000000004801 . PMC 5265899 . PMID 27684806 .
- ^ a b c d e f g h Равери В., Физази К., Удар С., Друэ Л., Эймар Дж. К., Кулин С., Гравис Дж., Хеннекен С., Зербиб М. (декабрь 2011 г.). «Использование эстрамустинфосфата в современном лечении рака простаты на поздних стадиях» . BJU Int . 108 (11): 1782–6. DOI : 10.1111 / j.1464-410X.2011.10201.x . PMID 21756277 .
- ^ a b c Симпсон, D; Вагстафф, AJ (2003). «Эстрамустин фосфат натрия». Американский журнал рака . 2 (5): 373–390. DOI : 10.2165 / 00024669-200302050-00013 . S2CID 70507026 .
- ^ Hudes G (февраль 1997). «Химиотерапия на основе эстрамустина». Семин. Урол. Онкол . 15 (1): 13–9. PMID 9050135 .
- ^ а б в г Крейс В. (1995). «Возвращение к эстрамустину». Лечение рака. Res . Лечение рака и исследования. 78 : 163–84. DOI : 10.1007 / 978-1-4615-2007-8_8 . ISBN 978-1-4613-5829-9. PMID 8595142 .
- ^ a b c Гэлбрейт С.М., Дюшен Г.М. (апрель 1997 г.). «Андрогены и рак простаты: биология, патология и гормональная терапия». Евро. J. Рак . 33 (4): 545–54. DOI : 10.1016 / S0959-8049 (96) 00444-3 . PMID 9274433 .
- ^ a b c d e f g h Майкл Эттель; Эккехард Шиллингер (6 декабря 2012 г.). Эстрогены и антиэстрогены II: фармакология и клиническое применение эстрогенов и антиэстрогенов . Springer Science & Business Media. С. 540–. ISBN 978-3-642-60107-1.
- ^ a b c d e f g h i j k Номинальный индекс 2000: Международный справочник лекарственных средств . Тейлор и Фрэнсис. Январь 2000. С. 406–407. ISBN 978-3-88763-075-1.
- ^ а б в г д https://www.drugs.com/international/estramustine.html
- ^ a b c d e f g h i j "Капсулы с эстрацитом - Сводка характеристик продукта (SPC)" . Электронный сборник лекарств . Pfizer Limited. 12 августа 2013 . Проверено 8 февраля 2014 года .
- ^ Аурел Lupulescu (24 октября 1990). Гормоны и витамины в лечении рака . CRC Press. С. 40–. ISBN 978-0-8493-5973-6.
- ^ a b c Валентино Стелла; Рональд Борчардт; Майкл Хагеман; Реза Олияи, Ханс Мааг, Джефферсон Тилли (12 марта 2007 г.). Пролекарства: проблемы и награды . Springer Science & Business Media. С. 174–. ISBN 978-0-387-49782-2.CS1 maint: multiple names: authors list (link)
- ↑ Китамура Т., Сузуки М., Нисимацу Н., Куросаки Т., Эномото Ю., Фукухара Н., Куме Н., Такеучи Т., Мяо Л., Цзянган Н., Сяоцян Л. (январь 2010 г.). «Окончательный отчет о монотерапии низкими дозами эстрамустинфосфата (EMP) и терапии очень низкими дозами EMP в сочетании с агонистом LH-RH для ранее нелеченного распространенного рака простаты». Aktuelle Urologie . 41 Приложение 1: S34–40. DOI : 10,1055 / с-0029-1224657 . PMID 20094950 .
- ^ Сайед Y, Taxel P (2003). «Применение терапии эстрогенами у мужчин». Curr Opin Pharmacol . 3 (6): 650–4. DOI : 10.1016 / j.coph.2003.07.004 . PMID 14644018 .
- ^ a b Hedlund PO, Henriksson P (2000). «Парентеральное введение эстрогена по сравнению с полным удалением андрогенов при лечении прогрессирующей карциномы простаты: влияние на общую выживаемость и сердечно-сосудистую смертность. Скандинавская группа рака простаты (SPCG) -5 Trial Study». Урология . 55 (3): 328–33. DOI : 10.1016 / s0090-4295 (99) 00580-4 . PMID 10699602 .
- ↑ Симидзу Т.С., Сибата Й, Дзинбо Х, Сато Дж, Яманака Х (1995). «Эстрамустин фосфат для предотвращения обострения при терапии депо аналогом лютеинизирующего гормона-рилизинг-гормона». Евро. Урол . 27 (3): 192–5. DOI : 10.1159 / 000475159 . PMID 7541359 .
- ^ a b c d Мюллер (19 июня 1998 г.). Европейский индекс лекарств: европейские регистрации лекарств, четвертое издание . CRC Press. с. 245, 454. ISBN 978-3-7692-2114-5.
- ^ Кеннет Л. Беккер (2001). Принципы и практика эндокринологии и обмена веществ . Липпинкотт Уильямс и Уилкинс. С. 2153–. ISBN 978-0-7817-1750-2.
- ^ Tammela T (ноябрь 2004). «Эндокринное лечение рака простаты». J. Steroid Biochem. Мол. Биол . 92 (4): 287–95. DOI : 10.1016 / j.jsbmb.2004.10.005 . PMID 15663992 .
- ^ Cox RL, Crawford ED (декабрь 1995). «Эстрогены в лечении рака простаты». J. Urol . 154 (6): 1991–8. DOI : 10.1016 / S0022-5347 (01) 66670-9 . PMID 7500443 .
- ^ Fizazi K, Le Maitre A, Hudes G, Berry WR, Келли WK, Eymard JC, Logothetis CJ, Pignon JP, Michiels S (2007). «Добавление эстрамустина к химиотерапии и выживаемость пациентов с рефрактерным к кастрации раком простаты: метаанализ индивидуальных данных пациента». Ланцет Онкол . 8 (11): 994–1000. DOI : 10.1016 / S1470-2045 (07) 70284-X . PMID 17942366 .
- ^ Petrioli R, G Roviello, Fiaschi А.И., Laera л, Bianco В, Ponchietti R, Barbanti , G, Е Франчини (октябрь 2015 г.). «Низкие дозы эстрамустинфосфата и сопутствующие низкие дозы ацетилсалициловой кислоты у пациентов с тяжелым предварительным лечением с прогрессирующим устойчивым к кастрации раком простаты». Clin Genitourin Cancer . 13 (5): 441–6. DOI : 10.1016 / j.clgc.2015.03.004 . PMID 25920994 .
- ^ a b c d e f g h i j k l m n o p Gunnarsson PO, Forshell GP (июнь 1984 г.). «Клиническая фармакокинетика эстрамустинфосфата». Урология . 23 (6 Suppl): 22–7. DOI : 10.1016 / S0090-4295 (84) 80093-X . PMID 6375076 .
- ^ a b Александр NC, Хэнкок AK, Масуд МБ, Пит Б.Г., Прайс Дж. Дж., Тернер Р. Л., Стоун Дж., Уорд А. Дж. (март 1979 г.). «Эстрацит в запущенной карциноме груди: исследование фазы II». Clin Radiol . 30 (2): 139–47. DOI : 10.1016 / S0009-9260 (79) 80133-6 . PMID 86404 .
- ^ a b Daponte D, Sylvester R, De Pauw M, Fryszman A, Smith RM, Smith PH (август 1983). «Изменение количества лейкоцитов при лечении запущенного рака простаты эстрамустинфосфатом и стильбоэстролом». Br J Urol . 55 (4): 408–12. DOI : 10.1111 / j.1464-410X.1983.tb03333.x . PMID 6349745 .
- ^ a b c d e f g h i j J. Elks (14 ноября 2014 г.). Словарь лекарств: химические данные: химические данные, структуры и библиографии . Springer. С. 502–503. ISBN 978-1-4757-2085-3.
- ^ a b Ван LG, Лю XM, Kreis W, Budman DR (май 1998 г.). «Антагонистический эффект андрогенов метаболитов эстрамустинфосфата (EMP) на рецепторы андрогенов дикого типа и мутировавшие». Biochem. Pharmacol . 55 (9): 1427–33. DOI : 10.1016 / S0006-2952 (97) 00657-6 . PMID 10076535 .
- ^ а б Ван Поппель Х., Вербрук П.В., Берт Л. (1990). «Влияние эстрамустинфосфата на свободные андрогены. Сравнительное исследование влияния орхиэктомии и эстрамустинфосфата на свободные андрогены у пациентов с раком простаты». Acta Urol Belg . 58 (4): 89–95. PMID 2093302 .
- ^ a b c Карр Дж. П., Вайсман З., Кирдани Р. Ю., Мерфи Г. П., Сандберг А. А. (август 1980 г.). «Влияние диэтилстильбэстрола и эстрамустинфосфата на сывороточный глобулин, связывающий половые гормоны, и уровни тестостерона у пациентов с раком простаты». J. Urol . 124 (2): 232–6. DOI : 10.1016 / S0022-5347 (17) 55383-5 . PMID 7190620 .
- ↑ Olson KB, Pienta KJ (май 2000 г.). «Последние достижения в химиотерапии запущенного рака простаты». Curr Urol Rep . 1 (1): 48–56. DOI : 10.1007 / s11934-000-0035-Z . PMID 12084341 .
- ^ a b Дэлин Л., Дамбер Дж. Э., фон Шульц Б., Бергман Б. (август 1986 г.). «Эстрогенные эффекты этинилэстрадиола / полиэстрадиолфосфата и эстрамустинфосфата у пациентов с карциномой простаты. Сравнительное исследование эстроген-чувствительных белков печени, гонадотропинов и пролактина». Br J Urol . 58 (4): 412–6. DOI : 10.1111 / j.1464-410X.1986.tb09095.x . PMID 3092893 .
- Перейти ↑ Fredholm, B., Jensen, G., Lindskog, M., & Muntzing, J. (1974, январь). Влияние эстрамустинфосфата (эстрацита) на рост DMBA-индуцированных опухолей молочной железы у крыс. В Acta Pharmacologica et Toxicologica (Vol. 35, pp. 28-28). 35 Norre Sogade, PO Box 2148, DK-1016 Копенгаген, Дания: Munksgaard Int Publ Ltd.
- ^ a b c Punzi JS, Duax WL, Strong P, Griffin JF, Flocco MM, Zacharias DE, Carrell HL, Tew KD, Glusker JP (март 1992). «Молекулярная конформация эстрамустина и двух аналогов» . Мол. Pharmacol . 41 (3): 569–76. PMID 1545778 .
- ↑ a b Hauser AR, Merryman R (май 1984). «Эстрамустин фосфат натрия». Препарат Интелл Клин Фарм . 18 (5): 368–74. DOI : 10.1177 / 106002808401800502 . PMID 6373212 . S2CID 25303747 .
- Перейти ↑ Tew KD, Stearns ME (1989). «Эстрамустин - азотистый иприт / стероид с антимикротрубочковой активностью». Pharmacol. Ther . 43 (3): 299–319. DOI : 10.1016 / 0163-7258 (89) 90012-0 . PMID 2682681 .
- ^ Франко Кавалли; Стэн Б. Кэй; Heine H Hansen; Джеймс О Армитидж; Мартина Пикар-Гебхарт (12 сентября 2009 г.). Учебник медицинской онкологии, четвертое издание . CRC Press. С. 442–. ISBN 978-0-203-09289-7.
- Перейти ↑ Gunnarsson O, Andersson SB, Johansson SA (1983). «Гидролиз эстрамустинфосфата; исследования in vitro». Eur J Drug Metab Pharmacokinet . 8 (4): 395–402. DOI : 10.1007 / BF03188772 . PMID 6673977 . S2CID 22105700 .
- ^ a b Озэки Т., Такеучи М., Судзуки М., Китамура Т., Такаянаги Р., Йокояма Н., Ямада Ю. (октябрь 2009 г.). «Однонуклеотидные полиморфизмы гена 17бета-гидроксистероид дегидрогеназы типа 7: механизм побочных реакций, связанных с эстрамустином?». Int. J. Urol . 16 (10): 836–41. DOI : 10.1111 / j.1442-2042.2009.02374.x . PMID 19735314 .
- ^ Б Suzuki M, S, Muto Хара K, T, Озэки Ямада Y, T, Кадоваки Томита K, S, Kameyama Китамурой T (февраль 2005 г.). «Однонуклеотидные полиморфизмы в генах 17-бета-гидроксистероид дегидрогеназы могут предсказывать риск побочных эффектов натрия эстрамустинфосфата у пациентов с раком простаты» . Int. J. Urol . 12 (2): 166–72. DOI : 10.1111 / j.1442-2042.2005.01004.x . PMID 15733111 .
- ^ Ворота, Лоран; Тью, Кеннет Д. (2011). «Алкилирующие агенты». Лечение рака у человека: химиотерапия, биологическая терапия, гипертермия и поддерживающие меры . С. 61–85. DOI : 10.1007 / 978-90-481-9704-0_4 . ISBN 978-90-481-9703-3.
- ^ http://www.ilexmedical.com/files/PDF/Estradiol_ARC.pdf
- ^ Торстейнн Loftsson (25 января 2014). Стабильность лекарств для ученых-фармацевтов . Академическая пресса. С. 77–. ISBN 978-0-12-411562-0.
- ↑ С. Бернал (21 августа 1997 г.). Лекарственная устойчивость в онкологии . CRC Press. С. 287–. ISBN 978-1-4200-0209-6.
- ^ Samuel J. Murff (20 февраля 2012). Справочник по безопасности и здоровью цитотоксических препаратов . Правительственные институты. С. 89–. ISBN 978-1-60590-705-5.
- ^ Уильям Д. Фигг; Синди Х. Чау; Эрик Дж. Смолл (14 сентября 2010 г.). Медикаментозное лечение рака простаты . Springer Science & Business Media. С. 402–. ISBN 978-1-60327-829-4.
- ^ И. К. Мортон; Джудит М. Холл (6 декабря 2012 г.). Краткий словарь фармакологических агентов: свойства и синонимы . Springer Science & Business Media. С. 114–. ISBN 978-94-011-4439-1.
- ^ «Наркотики @ FDA: одобренные FDA лекарственные препараты» . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США . Проверено 29 января 2017 года .
- ^ Sweetman, S, изд. (12 февраля 2013 г.). «Эстрамустин натрия фосфат». Мартиндейл: Полный справочник лекарств . Лондон, Великобритания: Pharmaceutical Press . Проверено 8 февраля 2014 года .
Дальнейшее чтение [ править ]
- Тью К.Д. (сентябрь 1983 г.). «Механизм действия эстрамустина». Семин. Онкол . 10 (3 Suppl 3): 21–6. PMID 6364362 .
- Hoisaeter PA, Bakke A (сентябрь 1983 г.). «Эстрамустин фосфат (эстрацит): экспериментальные и клинические исследования в Европе». Семин. Онкол . 10 (3 Дополнение 3): 27–33. PMID 6364363 .
- Сандберг А.А. (сентябрь 1983 г.). «Метаболические аспекты и действия, уникальные для Estracyt». Семин. Онкол . 10 (3 Suppl 3): 3–15. PMID 6364364 .
- Хаукаас С.А. (1984). «Иммунологические эффекты диэтилстильбэстрола и эстрамустинфосфата». Scand J Urol Nephrol Suppl . 83 : 1–32. PMID 6387896 .
- Хаузер А. Р., Мерриман Р. (май 1984 г.). «Эстрамустин фосфат натрия». Препарат Интелл Клин Фарм . 18 (5): 368–74. DOI : 10.1177 / 106002808401800502 . PMID 6373212 . S2CID 25303747 .
- Сандберг А.А. (июнь 1984 г.). «Метаболические параметры эстрацита, имеющие отношение к его эффектам при раке простаты». Урология . 23 (6 Suppl): 11–21. DOI : 10.1016 / S0090-4295 (84) 80092-8 . PMID 6375075 .
- Gunnarsson PO, Forshell GP (июнь 1984 г.). «Клиническая фармакокинетика эстрамустинфосфата». Урология . 23 (6 Suppl): 22–7. DOI : 10.1016 / S0090-4295 (84) 80093-X . PMID 6375076 .
- Форсгрен Б., Бьорк П. (июнь 1984 г.). «Специфическое связывание эстрамустина с белками простаты». Урология . 23 (6 Suppl): 34–8. DOI : 10.1016 / S0090-4295 (84) 80095-3 . PMID 6375077 .
- Калланд Т., Хаукаас С.А. (июнь 1984 г.). «Иммунологические эффекты эстрамустинфосфата». Урология . 23 (6 Suppl): 39–45. DOI : 10.1016 / S0090-4295 (84) 80096-5 . PMID 6375078 .
- Høisaeter PA (июнь 1984 г.). «Механизм действия Эмцита». Урология . 23 (6 Suppl): 46–8. DOI : 10.1016 / S0090-4295 (84) 80097-7 . PMID 6375079 .
- Müntzing J, Gunnarsson K (июнь 1984 г.). «Доклиническая фармакология и токсикология эстрамустинфосфата». Урология . 23 (6 Suppl): 6–10. DOI : 10.1016 / S0090-4295 (84) 80091-6 . PMID 6375082 .
- Slack NH, Murphy GP (июнь 1984 г.). «Клиническая токсичность и отдаленные результаты терапии Эмцитом рака простаты». Урология . 23 (6 Suppl): 73–7. DOI : 10.1016 / S0090-4295 (84) 80103-X . PMID 6375085 .
- Hedlund PO (1985). «Механизм действия эстрамустинфосфата при гормонозависимом и гормононезависимом раке простаты». Прог. Clin. Биол. Res . 185А : 197–202. PMID 3898129 .
- Hedlund PO (1987). «Эстрацит - механизм действия и клинический опыт». Прог. Clin. Биол. Res . 243B : 215–9. PMID 3309981 .
- Мерфи Г.П. (1987). «Текущий обзор клинического опыта с Estracyt». Прог. Clin. Биол. Res . 243B : 221–5. PMID 3309982 .
- Форсгрен Б. (1988). «Эстрамустин-связывающий белок в простате крысы и человека». Scand J Urol Nephrol Suppl . 107 : 56–8. PMID 3287598 .
- Тью К.Д., Стернс М.Э. (1989). «Внутриклеточные эффекты эстрамустина (Estracyt / Emcyt)». Прог. Clin. Биол. Res . 303 : 169–75. PMID 2674983 .
- Тью К.Д., Стернс М.Э. (1989). «Эстрамустин - азотистый иприт / стероид с антимикротрубочковой активностью». Pharmacol. Ther . 43 (3): 299–319. DOI : 10.1016 / 0163-7258 (89) 90012-0 . PMID 2682681 .
- Кёнивес I (1989). «Эстрамустин фосфат (эстрацит) в лечении рака предстательной железы». Int Urol Nephrol . 21 (4): 393–7. DOI : 10.1007 / BF02559635 . PMID 2693392 .
- Бенсон Р., Хартли-Асп Б. (1990). «Механизмы действия и клиническое применение эстрамустина». Рак Инвест . 8 (3–4): 375–80. DOI : 10.3109 / 07357909009012056 . PMID 2207764 .
- Ван Поппель Х, Берт Л. (1991). «Настоящая роль эстрамустинфосфата в распространенном раке простаты». Прог. Clin. Биол. Res . 370 : 323–41. PMID 1924466 .
- Янкнегт Р.А. (1992). «Эстрамустин фосфат и другие цитотоксические препараты в лечении прогрессирующего рака простаты с плохим прогнозом». Prostate Suppl . 4 : 105–10. DOI : 10.1002 / pros.2990210516 . PMID 1574449 . S2CID 40562112 .
- Tew KD, Glusker JP, Hartley-Asp B, Hudes G, Speicher LA (декабрь 1992 г.). «Доклинические и клинические перспективы использования эстрамустина в качестве антимитотического средства». Pharmacol. Ther . 56 (3): 323–39. DOI : 10.1016 / 0163-7258 (92) 90023-S . PMID 1301594 .
- Крейс В. (1995). «Возвращение к эстрамустину». Лечение рака. Res . Лечение рака и исследования. 78 : 163–84. DOI : 10.1007 / 978-1-4615-2007-8_8 . ISBN 978-1-4613-5829-9. PMID 8595142 .
- Перри С.М., Мактавиш Д. (июль 1995 г.). «Эстрамустин фосфат натрия. Обзор его фармакодинамических и фармакокинетических свойств, а также терапевтическая эффективность при раке простаты». Наркотики старения . 7 (1): 49–74. DOI : 10.2165 / 00002512-199507010-00006 . PMID 7579781 .
- Худес Г. (февраль 1997 г.). «Химиотерапия на основе эстрамустина». Семин. Урол. Онкол . 15 (1): 13–9. PMID 9050135 .
- Bergenheim AT, Henriksson R (февраль 1998 г.). «Фармакокинетика и фармакодинамика эстрамустинфосфата». Clin Pharmacokinet . 34 (2): 163–72. DOI : 10.2165 / 00003088-199834020-00004 . PMID 9515186 .
- Китамура Т. (февраль 2001 г.). «Необходимость переоценки эстрамустинфосфата натрия (EMP) в качестве варианта лечения для монотерапии первой линии при распространенном раке простаты». Int. J. Urol . 8 (2): 33–6. DOI : 10.1046 / j.1442-2042.2001.00254.x . PMID 11240822 .
- Симпсон, Д.; Вагстафф, AJ (2003). «Эстрамустин фосфат натрия». Американский журнал рака . 2 (5): 373–390. DOI : 10.2165 / 00024669-200302050-00013 . S2CID 70507026 .
- Равери В., Физази К., Удар С., Друэ Л., Эймар Дж. К., Кулин С., Гравис Дж., Хеннекен С., Зербиб М. (декабрь 2011 г.). «Использование эстрамустинфосфата в современном лечении рака простаты на поздних стадиях» . BJU Int . 108 (11): 1782–6. DOI : 10.1111 / j.1464-410X.2011.10201.x . PMID 21756277 .
- Цинь З, Ли Х, Чжан Дж, Тан Дж, Хан П, Сюй З, Ю И, Ян Ц, Ван С, Сюй Т, Сюй З, Цзоу Цзюй (сентябрь 2016 г.). «Химиотерапия с эстрамустином или без него для лечения кастрационно-резистентного рака простаты: систематический обзор и метаанализ» . Медицина (Балтимор) . 95 (39): e4801. DOI : 10.1097 / MD.0000000000004801 . PMC 5265899 . PMID 27684806 .
- Иноуэ, Такахиро (2018). «Роль эстрамустинфосфата и других эстрогенов в устойчивом к кастрации раке простаты». Гормональная терапия и устойчивость к кастрации рака простаты . С. 249–256. DOI : 10.1007 / 978-981-10-7013-6_26 . ISBN 978-981-10-7012-9.