 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Этан-1,2-диамин [2] | |||
| Другие названия Эдамин [1] , 1,2-диаминоэтан, 'en', когда лиганд | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| Сокращения | en | ||
| 605263 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.154 | ||
| Номер ЕС |
| ||
| 1098 | |||
| КЕГГ | |||
| MeSH | этилендиамин | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1604 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 2 H 8 N 2 | |||
| Молярная масса | 60,100 г · моль -1 | ||
| Появление | Бесцветная жидкость [3] | ||
| Запах | Аммиачный [3] | ||
| Плотность | 0,90 г / см 3 [3] | ||
| Температура плавления | 8 ° C (46 ° F, 281 K) [3] | ||
| Точка кипения | 116 ° С (241 ° F, 389 К) [3] | ||
Растворимость в воде | смешивающийся | ||
| журнал P | −2,057 | ||
| Давление газа | 1,3 кПа (при 20 ° C) | ||
Константа закона Генри ( k H ) | 5,8 моль Па −1 кг −1 | ||
Магнитная восприимчивость (χ) |
| ||
Показатель преломления ( n D ) | 1,4565 | ||
| Термохимия | |||
Теплоемкость ( C ) | 172,59 Дж -1 моль -1 | ||
Стандартная мольная энтропия ( S | 202,42 Дж -1 моль -1 | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | −63,55–−62,47 кДж моль −1 | ||
Std энтальпии сгорания (Δ с Н ⦵ 298 ) | −1,8678–−1,8668 МДж моль −1 | ||
| Опасности | |||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H226 , H302 , H312 , H314 , H317 , H334 | ||
Меры предосторожности GHS | P261 , P280 , P305 + 351 + 338 , P310 | ||
| NFPA 704 (огненный алмаз) |  3 3 0 | ||
| точка возгорания | 34 ° С (93 ° F, 307 К) [3] | ||
самовоспламенения температуру | 385 ° С (725 ° F, 658 К) [3] | ||
| Пределы взрываемости | 2,7–16% | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 500 мг / кг (перорально, крыса) 470 мг / кг (перорально, морская свинка) 1160 мг / кг (перорально, крыса) [5] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 10 частей на миллион (25 мг / м 3 ) [4] | ||
REL (рекомендуется) | TWA 10 частей на миллион (25 мг / м 3 ) [4] | ||
IDLH (Непосредственная опасность) | 1000 частей на миллион [4] | ||
| Родственные соединения | |||
Родственные алканамины | 1,2-диаминопропан , 1,3-диаминопропан | ||
Родственные соединения | Этиламин , Этилендинитрамин | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
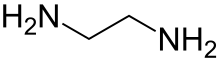
Этилендиамин (сокращенно en, когда лиганд ) представляет собой органическое соединение с формулой C 2 H 4 (NH 2 ) 2 . Это бесцветная жидкость с аммиаком -подобного запаха является сильно основным амином . Это широко используемый строительный блок в химическом синтезе, в 1998 году было произведено около 500 000 тонн [6].Этилендиамин легко вступает в реакцию с влагой влажного воздуха, образуя едкий, токсичный и раздражающий туман, даже кратковременное воздействие которого может нанести серьезный вред здоровью (см. Раздел «Безопасность»). Этилендиамин - первый член так называемых полиэтиленаминов .
Синтез [ править ]
Этилендиамин получают обработкой промышленно 1,2-дихлорэтана с аммиаком под давлением при 180 ° С в водной среде: [6] [7]
В этой реакции образуется хлористый водород , который образует соль с амином. Амин высвобождается при добавлении гидроксида натрия и затем может быть восстановлен ректификацией . Диэтилентриамин (ДЭТА) и триэтилентетрамин (ТЭТА) образуются как побочные продукты.
Другой промышленный путь получения этилендиамина включает реакцию этаноламина и аммиака: [8]
Этот процесс включает прохождение газообразных реагентов над слоем никелевых гетерогенных катализаторов .
Этилендиамин можно очистить обработкой гидроксидом натрия для удаления воды с последующей дистилляцией. [9]
Приложения [ править ]
Этилендиамин в больших количествах используется для производства многих промышленных химикатов. Он образует производные с карбоновыми кислотами (включая жирные кислоты ), нитрилами , спиртами (при повышенных температурах), алкилирующими агентами, сероуглеродом , альдегидами и кетонами . Благодаря своей бифункциональной природе, содержащей два амина, он легко образует гетероциклы, такие как имидазолидины .
Предшественник хелатирующих агентов, лекарств и агрохимикатов [ править ]
Наиболее известным производным этилендиамина является хелатирующий агент ЭДТА , который получают из этилендиамина посредством синтеза Стрекера с участием цианида и формальдегида . Гидроксиэтилэтилендиамин - еще один коммерчески значимый хелатирующий агент. [6] Многие биоактивные соединения и лекарства содержат связь N-CH 2 -CH 2 -N, в том числе некоторые антигистаминные препараты . [10] Соли этиленбисдитиокарбамата являются коммерчески значимыми фунгицидами под торговыми марками Maneb , Mancozeb , Zineb и Metiram. Немного имидазолина-содержащие фунгициды являются производными этилендиамина. [6]
Фармацевтический ингредиент [ править ]
Этилендиамин является ингредиентом обычного бронхолитического препарата аминофиллина , где он служит для растворения активного ингредиента теофиллина . Этилендиамин также использовался в дерматологических препаратах, но был удален из некоторых из-за того, что он вызывает контактный дерматит. [11] При использовании в качестве фармацевтического наполнителя после перорального приема его биодоступность составляет около 0,34 из-за значительного эффекта первого прохождения . Менее 20% устраняется путем почечной экскреции. [12]
Антигистаминные препараты на основе этилендиамина являются старейшими из пяти классов антигистаминных препаратов первого поколения , начиная с пипероксана или бенодаина, открытого в 1933 году в Институте Пастера во Франции, а также включающих мепирамин , трипеленнамин и антазолин . Другие классы являются производными этаноламина, алкиламином , пиперазин и другие ( в основном трициклические и тетрациклические соединения , связанные с фенотиазины , трициклические антидепрессанты , а также ципрогептадин - фениндамин семьи)
Роль в полимерах [ править ]
Этилендиамин, поскольку он содержит две аминогруппы, является широко используемым предшественником различных полимеров. Конденсаты, полученные из формальдегида, являются пластификаторами. Он широко используется при производстве полиуретановых волокон. Дендримеры класса PAMAM являются производными этилендиамина. [6]
Тетраацетилэтилендиамин [ править ]
Отбеливания активатор тетраацетилэтилендиамин генерируется из этилендиамина. Производное N , N- этиленбис (стеарамид) (EBS) представляет собой коммерчески значимое антиадгезионное средство и поверхностно-активное вещество в бензине и моторном масле.
Другие приложения [ править ]
- в качестве растворителя он смешивается с полярными растворителями и используется для солюбилизации белков, таких как альбумины и казеин . Он также используется в некоторых гальванических ваннах.
- как ингибитор коррозии в красках и охлаждающих жидкостях .
- дигидроиодид этилендиамина (EDDI) добавляют в корма для животных в качестве источника йодида.
- химикаты для проявки цветной фотографии , связующие , клеи , смягчители тканей , отвердители для эпоксидных смол и красители .
- как соединение, превращающее нитрометан во взрывчатое вещество. Эта смесь использовалась в Арсенале Пикатинни во время Второй мировой войны, что дало смеси нитрометана и этилендиамина прозвище PLX , или жидкое взрывчатое вещество Пикатинни.
Координационная химия [ править ]
Этилендиамин является хорошо известным бидентатным хелатирующим лигандом для координационных соединений , в котором два атома азота отдают свои неподеленные пары электронов, когда этилендиамин действует как лиганд. В неорганической химии его часто называют аббревиатурой «en». Комплекс [Со (этилендиамин) 3 ] 3+ представляет собой архетипический хиральный трис-хелатный комплекс. В саленовые лиганды , некоторые из которых используются в катализе, являются производными от конденсации салицилальдегидов и этилендиамина.
Связанные лиганды [ править ]
Родственные производные этилендиамина включают этилендиаминтетрауксусную кислоту (EDTA) , тетраметилэтилендиамин (TMEDA) и тетраэтилэтилендиамин (TEEDA). Хиральные аналоги этилендиамина включают 1,2-диаминопропан и транс- диаминоциклогексан .
Безопасность [ править ]
Этилендиамин, как и аммиак и другие низкомолекулярные амины, вызывает раздражение кожи и дыхательных путей. Жидкий этилендиамин, если его не хранить плотно, выделяет токсичные и раздражающие пары в окружающую среду, особенно при нагревании. Пары реагируют с влагой во влажном воздухе, образуя характерный белый туман, который чрезвычайно раздражает кожу, глаза, легкие и слизистые оболочки.
Ссылки [ править ]
- ^ "32007R0129" . Евросоюз. 12 февраля 2007 г. Приложение II . Проверено 3 мая 2012 года .
- ^ Международный союз чистой и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные наименования 2013 . Королевское химическое общество . п. 676. DOI : 10.1039 / 9781849733069 . ISBN 978-0-85404-182-4.
- ^ a b c d e f g Запись в базе данных веществ GESTIS Института охраны труда
- ^ a b c Карманный справочник NIOSH по химической опасности. «# 0269» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Этилендиамин» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b c d e Карстен Эллер, Эрхард Хенкес, Роланд Россбахер, Хартмут Хёке «Амины, алифатические» в Энциклопедии промышленной химии Ульмана, 2005 Wiley-VCH Verlag, Weinheim. DOI : 10.1002 / 14356007.a02_001
- ↑ Hans-Jürgen Arpe, Industrielle Organische Chemie, 6. Auflage (2007), Seite 245, Wiley VCH
- ↑ Hans-Jürgen Arpe, Industrielle Organische Chemie, 6. Auflage (2007), Seite 275, Wiley VCH
- ^ Роллинсон, Карл L .; Байлар-младший, Джон К. (1946). «Соли трис (этилендиамин) хрома (III)». Неорганические синтезы . Неорганические синтезы. 2 . С. 196–200. DOI : 10.1002 / 9780470132333.ch60 . ISBN 9780470132333.
- ^ Котти, SRSS; Тиммонс, К. и Ли, Г. (2006). «Вицинальные диамино-функциональные группы как привилегированные структурные элементы в биологически активных соединениях и использование их синтетической химии». Химическая биология и дизайн лекарств . 67 (2): 101–114. DOI : 10.1111 / j.1747-0285.2006.00347.x . PMID 16492158 .
- ↑ Hogan DJ (январь 1990 г.). «Аллергический контактный дерматит на этилендиамин. Постоянная проблема». Dermatol Clin . 8 (1): 133–6. DOI : 10.1016 / S0733-8635 (18) 30536-9 . PMID 2137392 .
- ^ Zuidema Дж (1985-08-23). «Этилендиамин, профиль сенсибилизирующего вспомогательного вещества». Аптечный мир и наука . 7 (4): 134–40. DOI : 10.1007 / BF02097249 . PMID 3900925 .
Внешние ссылки [ править ]
СМИ, связанные с этилендиамином, на Викискладе?
- IRIS EPA Этилендиамин
- CDC - Карманный справочник NIOSH по химическим опасностям
- Химические данные

