 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Гексафторкремниевая кислота | |
| Систематическое название ИЮПАК Гексафторсиликат дигидрогена | |
| Другие названия Кремнефтористоводородная кислота, кремнефтористоводородная кислота, кремнефтористоводородная кислота, кремнефторид, кремнефтористоводородная кислота, гексафторсиландиуид оксония, гексафторидосиликат оксония (2-) | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.037.289 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1778 |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| F 6 H 2 Si | |
| Молярная масса | 144,091 г · моль -1 |
| Появление | прозрачная бесцветная дымящаяся жидкость |
| Запах | кислый, острый |
| Плотность | 1,22 г / см 3 (25% раствор) 1,38 г / см 3 (35% раствор) 1,46 г / см 3 (61% раствор) |
| Температура плавления | ок. 19 ° C (66 ° F, 292 K) (60–70% раствор) <−30 ° C (−22 ° F, 243 K) (35% раствор) |
| Точка кипения | 108,5 ° С (227,3 ° F, 381,6 К) (разлагается) |
| смешивающийся | |
Показатель преломления ( n D ) | 1,3465 |
| Состав | |
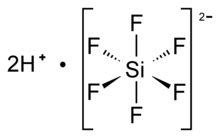
| Октаэдрический SiF 6 2− | |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Опасность |
| H314 | |
| Р260 , Р264 , Р280 , Р301 + 330 + 331 , P303 + 361 + 353 , Р304 + 340 , P305 + 351 + 338 , P310 , P321 , P363 , P405 , P501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 430 мг / кг (перорально, крыса) |
| Родственные соединения | |
Другие катионы | Гексафторсиликат аммония Фторсиликат натрия |
Родственные соединения | Гексафторфосфорная кислота Фторборная кислота |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Гексафторкремниевая кислота - неорганическое соединение с химической формулой H
2SiF
6также записывается как (H
3O)
2[SiF
6] . Это бесцветная жидкость, которая чаще всего встречается в виде разбавленного водного раствора, отсюда также предложено второе химическое обозначение. Гексафторкремниевая кислота имеет характерный кисловатый вкус и резкий запах. Он производится естественным образом в больших количествах в вулканах. [1] [2] Он производится как побочный продукт при производстве фосфорных удобрений. Полученная гексафторкремниевая кислота почти исключительно используется в качестве предшественника трифторида алюминия и синтетического криолита , которые используются при обработке алюминия. Соли, полученные из гексафторкремниевой кислоты, называются гексафторсиликатами .
Структура [ править ]
Обычно предполагается, что гексафторкремниевая кислота состоит из заряда ионов оксония, уравновешенного гексафторсиликатными дианионами, а также водой. В водном растворе катион гидроксония (H 3 O + ) традиционно приравнивается к сольватированному протону, и поэтому формула этого соединения часто записывается как H
2SiF
6. Расширяя эту метафору, изолированное соединение записывается как H
2SiF
6· 2H
2O или (H
3O)
2SiF
6Ситуация аналогична ситуации с платинохлористоводородной , фторборной и гексафторфосфорной кислотами . Гексафторсиликат - октаэдрический анион; расстояния связи Si – F составляют 1,71 Å . [3] Гексафторкремниевая кислота коммерчески доступна только в виде раствора. [4]
Производство и основные реакции [ править ]
Товарный химический фтороводород получают из флюорита обработкой серной кислотой . [5] В качестве побочного продукта получается около 50 кг (H 3 O) 2 SiF 6 на тонну HF в результате реакций с участием кремнеземсодержащих минеральных примесей. (H 3 O) 2 SiF 6 также производится как побочный продукт при производстве фосфорной кислоты из апатита и фторапатита . Опять же, часть HF, в свою очередь, реагирует с силикатными минералами, которые являются неизбежным компонентом минерального сырья, с образованиемтетрафторид кремния . Образованный таким образом тетрафторид кремния далее реагирует с HF. Сетевой процесс можно описать так: [6]
- SiO
2+ 6 ВЧ → SiF2-
6+ 2 часа
3О+
Гексафторкремниевую кислоту можно также получить обработкой тетрафторида кремния плавиковой кислотой.
В воде гексафторкремниевая кислота легко гидролизуется до плавиковой кислоты и различных форм аморфного и гидратированного кремнезема («SiO 2 »). При концентрации, обычно используемой для фторирования воды, происходит 99% гидролиз, и pH падает. Скорость гидролиза увеличивается с увеличением pH. При pH питьевой воды степень гидролиза составляет практически 100%. [7]
- H 2 SiF 6 + 2 H 2 O → 6 HF + «SiO 2 »
Нейтрализация растворов гексафторкремниевой кислоты основаниями щелочных металлов дает соответствующие фторосиликатные соли щелочных металлов:
- (H 3 O) 2 SiF 6 + 2 NaOH → Na 2 SiF 6 + 4 H 2 O
Полученная соль Na 2 SiF 6 в основном используется при фторировании воды. Аналогичным образом производятся родственные соли аммония и бария для других применений.
При pH, близком к нейтральному, соли гексафторсиликата быстро гидролизуются в соответствии с этим уравнением: [8]
- SiF2-
6 + 2 H 2 O → 6 F - + SiO 2 + 4 H +
Использует [ редактировать ]
Большая часть гексафторкремниевой кислоты превращается во фторид алюминия и синтетический криолит . [6] Эти материалы играют центральную роль в превращении алюминиевой руды в металлический алюминий . Превращение в трифторид алюминия описывается как:
- H 2 SiF 6 + Al 2 O 3 → 2 AlF 3 + SiO 2 + H 2 O
Гексафторкремниевая кислота также превращается во множество полезных солей гексафторсиликата. Соль калия, фторосиликат калия , используется в производстве фарфора, соль магния для затвердевшего бетона и в качестве инсектицида, а соли бария для люминофоров.
Гексафторкремниевая кислота также используется в качестве электролита в электролитическом процессе Беттса для рафинирования свинца.
Гексафторкремниевая кислота (обозначенная на этикетке как кремнефтористоводородная кислота) вместе с щавелевой кислотой являются активными ингредиентами, используемыми в очищающих средствах Iron Out для удаления ржавчины, которые, по сути, представляют собой разновидности кислот для стирки .
Нишевые приложения [ править ]
H 2 SiF 6 - специализированный реагент в органическом синтезе для разрыва связей Si – O силиловых эфиров . Для этого он более реактивен, чем HF. Он реагирует быстрее с т - butyldimethysilyl ( TBDMS ) простые эфиры , чем триизопропилсилил ( СОВЕТЫ ) простые эфиры. [9]
Гексафторкремниевая кислота и ее соли используются в качестве консервантов древесины . [10]
Натуральные соли [ править ]
Некоторые редкие минералы, встречающиеся в вулканических или угольных фумаролах, представляют собой соли гексафторкремниевой кислоты. Примеры включают гексафторсиликат аммония, который в природе встречается в виде двух полиморфов: криптогалита и барарита. [11] [12] [13]
Безопасность [ править ]
Гексафторкремниевая кислота может выделять фтористый водород при испарении, поэтому имеет аналогичные риски. Вдыхание паров может вызвать отек легких . Как и фтористый водород, он разрушает стекло и керамику . [14] Значение LD 50 гексафторкремниевой кислоты составляет 430 мг / кг. [15]
См. Также [ править ]
- Фторосиликат аммония
- Фторсиликат натрия
- Фторсиликат калия
Ссылки [ править ]
- ^ Palache, С. Берман, H., и Frondel, C. (1951) Система Даны минералогии, Том II: галогениды, нитраты, бораты, карбонаты, сульфаты, фосфаты, Арсенаты, Вольфраматы, молибдаты и т.д. John Wiley и Sons, Inc., Нью-Йорк, 7-е издание.
- ^ Энтони, JW, Бидо, RA, Bladh, KW, и Николс, MC (1997) Справочник по минералогии, том III: Галогениды, гидроксиды, оксиды. Издательство минеральных данных, Тусон.
- ссылка на барарите
- ссылка на криптохалит
- ^ Holleman, AF; Виберг, Э. (2001). Неорганическая химия . Сан-Диего: Academic Press. ISBN 0-12-352651-5.
- ^ JP Nicholson (2005). «Электроосаждение кремния из неводных растворителей». J. Electrochem. Soc. 152 (12): C795 – C802. DOI : 10.1149 / 1.2083227 .
- ^ USGS. Плавиковый шпат .
- ^ a b Aigueperse, J .; Mollard, P .; Devilliers, D .; Chemla, M .; Faron, R .; Romano, R .; Cuer, JP "Соединения фтора, неорганические". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a11_307 .
- ^ «Гексафторсиликат натрия [CASRN 16893-85-9] и кремнефтористоводородная кислота [CASRN 16961-83-4] Обзор токсикологической литературы» (PDF) . ntp.niehs.nih.gov . Проверено 13 июля 2017 года .
- ^ Финни, Уильям Ф .; Уилсон, Эрин; Каллендер, Эндрю; Моррис, Майкл Д .; Бек, Ларри В. (2006). «Повторное исследование гидролиза гексафторсиликата с помощью 19 F ЯМР и измерения pH». Environ. Sci. Technol . 40 (8): 2572–2577. Bibcode : 2006EnST ... 40.2572F . DOI : 10.1021 / es052295s .
- ^ Pilcher, AS; ДеШонг, П. (2001). «Кремнефтористоводородная кислота». Энциклопедия реагентов для органического синтеза . Джон Вили и сыновья. DOI : 10.1002 / 047084289X.rf013 . ISBN 0471936235.
- ^ Карстен Mai, Хольгер Militz (2004). «Модификация древесины соединениями кремния. Неорганические соединения кремния и золь-гель системы: обзор». Древесная наука и технология . 37 (5): 339. DOI : 10.1007 / s00226-003-0205-5 .
- ^ https://www.mindat.org/min-1163.html
- ^ https://www.mindat.org/min-511.html
- ^ Крушевски, л., Fabiańska, MJ, Segit, T., Kusy Д., Motyliński, R., Ciesielczuk, J., Deput, E., 2020. углерод-азотные соединения, спирты, меркаптаны, Монотерпены, ацетаты, альдегиды, кетоны, SF6, PH3 и другие горючие газы в отвалах угледобычи Верхнесилезского угольного бассейна (Польша) - повторное исследование с использованием метода внешней базы данных FTIR in situ. Sci. Всего Env., 698, 134274, DOI: 10.1016 / j.scitotenv.2019.134274
- ^ "CDC - Кремнефтористоводородная кислота - Международные карты химической безопасности - NIOSH" . Cdc.gov . Проверено 10 марта 2015 .
- ^ [1] Архивировано 22 октября 2012 года в Wayback Machine.
