 | |
 | |
| Имена | |
|---|---|
| Другие имена Хлорид галлия (III), трихлорогаллий, трихлорогаллан | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.033.268 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| Характеристики | |
| GaCl 3 | |
| Молярная масса | 176,073 г / моль |
| Внешность | бесцветные кристаллы, растворяющиеся в воздухе |
| Плотность | 2,47 г / см 3 2,053 г / см 3 при температуре плавления |
| Температура плавления | 77,9 ° C (172,2 ° F, 351,0 K) (безводный) 44,4 ° C (гидрат) |
| Точка кипения | 201 ° С (394 ° F, 474 К) |
| очень растворимый | |
| Растворимость | растворим в бензоле , CCl 4 , CS 2 |
| −63,0 · 10 −6 см 3 / моль | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 4700 мг / кг (крыса, перорально) |
| Родственные соединения | |
Другие анионы | Фторид галлия (III) Бромид галлия (III) Иодид галлия (III) |
Другие катионы | Хлорид алюминия Хлорид индия (III) Хлорид таллия (III) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Трихлорид галлия - это химическое соединение с формулой GaCl 3 . Твердый трихлорид галлия существует в виде димера с формулой Ga 2 Cl 6 . [1] Он бесцветен и растворим практически во всех растворителях, даже в алканах, что действительно необычно для галогенида металла. Это главный предшественник большинства производных галлия и реагент в органическом синтезе . [2]
Как кислота Льюиса , GaCl 3 мягче, чем трихлорид алюминия . Галлий (III) восстановить легче, чем Al (III), поэтому химический состав восстановленных соединений галлия более обширен, чем для алюминия. Ga 2 Cl 4 известен, тогда как соответствующий Al 2 Cl 4 - нет. Координационная химия Ga (III) и Fe (III) схожа, и соединения галлия (III) использовались в качестве диамагнитных аналогов соединений трехвалентного железа.
Подготовка [ править ]
Трихлорид галлия можно получить из элементов, нагревая металлический галлий в потоке хлора и очищая продукт сублимацией в вакууме. [3] [4]
- 2 Ga + 3 Cl 2 → 2 GaCl 3
Его также можно получить путем нагревания оксида галлия с тионилхлоридом : [5]
- Ga 2 O 3 + 3 SOCl 2 → 2 GaCl 3 + 3 SO 2
Металлический галлий медленно реагирует с соляной кислотой. В этой реакции медленно образуется газообразный водород .
Структура [ править ]
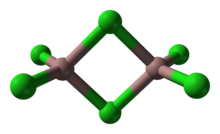
В качестве твердого вещества он имеет битетраэдрическую структуру с двумя мостиковыми хлоридами. Его структура напоминает трибромид алюминия . В отличие от AlCl 3 и InCl 3 элемент содержит 6 координатных металлических центров. Вследствие своей молекулярной природы и связанной с этим низкой энергии решетки трихлорид галлия имеет более низкую температуру плавления по сравнению с тригалогенидами алюминия и индия. Формулу Ga 2 Cl 6 часто записывают как Ga 2 (μ-Cl) 2 Cl 4 . В газовой фазе димеры диссоциируют на тригональные плоские мономеры.
Комплексы [ править ]
Галлий - самый легкий член Группы 13, который имеет полную d- оболочку (галлий имеет электронную конфигурацию [ Ar ] 3 d 10 4 s 2 4 p 1 ) ниже валентных электронов, которые могут принимать участие в d -π-связывании с лигандами. Низкая степень окисления Ga в Ga (III) Cl 3 , наряду с низкой электроотрицательностью и высокой поляризуемостью , позволяет GaCl 3 вести себя как «мягкая кислота» с точки зрения теории HSAB . Прочность связей между галогенидами галлия и лигандами широко изучалась. Что появляется:
- GaCl 3 является более слабой кислотой Льюиса, чем AlCl 3, в отношении доноров азота и кислорода, например пиридина.
- GaCl 3 является более сильной кислотой Льюиса, чем AlCl 3, по отношению к тиоэфирам, например диметилсульфиду , Me 2 S
С ионом хлорида в качестве лиганда образуется тетраэдрический ион GaCl 4 - , 6-координатный GaCl 6 3- не может быть получен. Известны соединения, подобные KGa 2 Cl 7, которые содержат мостиковый хлорид- анион. [6] В расплавленной смеси KCl и GaCl 3 существует следующее равновесие:
- 2 GaCl 4 - ⇌ Ga 2 Cl 7 - + Cl -
Использует [ редактировать ]
Органический синтез [ править ]
Трихлорид галлия является кислотным катализатором Льюиса , например, в реакции Фриделя – Крафтса , а также используется в реакциях карбогаллирования соединений с тройной углерод-углеродной связью. Это предшественник галлийорганических реагентов . [2]
Обнаружение солнечных нейтрино [ править ]
110 тонн водного раствора трихлорида галлия было использовано в экспериментах GALLEX и GNO, проведенных в Laboratori Nazionali del Gran Sasso в Италии для обнаружения солнечных нейтрино . В этих экспериментах германий -71 был произведен нейтринными взаимодействиями с изотопом галлий-71 (естественное содержание которого составляет 40%), и были измерены последующие бета-распады германия-71. [7]
См. Также [ править ]
- Галогениды галлия
Ссылки [ править ]
- Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- «Галлий» . Периодическая таблица WebElements .
- ^ Уэллс, AF (1984) Структурная неорганическая химия, Оксфорд: Clarendon Press. ISBN 0-19-855370-6 .
- ^ a b Ямагути, Масахико; Мацунага, Сигеки; Шибасаки, Масакацу; Мишле, Бастьен; Бур, Кристоф; Гандон, Винсент (2014), «Трихлорид галлия», Энциклопедия реагентов для органического синтеза , John Wiley & Sons, Ltd, стр. 1–8, doi : 10.1002 / 047084289x.rn00118u.pub3 , ISBN 9780470842898
- ^ SC Wallwork IJWorral J. Chem. Soc 1965,1816
- ^ Ковар РА "Галлий трихлорид" Неорганические синтезы, 1977, том XVII, стр 167-172. ISBN 0-07-044327-0
- ^ H.Hecht, G.Jander, H.Schlapmann Z. Anorg. Allgem. Chem. Т.254, с.255 (1947)
- ^ JH фон Барнер Inorg Chem 1985 24 1686
- ^ Дэвид Р. Лид, изд. Справочник по химии и физике, 85-е издание , Интернет-версия 2005 г. CRC Press, 2005 г.
Внешние ссылки [ править ]
- «Руководство по оказанию неотложной первой помощи - трихлорид галлия» . Агентство по охране окружающей среды США . Архивировано из оригинала на 2004-11-12.
