| |||
| |||
| |||
| Имена | |||
|---|---|---|---|
| Другие имена 2-аминоэтановая кислота, гликокол | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| Сокращения | Gly , G | ||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.248 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 2 H 5 N O 2 | |||
| Молярная масса | 75,067 г · моль -1 | ||
| Внешность | Белое твердое вещество | ||
| Плотность | 1,1607 г / см 3 [2] | ||
| Температура плавления | 233 ° С (451 ° F, 506 К) (разложение) | ||
Растворимость в воде | 24,99 г / 100 мл (25 ° C) [3] | ||
| Растворимость | растворим в пиридине умеренно растворим в этаноле нерастворим в эфире | ||
| Кислотность (p K a ) | 2,34 (карбоксил), 9,6 (амино) [4] | ||
Магнитная восприимчивость (χ) | -40,3 · 10 −6 см 3 / моль | ||
| Фармакология | |||
Код УВД | B05CX03 ( ВОЗ ) | ||
| Опасности | |||
| Паспорт безопасности | См .: страницу данных | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 2600 мг / кг (мышь, перорально) | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
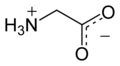
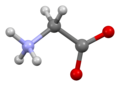
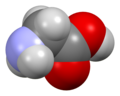
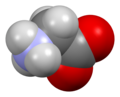
Глицин (символ Gly или G ; [5] / ɡ л aɪ с я п / ) [6] представляет собой аминокислоту , которая имеет один водородный атом в качестве своей боковой цепи . Это простейшая аминокислота (поскольку карбаминовая кислота нестабильна) с химической формулой NH 2 - CH 2 - COOH . Глицин - одна из протеиногенных аминокислот . Он кодируется всеми кодоновначиная с GG (GGU, GGC, GGA, GGG). Глицин является неотъемлемой частью образования альфа-спиралей во вторичной структуре белка из-за своей компактной формы. По той же причине это самая распространенная аминокислота в тройных спиралях коллагена . Глицин также является тормозным нейротрансмиттером - вмешательство в его высвобождение в спинном мозге (например, во время инфекции Clostridium tetani ) может вызвать спастический паралич из-за несдерживаемого мышечного сокращения.
Глицин представляет собой бесцветное кристаллическое вещество со сладким вкусом. Это единственная ахиральная протеиногенная аминокислота . Он может вписаться в гидрофильную или гидрофобную среду благодаря минимальной боковой цепи из одного атома водорода. Ацильный радикал представляет собой глицил .
История и этимология [ править ]
Глицин был открыт в 1820 году французским химиком Анри Браконно, когда он гидролизовал желатин путем кипячения его с серной кислотой . [7] Первоначально он называл его «сахаром из желатина», [8] [9] но французский химик Жан-Батист Буссинго показал, что он содержит азот. [10] Американский ученый Эбен Нортон Хорсфорд , в то время ученик немецкого химика Юстуса фон Либиха , предложил название «гликоколл»; [11] [12] однако шведский химик Берцелиус предложил более простое название «глицин». [13][14] Название происходит от греческого слова γλυκύς «сладкий вкус» [15] (которое также связано с приставками глико- и глюко- , такими как гликопротеин и глюкоза ). В 1858 году французский химик Огюст Cahours определилчто глицин был амин из уксусной кислоты . [16]
Производство [ править ]
Хотя глицин можно выделить из гидролизованного белка, он не используется в промышленном производстве, так как его удобнее производить химическим синтезом. [17] Два основных процессы аминирование хлоруксусной кислоты с аммиаком , давая глицин и аммоний хлорид , [18] и Стрекер аминокислотного синтеза , [19] , которая является основным методом синтетического в Соединенных Штатах Америки и Японии. [20] Таким способом ежегодно производится около 15 тысяч тонн . [21]
Глицин также образуется в качестве примеси при синтезе ЭДТА , возникающей в результате реакций с побочным продуктом аммиака. [22]
Химические реакции [ править ]
Наиболее важны его кислотно-основные свойства. В водном растворе глицин сам по себе является амфотерным : при низком pH молекула может быть протонирована с ap K a около 2,4, а при высоком pH она теряет протон с ap K a около 9,6 (точные значения p K a зависят от температуры и ионная сила).
Глицин действует как бидентатный лиганд для многих ионов металлов. Типичным комплексом является Cu (глицинат) 2 , т.е. Cu (H 2 NCH 2 CO 2 ) 2 , который существует как в цис-, так и в транс-изомерах.
Как бифункциональная молекула, глицин реагирует со многими реагентами. Их можно разделить на реакции с N-центром и с карбоксилатным центром.
Амин претерпевает ожидаемые реакции. С помощью хлорангидридов получают амидокарбоновую кислоту, такую как гиппуровая кислота [23] и ацетилглицин. [24] С помощью азотистой кислоты получают гликолевую кислоту ( определение Ван Слайка ). С метилиодидом амин становится кватернизованным с образованием бетаина , природного продукта:
- ЧАС
3N+
CH
2COO-
+ 3 CH 3 I → (CH
3)
3N+
CH
2COO-
+ 3 привет
Глицин конденсируется с образованием пептидов, начиная с образования глицилглицина :
- 2 ч
3N+
CH
2COO-
→ H
3N+
CH
2КОНХЧ
2COO-
+ H 2 O
Пиролиз глицина или глицилглицина дает 2,5- дикетопиперазин , циклический диамид.
Метаболизм [ править ]
Биосинтез [ править ]
Глицин не является необходимым для рациона человека , поскольку он биосинтезируется в организме из аминокислоты серина , которая, в свою очередь, является производной 3-фосфоглицерата , но метаболическая способность для биосинтеза глицина не удовлетворяет потребность в синтезе коллагена. [25] У большинства организмов фермент серингидроксиметилтрансфераза катализирует это преобразование через кофактор пиридоксальфосфата : [26]
- серин + тетрагидрофолат → глицин + N 5 , N 10 -метилентетрагидрофолат + H 2 O
В печени позвоночных синтез глицина катализируется глицинсинтазой (также называемой ферментом расщепления глицина). Это преобразование легко обратимо : [26]
- CO 2 + NH+
4+ N 5 , N 10 -метилентетрагидрофолат + NADH + H + ⇌ Глицин + тетрагидрофолат + NAD +
Деградация [ править ]
Глицин разлагается тремя путями. Преобладающий путь у животных и растений является обратным пути глицинсинтазы, упомянутому выше. В этом контексте задействованная ферментная система обычно называется системой расщепления глицина : [26]
- Глицин + тетрагидрофолат + НАД + ⇌ CO 2 + NH+
4+ N 5 , N 10 -метилентетрагидрофолат + NADH + H +
Во втором пути глицин разлагается в два этапа. Первый шаг - это процесс, обратный биосинтезу глицина из серина серин-гидроксиметилтрансферазой. Серин затем преобразуются в пируват с серином дегидратазом . [26]
В третьем пути ее деградации, глицин преобразуется в глиоксилату с помощью D-аминокислот оксидазы . Затем глиоксилат окисляется лактатдегидрогеназой печени до оксалата в НАД + -зависимой реакции. [26]
Период полувыведения глицина и его выведение из организма значительно зависит от дозы. [27] В одном исследовании период полувыведения варьировал от 0,5 до 4,0 часов. [27]
Глицин чрезвычайно чувствителен к антибиотикам, которые нацелены на фолиевую кислоту, и уровень глицина в крови резко падает в течение минуты после инъекции антибиотика. Некоторые антибиотики могут истощить более 90% глицина в течение нескольких минут после приема. [28]
Физиологическая функция [ править ]
Основная функция глицина - это предшественник белков . Большинство белков содержат лишь небольшие количества глицина, за исключением коллагена , который содержит около 35% глицина из-за его периодически повторяющейся роли в формировании спиральной структуры коллагена в сочетании с гидроксипролином . [26] [29] В генетическом коде глицин кодируется всеми кодонами, начинающимися с GG, а именно GGU, GGC, GGA и GGG.
Как биосинтетический промежуточный продукт [ править ]
В высших эукариот , δ-аминолевулиновой кислоты , ключ предшественник порфиринов , биосинтезируется из глицина и сукцинил-СоА ферментом АЛК - синтазы . Глицин обеспечивает центральную субъединицу C 2 N всех пуринов . [26]
Как нейротрансмиттер [ править ]
Глицин является тормозным нейротрансмиттером в центральной нервной системе , особенно в спинном мозге , стволе мозга и сетчатке . Когда рецепторы глицина активируются, хлорид проникает в нейрон через ионотропные рецепторы, вызывая тормозящий постсинаптический потенциал (IPSP). Стрихнин является сильным антагонистом ионотропных рецепторов глицина, а бикукуллин - слабым. Глицин является необходимым коагонистом наряду с глутаматом для рецепторов NMDA.. В отличие от ингибирующей роли глицина в спинном мозге, этому поведению способствуют ( NMDA ) глутаматергические рецепторы, которые являются возбуждающими. [30] ЛД 50 глицина 7930 мг / кг у крыс (пероральные), [31] , и это обычно приводит к смерти от гипервозбудимости.
Использует [ редактировать ]
В США глицин обычно продается двух сортов: Фармакопея США (USP) и технический. Продажи марки USP составляют от 80 до 85 процентов рынка глицина в США. Если требуется чистота выше, чем стандарт USP, например, для внутривенных инъекций, можно использовать более дорогой глицин фармацевтического качества. Глицин технической чистоты, который может соответствовать или не соответствовать стандартам качества USP, продается по более низкой цене для использования в промышленных приложениях, например, в качестве агента для комплексообразования металлов и отделки. [32]
Продукты животного и человеческого происхождения [ править ]
Глицин не широко используется в пищевых продуктах из-за его пищевой ценности, за исключением настоев. Вместо этого роль глицина в пищевой химии - ароматизатор. Он умеренно сладкий, с сахарным послевкусием. Он также обладает консервирующими свойствами, возможно, из-за его комплексообразования с ионами металлов. Комплексы глицината металлов, например глицинат меди (II) , используются в качестве добавок к корму для животных. [21]
Химическое сырье [ править ]
Глицин является промежуточным звеном в синтезе множества химических продуктов. Он используется в производстве гербицидов глифосата , [34] ипродиона , глифозина, имипротрина и эглиназина. [21] Он используется как промежуточное звено в лекарствах, таких как тиамфеникол . [ необходима цитата ]
Лабораторные исследования [ править ]
Глицин является важным компонентом некоторых растворов, используемых в методе анализа белков SDS-PAGE . Он служит буферным агентом, поддерживая pH и предотвращая повреждение образца во время электрофореза. Глицин также используется для удаления антител, меченных белками, с мембран вестерн-блоттинга, что позволяет исследовать многочисленные представляющие интерес белки из геля SDS-PAGE. Это позволяет получить больше данных из одного и того же образца, увеличивая надежность данных, уменьшая объем обработки образца и количество необходимых образцов. Этот процесс известен как зачистка.
Присутствие в космосе [ править ]
Присутствие глицина за пределами Земли было подтверждено в 2009 году на основе анализа проб, взятых в 2004 году космическим кораблем НАСА Stardust с кометы Wild 2 и впоследствии возвращенных на Землю. Глицин ранее был обнаружен в метеорите Мерчисон в 1970 году. [35] Открытие кометного глицина поддержало теорию панспермии , которая утверждает, что «строительные блоки» жизни широко распространены во Вселенной. [36] В 2016 году было объявлено об обнаружении глицина в комете 67P / Чурюмова-Герасименко космическим кораблем Rosetta . [37]
Обнаружение глицина вне Солнечной системы в межзвездной среде является предметом дискуссий. [38] В 2008 году Радиоастрономический институт им. Макса Планка обнаружил спектральные линии глициноподобной молекулы аминоацетонитрила в Большой молекуле Хеймат , гигантском газовом облаке около центра Галактики в созвездии Стрельца . [39]
Эволюция [ править ]
Несколько независимых эволюционных исследований с использованием различных типов данных показали, что глицин принадлежит к группе аминокислот, составляющих ранний генетический код. [40] [41] [42] [43] Например, участки низкой сложности (в белках), которые могут напоминать протопептиды раннего генетического кода , сильно обогащены глицином. [43]
Присутствие в пище [ править ]
| Еда | г / 100г |
|---|---|
| Закуски, шкуры свинины | 11.04 |
| Кунжутная мука (обезжиренная) | 3,43 |
| Напитки, протеиновый порошок (на основе сои ) | 2.37 |
| Семена, мука из семян сафлора, частично обезжиренная | 2.22 |
| Мясо, бизон, говядина и другие (разные части) | 1,5–2,0 |
| Желатиновые десерты | 1,96 |
| Семена, тыквы и тыквы ядра семян | 1,82 |
| Индейка, все классы, спина, мясо и кожа | 1,79 |
| Курица, бройлеры или фритюрницы, мясо и кожа | 1,74 |
| Свинина, фарш, 96% нежирная / 4% жира, вареная, в крошке | 1,71 |
| Бекон и говяжьи палочки | 1,64 |
| Арахис | 1,63 |
| Ракообразные , лангусты | 1,59 |
| Специи, семена горчицы , молотые | 1,59 |
| Салями | 1,55 |
| Орехи, орехи сушеные | 1,51 |
| Рыба, лосось, горбуша, консервы, соленые продукты | 1,42 |
| Миндаль | 1,42 |
| Рыба, скумбрия | 0,93 |
| Готовые злаки, мюсли, домашние | 0,81 |
| Лук-порей (луковица и нижняя часть листа), сублимированный | 0,7 |
| Сыр, пармезан (и др.) Тертый | 0,56 |
| Соевые бобы зеленые, вареные, вареные, сушеные, без соли | 0,51 |
| Хлеб, белок (включая глютен) | 0,47 |
| Яйцо, целое, вареное, жареное | 0,47 |
| Фасоль белая, зрелые семена, вареные, вареные, с солью | 0,38 |
| Чечевица, зрелые семена, вареные, вареные, с солью | 0,37 |
См. Также [ править ]
- Триметилглицин
- Аминокислотный нейромедиатор
Ссылки [ править ]
- ^ The Merck Index: Энциклопедия химикатов, лекарств и биологических препаратов (11-е изд.), Merck, 1989, ISBN 091191028X, 4386.
- ^ Справочник по химии и физике , CRC Press, 59-е издание, 1978
- ^ «Растворимость и плотности» . Prowl.rockefeller.edu . Проверено 13 ноября 2013 .
- ^ Доусон, RMC и др., Данные для биохимических исследований , Оксфорд, Clarendon Press, 1959.
- ^ «Номенклатура и символика аминокислот и пептидов» . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из оригинала 9 октября 2008 года . Проверено 5 марта 2018 .
- ^ «Глицин | Определение глицина на английском языке Оксфордскими словарями» .
- ^ Плиммер, RHA (1912) [1908]. Плиммер, RHA; Хопкинс, Ф.Г. (ред.). Химический состав белков . Монографии по биохимии. Часть I. Анализ (2-е изд.). Лондон: Longmans, Green and Co., стр. 82 . Проверено 18 января 2010 года .
- ^ Браконно, Анри (1820). "Sur la conversion des matières animales en nouvelles elements par le moyen de l'acide sulfique" [О преобразовании материалов животного происхождения в новые вещества с помощью серной кислоты]. Annales de Chimie et de Physique . 2-я серия (на французском языке). 13 : 113–125. ; см. стр. 114.
- ^ Маккензи, Колин (1822). Тысяча опытов в химии: с иллюстрациями природных явлений; и практические наблюдения за производственными и химическими процессами, которые в настоящее время проводятся для успешного выращивания полезных искусств… . Сэр Р. Филлипс и компания. п. 557 .
- ^ Буссенго (1838). "Sur la композиция du sucre de gélatine et de l'acide nitro-saccharique de Braconnot" [О составе сахара желатина и нитроглюкаровой кислоты Браконно]. Comptes Rendus (на французском). 7 : 493–495.
- ^ Хорсфорд, EN (1847). «Гликоколл (желатиновый сахар) и некоторые продукты его разложения» . Американский журнал науки и искусства . 2-я серия. 3 : 369–381.
- ^ Ihde, Аарон Дж. (1970). Развитие современной химии . Курьерская корпорация. ISBN 9780486642352.
- ^ Берцелиус, Якоб (1848). Jahres-Bericht über die Fortschritte der Chemie und Mineralogie (Годовой отчет о прогрессе в химии и минералогии) . т. 47. Tübigen, (Германия): Laupp. п. 654. С п. 654: «Er hat dem Leimzucker als Basis den Namen Glycocoll gegeben.… Glycin genannt werden, und diesen Namen werde ich anwenden». (Он [то есть, американский ученый Эбен Нортон Хорсфорд , в то время ученик немецкого химика Юстуса фон Либиха ] дал название «гликоколл» Леймцукеру (желатиновому сахару), основе. что он противоречит названиям остальных основ. Он составлен из γλυχυς (сладкий) и χολλα (животный клей). Поскольку эта органическая основа - единственная [одна], имеющая сладкий вкус, то ее можно гораздо более кратко назвать «глицин», и я буду использовать это имя.)
- ↑ Най, Мэри Джо (1999). Перед большой наукой: стремление к современной химии и физике, 1800-1940 гг . Издательство Гарвардского университета. ISBN 9780674063822.
- ^ «глицин» . Оксфордские словари . Проверено 6 декабря 2015 .
- ^ Cahours, A. (1858). "Recherches sur les acides amidés" [Исследования аминированных кислот]. Comptes Rendus (на французском). 46 : 1044–1047.
- ^ Okafor, Nduka (2016-03-09). Современная промышленная микробиология и биотехнология . CRC Press. ISBN 9781439843239.
- ^ Ингерсолл, AW; Бэбкок, SH (1932). «Гиппуровая кислота» . Органический синтез . 12 : 40.; Сборник , 2 , стр. 328
- ^ Wiley (2007-12-14). Kirk-Othmer Food and Feed Technology, набор из 2 объемов . Джон Вили и сыновья. ISBN 9780470174487.
- ^ "Глицин конференция (предварительная)" . USITC. Архивировано 22 февраля 2012 года . Проверено 13 июня 2014 .CS1 maint: bot: original URL status unknown (link)
- ^ a b c Драуз, Карлхайнц; Грейсон, Ян; Климанн, Аксель; Криммер, Ханс-Петер; Лойхтенбергер, Вольфганг и Векбекер, Кристоф (2007). "Аминокислоты". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH.
- ^ Харт, Дж. Роджер (2005). «Этилендиаминтетрауксусная кислота и родственные хелатирующие агенты». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a10_095 .
- ^ Ингерсолл, AW; Бэбкок, SH (1932). «Гиппуровая кислота». Орг. Synth . 12 : 40. DOI : 10,15227 / orgsyn.012.0040 .
- ^ Herbst, RM; Шемин, Д. (1939). «Ацетилглицин». Орг. Synth . 19 : 4. DOI : 10,15227 / orgsyn.019.0004 .
- ^ Мелендес Hevia, Е; Де Пас-Луго, П; Корниш-Боуден, А ; Карденас, ML (декабрь 2009 г.). «Слабое звено в метаболизме: метаболическая способность для биосинтеза глицина не удовлетворяет потребность в синтезе коллагена». Журнал биологических наук . 34 (6): 853–72. DOI : 10.1007 / s12038-009-0100-9 . PMID 20093739 . S2CID 2786988 .
- ^ a b c d e f g Нельсон, Дэвид Л .; Кокс, Майкл М. (2005). Принципы биохимии (4-е изд.). Нью-Йорк: У. Х. Фриман. С. 127, 675–77, 844, 854. ISBN 0-7167-4339-6.
- ^ а б Хан Р.Г. (1993). «Дозозависимый период полувыведения глицина». Урологическое исследование . 21 (4): 289–291. DOI : 10.1007 / BF00307714 . PMID 8212419 . S2CID 25138444 .
- ^ ACS Chem Biol. 2010 Aug 20; 5 (8): 787–795. DOI: 10.1021 / cb100096f
- ^ Шпак, Paul (2011). «Химия и ультраструктура костей рыб: значение для тафономии и анализа стабильных изотопов» . Журнал археологической науки . 38 (12): 3358–3372. DOI : 10.1016 / j.jas.2011.07.022 .
- ^ «Недавние разработки в рецепторах NMDA» . Китайский медицинский журнал. 2000 г.
- ^ «Данные по безопасности (MSDS) для глицина» . Лаборатория физической и теоретической химии Оксфордского университета. 2005. Архивировано из оригинала на 2007-10-20 . Проверено 1 ноября 2006 .
- ^ «Глицин из Японии и Кореи» (PDF) . Комиссия по международной торговле США. Январь 2008 . Проверено 13 июня 2014 .
- ^ Casari, BM; Махмудхани, AH; Лангер, В. (2004). « Повторное определение цис- аквабис (глицинато-κ 2 N, O ) меди (II)». Acta Crystallogr. E . 60 (12): m1949 – m1951. DOI : 10.1107 / S1600536804030041 .
- ^ Stahl, Shannon S .; Альстерс, Пол Л. (13.07.2016). Жидкофазный аэробный окислительный катализ: промышленное применение и академические перспективы . Джон Вили и сыновья. ISBN 9783527690152.
- ^ Квенволден, Кейт А .; Лоулесс, Джеймс; Перинг, Кэтрин; Петерсон, Этта; Флорес, Хосе; Поннамперума, Кирилл; Каплан, Исаак Р .; Мур, Карлтон (1970). «Доказательства наличия внеземных аминокислот и углеводородов в метеорите Мерчисон». Природа . 228 (5275): 923–926. Bibcode : 1970Natur.228..923K . DOI : 10.1038 / 228923a0 . PMID 5482102 . S2CID 4147981 .
- ^ «Строительный блок жизни, найденный на комете - Thomson Reuters 2009» . Рейтер . 18 августа 2009 . Проверено 18 августа 2009 .
- ^ Европейское космическое агентство (27 мая 2016 г.). «Комета Розетты содержит ингредиенты для жизни» . Проверено 5 июня 2016 .
- ^ Снайдер Л. Е., Ловас Ф. Дж., Холлис Дж. М. и др. (2005). «Строгая попытка проверить межзвездный глицин». Astrophys Дж . 619 (2): 914–930. arXiv : astro-ph / 0410335 . Bibcode : 2005ApJ ... 619..914S . DOI : 10.1086 / 426677 . S2CID 16286204 .
- ^ Персонал. «Органическая молекула, похожая на аминокислоту, найдена в созвездии Стрельца, 27 марта 2008 г. - Science Daily» . Проверено 16 сентября 2008 .
- ^ Трифонов, EN (декабрь 2000). «Согласованный временной порядок аминокислот и эволюция триплетного кода» . Джин . 261 (1): 139–151. DOI : 10.1016 / S0378-1119 (00) 00476-5 . PMID 11164045 .
- ^ Хиггс, Пол G .; Пудриц, Ральф Э. (июнь 2009 г.). «Термодинамическая основа для синтеза пребиотических аминокислот и природа первого генетического кода» . Астробиология . 9 (5): 483–490. arXiv : 0904.0402 . Bibcode : 2009AsBio ... 9..483H . DOI : 10.1089 / ast.2008.0280 . ISSN 1531-1074 . PMID 19566427 . S2CID 9039622 .
- ^ Chaliotis, Anargyros; Властаридис, Панайотис; Мосиалос, Димитрис; Ибба, Майкл; Becker, Hubert D .; Статопулос, Константинос; Амуциас, Григориос Д. (17 февраля 2017 г.). «Сложная эволюционная история аминоацил-тРНК синтетаз» . Исследования нуклеиновых кислот . 45 (3): 1059–1068. DOI : 10.1093 / NAR / gkw1182 . ISSN 0305-1048 . PMC 5388404 . PMID 28180287 .
- ^ а б Нтунтуми, Криса; Властаридис, Панайотис; Мосиалос, Димитрис; Статопулос, Константинос; Илиопулос, Иоаннис; Промпонас, Василиос; Оливер, Стивен Дж. Амуциас, Григорис Д. (04.11.2019). «Области низкой сложности в белках прокариот выполняют важные функциональные роли и являются высококонсервативными» . Исследования нуклеиновых кислот . 47 (19): 9998–10009. DOI : 10.1093 / NAR / gkz730 . ISSN 0305-1048 . PMC 6821194 . PMID 31504783 .
- ^ "Национальная база данных по питательным веществам для стандартной справки" . Министерство сельского хозяйства США. Архивировано из оригинала на 2015-03-03 . Проверено 7 сентября 2009 . Cite journal requires
|journal=(help)
Дальнейшее чтение [ править ]
- Куан Ю.Дж., Чарнли С.Б., Хуанг Х.С. и др. (2003). «Межзвездный глицин» . Astrophys Дж . 593 (2): 848–867. Bibcode : 2003ApJ ... 593..848K . DOI : 10.1086 / 375637 .
- Новак, Рэйчел. «Аминокислота, обнаруженная в глубоком космосе - 18 июля 2002 г. - New Scientist » . Проверено 1 июля 2007 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме глицина . |
- Глицин MS Spectrum
- Глицин на PDRHealth.com
- Система расщепления глицином
- Глициновая терапия - новое направление в лечении шизофрении?
- «Органическая молекула, похожая на аминокислоту, найдена в созвездии Стрельца» . ScienceDaily . 27 марта 2008 г.
- Цай, Гочуань Э. (1 декабря 2008 г.). «Новый класс антипсихотических средств: усиление нейротрансмиссии, опосредованной рецепторами NMDA» . Психиатрические времена . 25 (14).
- ChemSub Online (Глицин) .
- Ученые НАСА обнаружили глицин, фундаментальный строительный блок жизни, в образцах кометы Wild 2, возвращенных космическим кораблем НАСА Stardust.