 | |
Chloride.jpg/440px-Hexamminecobalt(III)Chloride.jpg) | |
| Имена | |
|---|---|
| Название ИЮПАК Гексаамминкобальта (III) хлорид | |
| Другие имена Гексамминхлорид кобальта, хлорид гексаамминкобальта (III) | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.991 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| H 18 N 6 Cl 3 Co | |
| Молярная масса | 267,48 г / моль |
| Внешность | желтые или оранжевые кристаллы |
| Плотность | 1,71 г / см 3 , |
| Температура плавления | разлагается |
| 0,26 M (20 ° C) трибромид: 0,04 M (18 ° C) | |
| Растворимость | растворим в NH 3 |
| Структура | |
| восьмигранный | |
| 0 Д | |
| Опасности | |
| Основные опасности | яд |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H315 , H319 , H335 | |
| Р261 , Р264 , Р271 , Р280 , Р302 + 352 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , Р405 , Р501 | |
| Родственные соединения | |
Другие анионы | [Co (NH 3 ) 6 ] Br 3 [Co (NH 3 ) 6 ] (OAc) 3 |
Другие катионы | [Cr (NH 3 ) 6 ] Cl 3 [Ni (NH 3 ) 6 ] Cl 2 |
Родственные соединения | [Co (H 2 NCH 2 CH 2 NH 2 ) 3 ] Cl 3 [Co (NH 3 ) 5 (H 2 O)] Cl 3 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
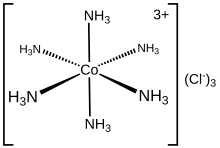
Хлорид гексаамминкобальта (III) представляет собой химическое соединение с формулой [Co (NH 3 ) 6 ] Cl 3 . Это хлоридная соль координационного комплекса [Co (NH 3 ) 6 ] 3+ , который считается архетипическим «комплексом Вернера», названным в честь пионера координационной химии Альфреда Вернера . Сам катион представляет собой комплекс аммиака металла с шестью аммиачными лигандами, присоединенными к иону кобальта (III).
Первоначально соли [Co (NH 3 ) 6 ] 3+ были описаны как лютео (латинское: желтый) комплекс кобальта. Это название было отброшено, поскольку современная химия считает цвет менее важным, чем молекулярная структура. У других подобных комплексов также были названия цветов, такие как purpureo (латинское: пурпурный) для комплекса пентаммина кобальта и praseo (по-гречески: зеленый) и violeo (латинское: фиолетовый) для двух изомерных комплексов тетраммина. [1]
Свойства и структура [ править ]
[Co (NH 3 ) 6 ] 3+ является диамагнитным с низкоспиновым 3d 6 октаэдрическим центром Co (III). Катион подчиняется правилу 18-электронов и считается классическим примером обменного комплекса инертного металла. В качестве проявления инертности [Co (NH 3 ) 6 ] Cl 3 можно перекристаллизовать без изменений из концентрированной соляной кислоты : NH 3 настолько прочно связан с центрами Co (III), что не диссоциирует, позволяя протонировать. Напротив, лабильные комплексы с аммиаками металлов, такие как [Ni (NH 3 ) 6 ] Cl 2, быстро реагируют с кислотами, отражая лабильность связей Ni (II) –NH 3 . При нагревании гексамминкобальт (III) начинает терять часть своих амминных лигандов, в конечном итоге образуя более сильный окислитель.
Ионы хлора в [Co (NH 3 ) 6 ] Cl 3 могут быть обменены с множеством других анионов, таких как нитрат , бромид , йодид , сульфамат, с получением соответствующего производного [Co (NH 3 ) 6 ] X 3 . Такие соли оранжевого или ярко-желтого цвета и обладают различной степенью растворимости в воде. Хлорид-ион также может быть заменен более сложными анионами, такими как гексатиоцианатохромат (III), давая розовое соединение с формулой [Co (NH 3 ) 6 ] [Cr (SCN) 6 ] или феррицианид ион.
Подготовка [ править ]
[Со (NH 3 ) 6 ] Cl 3 получают обработкой кобальта (II) , хлорид с аммиаком и аммония хлорида с последующим окислением. Окислители включают перекись водорода или кислород в присутствии угольного катализатора. [2] Об этой соли, по-видимому, впервые сообщил Фреми. [3]
Соли ацетата может быть получен путем аэробного окисления кобальта (II) ацетат , ацетат аммония и аммиак в метаноле. [4] Ацетатная соль хорошо растворима в воде до уровня 1,9 M (20 ° C) по сравнению с 0,26 M для трихлорида.
Использует [ редактировать ]
[Co (NH 3 ) 6 ] 3+ является компонентом некоторых методов структурной биологии (особенно для ДНК или РНК , где положительные ионы стабилизируют третичную структуру фосфатного остова), чтобы помочь определить их структуры с помощью рентгеновской кристаллографии [5] или ядерным магнитным резонансом . [6] В биологической системе противоионами, более вероятно, были бы Mg 2+ , но тяжелые атомы кобальта (или иногда иридия , как в PDB : 2GIS ) обеспечивают аномальное рассеяние для решения проблемыфазовой задачи и построить карту электронной плотности структуры. [7]
[Co (NH 3 ) 6 ] 3+ представляет собой необычный пример водорастворимого комплекса трехвалентного металла и полезен для приложений, экранирующих заряд, таких как стабилизация сильно отрицательно заряженных комплексов, таких как взаимодействия с нуклеиновыми кислотами и между ними .
Ссылки [ править ]
- ^ Хухи, Джеймс Э. (1983). Неорганическая химия (3-е изд.). п. 360.
- ^ Bjerrum, J .; Макрейнольдс, JP (1946). Соли гексамминкобальта (III) . Неорг. Synth. Неорганические синтезы. 2 . С. 216–221. DOI : 10.1002 / 9780470132333.ch69 . ISBN 9780470132333.
- ^ Fremy, ME (1852). "Исследования по кобальту" . Анна. Чим. Phys. 35 : 257–312.
- ^ Lindholm, RD; Бауза, Дэниел Э. (1978). Комплексы кобальт, содержащие аммиак или этилендиамин: соли гексаамминкобальта (III) . Неорг. Synth. Неорганические синтезы. 18 . С. 67–69. DOI : 10.1002 / 9780470132494.ch14 . ISBN 9780470132494.
- ^ Рамакришнан, Б .; Сехаруду, Ц .; Пан, В .; Сундаралингам, М. (2003). «Кристаллическая структура с близким к атомному разрешению декамером A-ДНК d (CCCGATCGGG): взаимодействие гексаммина кобальта с A-ДНК». Acta Crystallogr . D59 (Pt 1): 67–72. DOI : 10.1107 / s0907444902018917 . PMID 12499541 .
- ^ Rudisser, S .; Тиноко, И., младший (2000). «Структура раствора гексаммина кобальта (III) в комплексе с тетрапетлей GAAA, и связывание ионов металла с несоответствиями GA». J. Mol. Биол . 295 (5): 1211–1232. DOI : 10.1006 / jmbi.1999.3421 . PMID 10653698 .
- ^ Макферсон, Александр (2002). Введение в кристаллографию макромолекул . Джон Вили и сыновья. ISBN 0-471-25122-4.